
【题目】实验室制取的乙烯常含有少量二氧化硫,现设计如下实验,确认混合气体中有乙烯和二氧化硫。
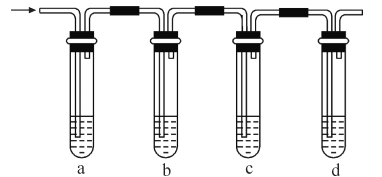
(1)a、b、c、d装置可盛放的试剂是:a_______,b________,c_______,d_______
A.品红溶液 B.NaOH溶液 C.浓硫酸 D.酸性高锰酸钾溶液
(2)b装置的作用是________________________________
(3)确定混合气体中含有乙烯的现象是_____________________
【答案】A B A D 除去SO2 c装置中品红溶液不褪色,d装置中酸性高锰酸钾溶液褪色
【解析】
由于乙烯和二氧化硫都能使溴水和酸性高锰酸钾溶液褪色,因此要想验证气体的成分,首先应该经混合气体通过品红溶液,利用二氧化硫的漂白性验证二氧化硫的存在,由于二氧化硫是酸性氧化物,能够与碱发生反应,所以再用NaOH将其吸收除去,并用品红溶液验证二氧化硫已经除干净,最后用酸性高锰酸钾溶液来证明乙烯气体的存在。
(1) 根据分析可知,a、b、c、d装置可盛放的试剂是:a为A,b为B,c为A,d为D;
(2) b装置用NaOH将SO2吸收除去;
(3) 确定混合气体中含有乙烯要先确认没有二氧化硫,所以现象是:c装置中品红溶液不褪色,d装置中酸性高锰酸钾溶液褪色。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】某学生用如图所示装置做浓硫酸和蔗糖反应的实验。下列有关实验操作或叙述错误的是( )
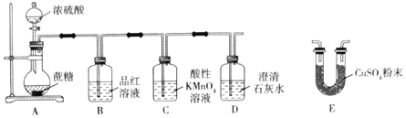
A.打开A中分液漏斗活塞,加入浓硫酸,充分反应后烧瓶内出现黑色膨化固体
B.品红溶液红色褪去,证明有SO2气体生成
C.检验A中产生的气体中含有水蒸气,应将E接在A和B之间
D.D中溶液变浑浊,即可证明反应产生了CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两种气态烃组成的混合气体完全燃烧后得到CO2和H2O的物质的量随混合烃的总物质的量的变化如图所示,则下列对混合烃的判断正确的是( )
①一定有乙烯;②一定有甲烷;③一定有丙烷;④一定无乙烷;⑤可能有乙烷;⑥可能有丙炔。

A. ②③⑤B. ⑤⑥C. ①②D. ②④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚合物F的合成路线图如下:
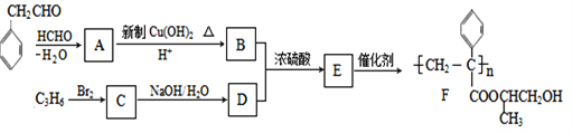
已知:HCHO+RCH2CHO![]()
请据此回答:
(1)A中含氧官能团名称是_____,D的系统命名为_____。
(2)检验B中含氧官能团所用的试剂是____;A→B的反应类型是_____。
(3)C生成D的反应化学方程式为_______,E合成F的反应化学方程式为________。
(4)G物质与![]() 互为同系物,且G物质的相对分子质量比
互为同系物,且G物质的相对分子质量比![]() 大14的,则符合下列条件的G的同分异构体有____种。
大14的,则符合下列条件的G的同分异构体有____种。
①分子中含有苯环,且苯环上有两个取代基
②遇氯化铁溶液变紫色
③能与溴水发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NOx是大气污染的主要污染物之一。
(1)NOx能形成酸雨,写出NO2完全转化为HNO3的总反应的化学方程式:_______________________
(2)硝酸厂常用如下两种方法处理NOx尾气。
①催化还原法:在催化剂存在时用H2将NO2还原为N2,写出该反应的化学方程式:_________________
②碱液吸收法:用Na2CO3溶液吸收NO2生成CO2,若9.2gNO2和Na2CO3溶液完全反应时转移0.1 mol电子,则反应的离子方程式为______________________________
(3)在汽车尾气系统中装置催化转化器,可有效降低NOx的排放。
①当尾气中空气不足时,NO在催化转化器中被还原成N2排出。写出NO被CO还原的化学方程式:_______________________________
②当尾气中空气过量时,催化转化器中的金属氧化物吸收NOx生成盐。第II A族金属氧化物吸收能力顺序如下:12 MgO<20CaO<38SrO<56BaO。原因是___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷酸铁(FePO4)常用作电极材料、陶瓷及制药等。以硫铁矿(主要成分是FeS2及少量SiO2、Fe3O4)为原料制备磷酸铁的流程如下:
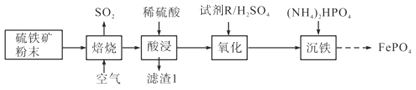
(1)焙烧时FeS2转化为Fe2O3,该反应中氧化剂与还原剂物质的量之比为___________。
(2)“酸浸”时为加速溶解,采取的措施有_________________________________(任写两种)。
(3)滤渣1是___________。
(4)氧化步骤是将少量的Fe2+转化为Fe3+,试剂R最好选择___________(填字母)。
A.KMnO4 B.H2O2 C.稀硝酸
(5)写出沉铁时反应的离子方程式______________________________________________。
(6)1 t硫铁矿中含FeS2 a mol、Fe3O4 b mol,按上述流程生成c t的FePO4,则FePO4的产率为__________________。(用含a、b、c的算式表示,不必化简)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于化学反应速率说法正确的是( )
A.对于A(s)+B(g)![]() 2C(g)的反应,增加A的质量,反应速率加快
2C(g)的反应,增加A的质量,反应速率加快
B.对于反应N2O5![]() 2NO2+O2(正反应吸热),升高温度,v(正)减小,v(逆)增大
2NO2+O2(正反应吸热),升高温度,v(正)减小,v(逆)增大
C.恒温恒容下反应2SO2(g)+O2(g)![]() 2SO3(g),充入氦气不改变化学反应速率
2SO3(g),充入氦气不改变化学反应速率
D.1 mol·L-1稀盐酸与锌反应时,加入少量3 mol·L-1稀硝酸,生成H2的速率加快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锰的化合物在工业生产和化学实验中应用广泛,请按要求回答下列问题。
(1)酸性KMnO4溶液可吸收空气污染物甲醛(CH2O),吸收过程中,高锰酸钾溶液逐渐褪色,则甲醛体现___________性。
(2)普通锌锰干电池的总反应为:2MnO2+Zn+2NH4Cl=2MnO(OH)+ZnCl2+2NH3,则放电时MnO2作___________极。(填“正”或“负”)
(3)MnO2能作为双氧水分解的催化剂,其反应可分两步。
第一步为氧化,对应化学方程式为:MnO2+H2O2=Mn(OH)2+O2
第二步为还原,对应化学方程式为:____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上可利用电解原理间接氧化法降解处理含有机污染物的废水,其原理如图所示,下列说法错误的是

A.介质离子在电极A上发生氧化反应,电极A为阳极
B.介质离子被氧化得到的强氧化剂可能为Cl2、O2
C.有机污染物在石墨电极上被还原为无污染物质
D.若介质离子为OH-,电极B上发生的反应为2H2O+2e-=H2↑+ 2OH-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com