
【题目】已知:①A的产量通常用来衡量一个国家的石油化工水平;②2CH3CHO+O2![]() 2CH3COOH。现以A为主要原料合成化合物E,其合成路线如图1所示。回答下列问题:
2CH3COOH。现以A为主要原料合成化合物E,其合成路线如图1所示。回答下列问题:

(1)写出下列物质的官能团名称:B:____________________;D:____________________。
(2)反应④的化学方程式为________________________________________________,反应类型:________。
(3)某学习小组设计物质B催化氧化的实验装置如下,根据图2装置回答问题。

①装置甲锥形瓶中盛放的固体药品可能为________(填字母)。
A.Na2O2 B.KClC.Na2CO3 D.MnO2
②实验过程中,丙装置硬质玻璃管中发生反应的化学方程式为_______________________________。
③物质B的催化氧化产物与葡萄糖具有相同的特征反应,将所得的氧化产物滴加到新制氢氧化铜悬浊液中加热,现象为______________________________________________。
【答案】羟基 羧基 CH3CH2OH+CH3COOH![]() CH3COOCH2CH3+H2O 取代反应(或酯化反应) AD 2CH3CH2OH+O2
CH3COOCH2CH3+H2O 取代反应(或酯化反应) AD 2CH3CH2OH+O2![]() 2CH3CHO + 2H2O 产生砖红色沉淀
2CH3CHO + 2H2O 产生砖红色沉淀
【解析】
A是石油裂解气的主要成份,A的产量通常用来衡量一个国家的石油化工水平,则A为CH2=CH2,与水发生加成反应生成B为CH3CH2OH,乙醇氧化生成C为CH3CHO,CH3CHO进一步氧化可得D为CH3COOH,E是一种无色透明、有香味的油状液体,CH3COOH与CH3CH2OH发生酯化反应生成E为CH3COOCH2CH3,F为高分子化合物,乙烯发生加聚反应生成F为![]() ,结合有机物的结构和性质解答该题。
,结合有机物的结构和性质解答该题。
A是石油裂解气的主要成份,A的产量通常用来衡量一个国家的石油化工水平,则A为CH2=CH2,与水发生加成反应生成B为CH3CH2OH,乙醇氧化生成C为CH3CHO,CH3CHO进一步氧化可得D为CH3COOH,E是一种无色透明、有香味的油状液体,CH3COOH与CH3CH2OH发生酯化反应生成E为CH3COOCH2CH3,F为高分子化合物,乙烯发生加聚反应生成F为![]() ;
;
(1)B为CH3CH2OH,D为CH3COOH,B、D分子中的官能团名称分别是:羟基、羧基;
(2)反应④为乙醇和乙酸的酯化反应,发生反应的化学方程式为CH3CH2OH+CH3COOH![]() CH3COOCH2CH3+H2O;
CH3COOCH2CH3+H2O;
(3)在乙醇的催化氧化的实验中,根据装置图可知,装置甲用于产生氧气,可以用双氧水和二氧化锰,也可以用过氧化钠和水反应,装置乙用水浴加热产生乙醇蒸气,与氧氧混合,通过丙装置中的铜网作催化剂,丁装置用冷水冷却得到产物;
①根据上面的分析可知,装置甲用于产生氧气,可以用双氧水和二氧化锰,也可以用过氧化钠和水反应,故答案为AD;
②实验过程中,丙装置硬质玻璃管中铜网作催化剂,乙醇被氧化成乙醛,反应的化学方程式为2CH3CH2OH+O2![]() 2CH3CHO + 2H2O;
2CH3CHO + 2H2O;
③乙醇被氧化成乙醛,书本滴加到新制氢氧化铜悬浊液中加热会产生砖红色沉淀。


科目:高中化学 来源: 题型:
【题目】如图所示装置(气密性良好),若先将甲中液体滴入丙中,观察到气球明显鼓起,一段时间后恢复原状;再将乙中液体滴入丁中,气球又明显鼓起。下列组合正确的是( )

选项 | 滴管甲 | 烧杯丙 | 滴管乙 | 烧杯丁 |
A | 双氧水 | 二氧化锰 | 水 | 氢氧化钙 |
B | 稀硫酸 | 镁 | 盐酸 | 碳酸钙 |
C | 水 | 氢氧化钠 | 水 | 硝酸铵 |
D | 水 | 氧化钙 | 盐酸 | 镁 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸钾(K2FeO4)是一种集强氧化性、吸附、絮凝于一体的新型多功能处理剂,其生产工艺如图所示:
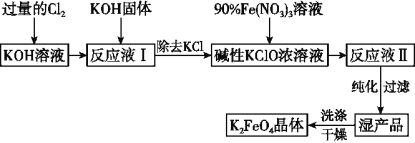
已知K2FeO4具有下列性质:
①可溶于水、微溶于浓KOH溶液
②在0~5 ℃、强碱性溶液中比较稳定
③在Fe3+和Fe(OH)3催化作用下发生分解
④在酸性至碱性条件下,能与水反应生成Fe(OH)3和O2
请完成下列填空:
(1)已知Cl2与KOH在较高温度下反应生成KClO3。在不改变KOH溶液的浓度和体积的条件下,生产KClO应在温度___________的情况下进行(填“较高”或“较低”)。
(2)生产K2FeO4的反应原理是:Fe(NO3)3+KClO+KOH→K2FeO4+KNO3+KCl+H2O(未配平),则该反应中氧化剂与还原剂的物质的量之比为______________。
(3)K2FeO4在弱碱性条件下能与水反应生成Fe(OH)3和O2,则该反应的化学方程式为________________。
(4)在“反应液Ⅰ”中加KOH固体的目的是___________。
A. 为下一步反应提供反应物
B. 与“反应液Ⅰ”中过量的Cl2继续反应,生成更多的KClO
C. KOH固体溶解时会放出较多的热量,有利于提高反应速率
D. 使副产物KClO3转化为KCl
(5)制备K2FeO4时,须将90%的Fe(NO3)3溶液缓慢滴加到碱性的KClO浓溶液中,并且不断搅拌。采用这种混合方式的原因是_______________________ (答出1条即可)。
(6)从“反应液Ⅱ”中分离出K2FeO4晶体后,可以得到的副产品有________ (写化学式)。
(7)工业上常用“间接碘量法”测定高铁酸钾样品中高铁酸钾的含量,其方法是:用碱性的碘化钾溶液(pH为11~12)溶解3.96 g高铁酸钾样品,调节pH为1,避光放置40分钟至反应完全(高铁酸根离子全部被还原成铁离子),再调节pH为3~4(弱酸性)。以1.0 mol/L的硫代硫酸钠标准溶液为滴定剂进行滴定(2Na2S2O3+I2=Na2S4O6+2NaI),当达到滴定终点时,用去硫代硫酸钠标准溶液15.00 mL,则原高铁酸钾样品中高铁酸钾的质量分数为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含氮的化合物广泛存在于自然界,是一类非常重要的化合物.回答下列有关问题:
(1)在一定条件下;2N2(g)+6H2O(g)=4NH3(g)+3O2(g)。已知该反应相关的化学键键能数据如表一:
表一:
化学键 | | H-O | N-H | O=O |
E/(kJ/mol) | 946 | 463 | 391 | 496 |
则该反应的△H=___________kJ/mol
(2)在恒容密闭容器中充入2 molNO2与1molO2发生反应如下:
4NO2(g)+O2(g)![]() 2N2O5(g)
2N2O5(g)
①已知在不同温度下测得N2O5的物质的量随时间的变化如图1所示.常温下,该反应能逆向自发进行,原因是____________________________________________。
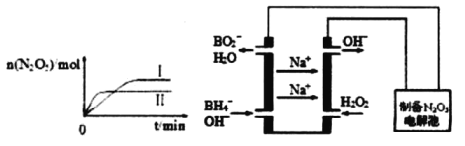
②下列有关该反应的说法正确的是___________。
A.扩大容器体积,平衡向逆反应方向移动,混合气体颜色变深
B.恒温恒容,再充入2molNO2和1molO2,再次达到平衡时NO2转化率增大
C.恒温恒容,当容器内的密度不再改变,则反应达到平衡状态
D.若该反应的平衡常数增大,则一定是降低了温度
(3)N2O5是一种新型绿色硝化剂,其制备可以用硼氢化钠燃料电池作电源,采用电解法制备得到N2O5,工作原理如图。则硼氢化钠燃料电池的负极反应式为______________________。
(4)X、Y、Z、W分别是HNO3、NH4NO3、NaOH、NaNO2四种强电解质中的一种。下表二是常温下浓度均为0.01mol/L的X、Y、Z、W溶液的pH。将X、Y、Z各lmol同时溶于水中得到混合溶液,则混合溶液中各离子的浓度由大到小的顺序为______________________。
0.01mol/L的溶液 | X | Y | Z | W |
pH | 12 | 2 | 8.5 | 4.5 |
(5)氮的氧化物与悬浮在大气中的海盐粒子相互作用时,涉及如下反应:
I: 2NO2(g)+NaCl(s)![]() NaNO3(s)+ClNO(g) K1
NaNO3(s)+ClNO(g) K1
II: 2NO(g)+Cl2(g)![]() 2ClNO(g) K2
2ClNO(g) K2
①4NO2(g)+2NaCl(s)![]() 2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K=___________(用K1、K2表示)
2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K=___________(用K1、K2表示)
②在恒温条件下,向2L恒容密闭容器中加入0.2molNO和0.1molCl2,10min时反应Ⅱ达到平衡测得10min内v(ClNO)=7.5×10-3mol/(L·min),则平衡时NO的转化率α1=___________;其他条件不变,反应Ⅱ在恒压条件下进行,平衡时NO的转化率α2=___________α1 (填“>”“<”或“=”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】增塑剂DCHP可由环己醇制得。DCHP和环己醇的结构简式如图所示,下列说法错误的是( )
![]()
环己醇
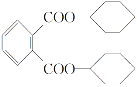
DCHP
A. DCHP的分子式为C20H26O4
B. 环己醇分子中所有碳原子不可能共平面
C. DCHP的一氯取代物有5种
D. DCHP通过取代反应可以得到环己醇
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于硅的说法中正确的是
A.硅的化学性质很稳定,常温下不能与其他物质发生反应
B.硅在自然界中的含量很大,自然界中存在大量的单质硅
C.高纯度的硅被用于制作计算机芯片
D.高纯度的硅常被用来制造光导纤维
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于反应能量的说法正确的是
A. 若反应A=B △H<0,说明A物质比B物质稳定,分子内共价键键能 A比B大
B. 500 ℃、30 Mpa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g), 放热 akJ,热化学方程式为:N2(g)+3H2(g)![]() 2NH3(g) △H= -2a kJmol-1
2NH3(g) △H= -2a kJmol-1
C. 101kPa时,2H2(g)+O2(g)==2H2O(g);△H=-QkJ·mol-1,则H2的燃烧热为1/2QkJ·mol-l
D. 化学反应中,吸热反应不一定需要加热也能发生
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列叙述正确的是
A. 0.5mol![]() 含中子数为8NA
含中子数为8NA
B. 常温下,1 mol NH4Cl含共价键数目为5NA
C. 足量的Cu与含溶质1mol的浓H2SO4反应,转移的电子数为NA
D. 标况下,22.4LNO和11.2LO2混合后的气体分子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨硼烷(NH3·BH3)电池可在常温下工作,装置如图所示。未加入氨硼烷之前,两极室质量相等,电池反应为NH3·BH3+3H2O2==NH4BO2+4H2O 。已知H2O2足量,下列说法正确的是( )

A. 正极的电极反应式为2H++2e-===H2↑
B. 电池工作时,H+通过质子交换膜向负极移动
C. 电池工作时,正、负极分别放出H2和NH3
D. 工作足够长时间后,若左右两极室质量差为1.9 g,则电路中转移0.6 mol电子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com