
下列叙述中正确的是 ( )
A.1 mol CO2的质量是44g/mol B.铝离子的摩尔质量是27g
C. H2O的摩尔质量是18g/mol D.H2的相对分子质量是2g/mol
 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案科目:高中化学 来源: 题型:
下表是二种银盐的溶度积常数KSP(25℃).下列说法不正确的是

A.25℃时.二种银盐的饱和溶液中,c(Ag+)最大的是AgCl溶液
B.在AgCl的悬浊液中加入0.1mol·L—1的KI溶液,可能有黄色沉淀产生
C.25℃时.AgC1固体在等物质的量浓度的NaC1CaC1溶液中的溶度积相同
D.在AgBr的悬浊液中加入0.1mol·L-1的KI溶液.发生反应的离子方程式为

查看答案和解析>>
科目:高中化学 来源: 题型:
碲的某化合物就是常用的VCD光盘记录材料之一,碲位于钾的下一周期,与氧元素同一主族,对碲及其化合物的以下认识中不正确的是( )
A.单质碲在常温下是固体 B.H2TeO4的酸性比H2SO4的酸性弱
C.H2Te不如HI稳定 D.Te元素位于第六周期ⅥA族
查看答案和解析>>
科目:高中化学 来源: 题型:
可逆反应A(g)+3B(g)  2C(g);△H= -QkJ/mol。有甲、乙两个容积相同且固定不变的密闭容器,向甲容器中加入1molA和3molB,在一定条件下达到平衡时放出热量为Q1kJ;在相同的条件下,向乙容器中加入2molC达到平衡后吸收热量为Q2kJ,已知Q1=2Q2。下列叙述正确的是
2C(g);△H= -QkJ/mol。有甲、乙两个容积相同且固定不变的密闭容器,向甲容器中加入1molA和3molB,在一定条件下达到平衡时放出热量为Q1kJ;在相同的条件下,向乙容器中加入2molC达到平衡后吸收热量为Q2kJ,已知Q1=2Q2。下列叙述正确的是
A.甲中A的转化率为75%
B.Q1 + Q2 < Q
C.达到平衡后,再向乙中加入1/3 molA、1 molB、4/3 molC,平衡向正反应方向移动
D.乙中热化学方程式为2C(g) A(g)+3B(g);△H= + Q2 kJ/mol
A(g)+3B(g);△H= + Q2 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关化学能与热能的说法正确的是( )
A.铝热反应属于吸热反应
B.若某反应的反应物的总能量大于生成物的总能量,则该反应为吸热反应
C.H2→H+H的变化需要吸收能量
D.凡经加热而发生的化学反应都是吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中,错误的是
A、 煤、石油、天然气是当今世界最重要的三种化石燃料 B、我国目前最主要的能源是煤炭
C、人体运动所消耗的能量与化学反应无关D、人类目前所直接利用的能量大部分是由化学反应产生的
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关电化学装置的说法正确的是

A.利用图a装置处理银器表面的黑斑Ag2S,银器表面发生的反应为
B.图b电解一段时间,铜电极溶解,石墨电极上有亮红色物质析出
C.图c中的X极若为负极,则该装置可实现粗铜的精炼
D.图d中若M是海水,该装置是通过“牺牲阳极的阴极保护法”使铁不被腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
根据氨气还原氧化铜的反应,可设计测定铜元素相对原子质量么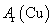 (近似值)的实验。先称量反应物氧化铜的质量m(CuO),反应完全后测定生成物水的质量m(H20),由此计算
(近似值)的实验。先称量反应物氧化铜的质量m(CuO),反应完全后测定生成物水的质量m(H20),由此计算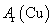 。为此,提供的实验仪器及试剂如下(根据需要可重复选用,加入的NH4C1与Ca(OH)2的量足以产生使CuO完全还原的氨气):
。为此,提供的实验仪器及试剂如下(根据需要可重复选用,加入的NH4C1与Ca(OH)2的量足以产生使CuO完全还原的氨气):



请回答下列问题:
(1)氨气还原炽热氧化铜的化学方程式为________________________________;
(2)从所提供的仪器及试剂中选择并组装本实验的一套合理、简单的装置,按气流方向的连接顺序为(用图中标注的导管口符号表示)a→________________;
(3)在本实验中,若测得m(CuO)= a g,m(H2O)= b g,则Ar(Cu)= _______________;
(4)在本实验中,使测定结果Ar(Cu)偏大的是_______________ (填序号);
①Cu0未完全起反应 ② CuO不干燥
③Cu0中混有不反应的杂质 ④ 碱石灰不干燥
⑤NH4C1与Ca(OH)2混合物不干燥
(5)在本实验中,还可通过测定__________和________,或_________和________达到实验目的。
10.高纯MnCO3是制备高性能磁性材料的主要原料。实验室以MnO2为原料制备少量高纯MnCO3的操作步骤如下:

(1)制备MnSO4溶液:在烧瓶中(装置见上图)加入一定量MnO2和水,搅拌,通入SO2和N2混合气体,反应3h。停止通入SO2,继续反应片刻,过滤(已知MnO2+H2SO4=MnSO4+H2O)。
①石灰乳参与反应的化学方程式为 。
②反应过程中,为使SO2尽可能转化完全,在通入SO2和N2比例一定、不改变固液投料的条件下,可采取的合理措施有 、 。
③若实验中将N2换成空气,测得反应液中Mn2+、SO42-的浓度随反应时间t变化如上图。导致溶液中Mn2+、SO42-浓度变化产生明显差异的原因是 。
(2)制备高纯MnCO3固体:已知MnCO3难溶于水、乙醇,潮湿时易被空气氧化,100℃开始分解;Mn(OH)2开始沉淀时pH=7.7。请补充由(1)制得的MnSO4溶液制备高纯MnCO3的操作步骤[实验中可选用的试剂:Ca(OH)2、NaHCO3、Na2CO3、C2H5OH]。
① ;② ;③ ;④ ;⑤低于100℃干燥。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com