
| A、只有①②③ | B、只有②③ |
| C、只有③④ | D、①②③④ |


 一线名师提优试卷系列答案
一线名师提优试卷系列答案 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案科目:高中化学 来源: 题型:
| A、先装好药品,再检查装置的气密性 |
| B、先用双手捂紧试管,再将导管插入水中检查装置的气密性 |
| C、氢气还原氧化铜的实验,先通一段时间的氢气,后检验氢气纯度,再加热 |
| D、稀释浓硫酸时,先在烧杯里倒入浓硫酸,再小心倒入水并不断搅拌 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、提倡双面使用纸张 |
| B、推广一次性竹筷 |
| C、提倡使用太阳能热水器 |
| D、推广公用自行车 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、(NH4)2SO4的大量使用可能造成土壤的碱化 |
| B、磷肥的大量使用可能造成水体富营养化 |
| C、农药的使用可能影响害虫与其天敌之间的生态平衡 |
| D、家蚕吞食喷洒过农药的桑叶,可能引起中毒 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、等于2cmol?L-1 |
| B、大于2cmol?L-1 |
| C、小于2cmol?L-1 |
| D、在c~2cmol?L-1之间 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 | 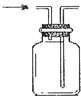 |  |  |
| A.配制一定物质的量浓度硫酸溶液 | B.排空气法收集氢气 | C.量取9.3ml稀盐酸 | D.制备少量氧气 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com