
| A、MgCl2 |
| B、AlCl3 |
| C、SiCl4 |
| D、PCl5 |
科目:高中化学 来源: 题型:
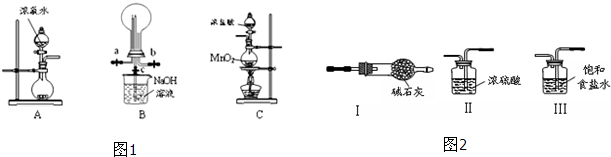
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、△H<0、△S>0的反应在任何温度下都能自发进行 |
| B、NH4HCO3(s)═NH3 (g)+H2O(g)+CO2(g)△H=+185.57 kJ?mol-1能自发进行,原因是体系有自发地向混乱度增加的方向转变的倾向 |
| C、因为焓变和熵变都与反应的自发性有关,因此焓变或熵变均可以单独作为反应自发性的判据 |
| D、在其他外界条件不变的情况下,使用催化剂,可以改变化学反应进行的速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、中和HCl的物质的量相同 |
| B、两溶液中所含的OH-数目相同 |
| C、NaOH溶液中c(H+)小 |
| D、氨水中c(OH-)大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
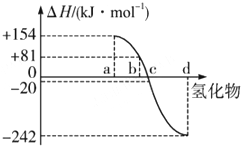 热力学标准态(298K、101kPa)下,由稳定单质发生反应生成1mol化合物的反应热叫该化合物的生成热(△H),图为氧族元素氢化物a、b、c、d的生成热数据示意图,(氧族元素包括氧、硫、硒、碲).试完成下列问题:
热力学标准态(298K、101kPa)下,由稳定单质发生反应生成1mol化合物的反应热叫该化合物的生成热(△H),图为氧族元素氢化物a、b、c、d的生成热数据示意图,(氧族元素包括氧、硫、硒、碲).试完成下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、只有①②③ | B、只有②③ |
| C、只有③④ | D、①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、不可用澄清石灰水鉴别Na2CO3和NaHCO3溶液 |
| B、1mol过氧化钠与2 mol碳酸钠固体混合后,在密闭容器中加热充分反应,排出气体物质后冷却,残留的固体物质是纯净物 |
| C、等质量的NaHCO3和Na2 CO3分别与足量盐酸反应,在同温同压下,生成的CO2体积相同 |
| D、可利用焰色反应来鉴别Na2CO3和NaHCO3固体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com