
 | 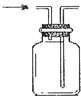 |  |  |
| A.配制一定物质的量浓度硫酸溶液 | B.排空气法收集氢气 | C.量取9.3ml稀盐酸 | D.制备少量氧气 |
| A、A | B、B | C、C | D、D |


科目:高中化学 来源: 题型:
| A、中和HCl的物质的量相同 |
| B、两溶液中所含的OH-数目相同 |
| C、NaOH溶液中c(H+)小 |
| D、氨水中c(OH-)大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、只有①②③ | B、只有②③ |
| C、只有③④ | D、①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验内容 | 实验现象 | 实验结论 |
| (1)将两块一样大小的镁条、铁片分别同时加入等体积的0.5mol.L-1的盐酸中. | 影响化学反应速率大小的内因为 | |
| (2)将等体积等浓度(3mol.L-1)的盐酸两份分别同时加入盛有等质量的块状碳酸钙及粉末状碳酸钙的试管中. | 参加反应的固体物质颗粒 | |
| (3)分别将两块同样大小的铁片同时加入等体积不同浓度(3mol.L-1、5mol.L-1、)的盐酸中. | 铁片与 | 反应物的浓度 |
| (4)分别将两块同样大小的铁片放入盛有等体积0.5mol.L-1盐酸的甲乙两试管中,再将甲试管用酒精灯加热,对比观察现象.. | 温度 |
查看答案和解析>>
科目:高中化学 来源: 题型:
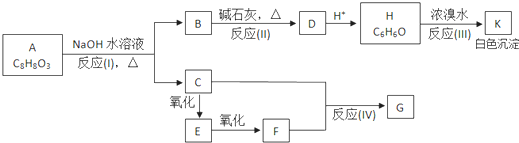
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、不可用澄清石灰水鉴别Na2CO3和NaHCO3溶液 |
| B、1mol过氧化钠与2 mol碳酸钠固体混合后,在密闭容器中加热充分反应,排出气体物质后冷却,残留的固体物质是纯净物 |
| C、等质量的NaHCO3和Na2 CO3分别与足量盐酸反应,在同温同压下,生成的CO2体积相同 |
| D、可利用焰色反应来鉴别Na2CO3和NaHCO3固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、做银镜反应实验后的试管内壁附有银,可用稀硝酸清洗 |
| B、向MgCl2溶液中滴加NaOH溶液,产生白色沉淀,再加入FeCl3溶液,沉淀逐渐变为红褐色 |
| C、用0.1mol/L的酸性KMnO4溶液配成的溶液滴定一定质量的草酸晶体(H2C2O4?nH2O)以测定其n值,若终点仰视读数,则n值偏大 |
| D、环形玻璃搅拌棒材料若用铜代替,则测量出的中和热数值偏小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com