
将Cu、Cu2O和 CuO均匀混合物分成两等份,其中一份用足量的CO还原,测得反应后固体质量减少6.4g,另一份中加入150mL某浓度的硝酸,固体恰好完全溶解,且同时收集到标准状况下NOX气体6.72L,则所用硝酸的物质的量浓度可能为
| A.8.0mol·L-1 | B.9.0mol·L-1 | C.10.0mol·L-1 | D.11.0mol·L-1 |
CD
解析试题分析:将Cu2O拆分为Cu、CuO,原混合物看做Cu、CuO的混合物,其中一份用足量的CO气还原,反应后固体质量减少6.40g为拆分后Cu、CuO的混合物中O元素的质量,O原子的物质的量为6.4/16=0.4mol,根据Cu元素守恒可知n(CuO)=n(O)=0.4mol;另一份中加入150mL某浓度的硝酸,固体恰好完全溶解,固体恰好完全溶解,溶液中溶质为Cu(NO3)2,且同时收集到标准状况下NOX气体6.72L,,NOX的物质的量为6.72/22.4=0.3mol,若为NO:则根据电子转移守恒可知拆分后Cu、CuO的混合物中2n(Cu)=3n(NO)=3×0.3mol,n(Cu)=0.45mol,由铜元素守恒可知n[Cu(NO3)2]=n(CuO)+n(Cu)=0.4mol+0.45mol=0.85mol,根据氮元素守恒可知n(HNO3)=n(NO)+2n[Cu(NO3)2]=0.3mol+2×0.85mol=2mol,硝酸的浓度为2/0.15=11.3mol/L。若为NO2:则根据电子转移守恒可知拆分后Cu、CuO的混合物中2n(Cu)=n(NO2)=0.3mol,n(Cu)=0.15mol,由铜元素守恒可知n[Cu(NO3)2]=n(CuO)+n(Cu)=0.4mol+0.15mol=0.55mol,根据氮元素守恒可知n(HNO3)=n(NO)+2n[Cu(NO3)2]=0.3mol+2×0.55mol=1.4mol,硝酸的浓度为1.4/0.15=9.3mol/L。故选:A.故硝酸的物质的量浓度可能为10.0mol·L-1和11.0mol·L-1之间。
考点:本题考查了混合物的计算、守恒计算等。


 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案科目:高中化学 来源: 题型:单选题
某稀硫酸和稀硝酸的混合溶液200 mL,平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解19.2 g(已知硝酸只被还原为NO气体)。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如下图所示。下列分析或结果错误的是( )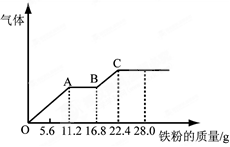
| A.H2SO4浓度为2.5 mol·L-1 |
| B.OA段产生的是NO,AB段的反应为Fe+2Fe3+=3Fe2+,BC段产生氢气 |
| C.第二份溶液中最终溶质为FeSO4 |
| D.混合酸中NO3-物质的量为0.4mol |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列叙述正确是的
| A.人工固氮的过程一定涉及到氧化还原反应 |
| B.1mol氯气在反应中一定得到2mol电子 |
| C.1mol钠在足量氧气中燃烧生成Na2O2,失去2mol电子 |
| D.发生化学反应时,失去电子越多的金属原子,还原能力越强 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
氢化亚铜(CuH)是一种不稳定物质,能在氯气中燃烧;也能与酸反应。用CuSO4溶液和“某物质”在40~50℃时反应可产生它。下列有关叙述中错误的是
| A.“某物质”具有还原性 |
| B.CuH与盐酸反应,可能产生H2 |
| C.CuH与足量的稀硝酸反应:CuH+ 3H++ NO3-→ Cu2++ NO↑+ 2H2O |
| D.CuH在氯气中燃烧:CuH+ Cl2→ CuCl+ HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
对剧毒的氰化物可在碱性条件下用如下方法进行处理:2CN-+8OH-+5Cl2=2CO2+N2+10Cl-+4H2O。下列判断正确的是
| A.当有0.2mol CO2生成时,溶液中阴离子的物质的量增加1mol |
| B.该反应中,每有2molCN-反应,转移电子为10mol |
| C.上述反应中的还原剂是OH- |
| D.还原性:C1->CN- |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
高铁酸钠(Na2FeO4)是一种新型、高效、多功能的水处理剂。湿法制备的离子反应方程式: 2Fe(OH)3+3ClO-+4OH-→ 2FeO42-+3Cl-+5H2O;干法制备化学反应方程式:2FeSO4+4Na2O2→2Na2FeO4+2Na2SO4。有关分析错误的是
| A.等物质的量Na2FeO4氧化能力优于次氯酸钠 |
| B.湿法中氢氧化铁被氧化 |
| C.干法中每生成1 mol Na2FeO4转移3 mol电子 |
| D.高铁酸钠的氧化性大于次氯酸钠 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
新型纳米材料氧缺位铁酸盐(MFe2Ox 3<x<4,M=Mn、Co、Zn或Ni,在该盐中均显+2价)由铁酸盐(MFe2O4)经高温与氢气反应制得,常温下,它能使工业废气中的酸性氧化物(SO2、NO2等)转化为其单质除去,转化流程如图。关于此转化过程的叙述不正确的是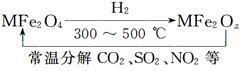
| A.MFe2O4在与H2的反应中表现了氧化性 |
| B.MFe2O4与MFe2Ox的相互转化反应均属于氧化还原反应 |
| C.MFe2Ox与SO2反应中MFe2Ox被还原 |
| D.若4 mol MFe2Ox与1 mol SO2恰好完全反应,则MFe2Ox中x的值为3.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
氢化亚铜(CuH)是一种不稳定物质,能在氯气中燃烧;也能与酸反应。用CuSO4溶液和“某物质”在40~50℃时反应可产生它。下列有关叙述中错误的是( )
| A.这“某物质”具有还原性 |
| B.CuH与盐酸反应,可能产生H2 |
| C.CuH与足量的稀硝酸反应:CuH+3H++NO3—=Cu2++NO↑+2H2O |
| D.CuH在氯气中燃烧:CuH+Cl2=CuCl+HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
三氟化氮(NF3)(提示氟只有两种价态:-1,0)是微电子工业中优良的等离子刻蚀气体,它在潮湿的环境中能发生反应:3NF3+5H2O=2NO+HNO3+9HF。下列有关该反应的说法正确的是
| A.NF3是氧化剂,H2O是还原剂 |
| B.还原剂与氧化剂的物质的量之比为2:1 |
| C.若生成0.2molHNO3,则转移0.2mol电子 |
| D.若1molNF3被氧化反应转移电子数为2NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com