
【题目】工业上利用软锰矿浆(软锰矿的主要成分是MnO2,还含有硅、铁、铝、钙、镁和少量重金属镍的化合物等杂质)为原料制取电解锰和四氧化三锰。

注:过量的软锰矿将Fe2+氧化为Fe3+。
(1)纤维素[(C6H10O5)n]还原MnO2时,发生反应的化学方程式为_______。
(2)已知:Kp[Al(OH)3]=1×10-33,Ksp[Fe(OH)3]=3×10-39,加入NH3·H2O后,Al3+浓度为l×10-6mol/L时,溶液中Fe3+浓度为_________
(3)pH对除镍效果的影响如图1:

控制pH为4.5~5.0除镍效果最好,原因是__________
(4)电解MnSO4溶液制备电解锰,用惰性电极电解,阳极的电极反应式为________,为保证电解的顺利进行,电解液必须保持一定的Mn2+浓度。Mn2+浓度和电流效率的关系如图2所示。由图可知当Mn2+浓度大于22g/L时,电流效率随Mn2+浓度增大反而下降,其原因是________。

(5)MnSO4溶液制备四氧化三锰。氨水作沉淀剂,沉淀被空气氧化所得产品的X射线图见图3。
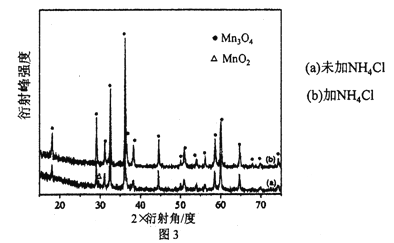
Mn2+形成Mn(OH)2时产生少量Mn2(OH)2SO4,加入NH4Cl会影响Mn2(OH)2SO4的氧化产物,写出NH4Cl存在时,Mn2(OH)2SO4被O2氧化发生反应的离子方程式___________。
【答案】 12nMnO2+(C6H10O5)n+12nH2SO4=12nMnSO4+6nCO2+17nH2O 3×10-12mol/L pH过低,会与硫化钡产生硫化氢气体;pH过高,Mn2+被沉淀 2H2O-4e-=O2↑+4H+或4OH--4e-=O2↑+2H2O Mn2+浓度增大,容易产生Mn(OH)2沉淀 3Mn2(OH)2SO4+O2=2Mn3O4+6H++3SO42-
【解析】(1)纤维素[(C6H10O5)n]具有还原性,MnO2具有氧化性,二者可发生氧化还原反应,发生反应的化学方程式为:12nMnO2+(C6H10O5)n+12nH2SO4=12nMnSO4+6nCO2+17nH2O,答案为:12nMnO2+(C6H10O5)n+12nH2SO4=12nMnSO4+6nCO2+17nH2O
(2)Kp[Al(OH)3]=c(Al3+)×c3(OH-)=1×10-33,所以c3(OH-)=1×10-27;,Ksp[Fe(OH)3]= c(Fe3+)×c3(OH-)=3×10-39,所以c(Fe3+)=![]() =3
=3![]() mol/L,答案为:3×10-12mol/L
mol/L,答案为:3×10-12mol/L
(3)pH过低,会与硫化钡反应产生硫化氢气体,pH过高,Mn2+被沉淀,并且根据表中的数据知道,当pH小于4.2的时候,镍离子随pH的减小而残留率增加,当pH大于5的时候,镍离子随pH的增大而残留率增加,所以控制pH为4.5![]() 5.0镍离子的含量最小,除镍效果最好;答案为:pH过低,会与硫化钡产生硫化氢气体,pH过高,Mn2+被沉淀
5.0镍离子的含量最小,除镍效果最好;答案为:pH过低,会与硫化钡产生硫化氢气体,pH过高,Mn2+被沉淀
(4)“电解”时用惰性电极电解,阳极发生氧化反应,应该是水电离出的氢氧根离子放电,电极反应式为:2H2O-4e-=O2↑+4H+或4OH--4e-=O2↑+2H2O;当Mn2+浓度大于22g/L时,容易产生Mn(OH)2沉淀,电流效率反而下降;答案为:2H2O-4e-=O2↑+4H+或4OH--4e-=O2↑+2H2O,Mn2+浓度增大,容易产生Mn(OH)2沉淀
(5)由X射线图可知,未加NH4Cl时Mn2(OH)2SO4的氧化产物主要是MnO2,加NH4Cl时Mn2(OH)2SO4的氧化产物主要是Mn3O4,因此NH4Cl存在时,Mn2(OH)2SO4被O2氧化发生反应的离子方程式为:3Mn2(OH)2SO4+O2=2Mn3O4+6H++3SO42-;答案为:3Mn2(OH)2SO4+O2=2Mn3O4+6H++3SO42-


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】室温时,向20mL0.1mol/L醋酸溶液中不断滴入0.1mol/L的NaOH溶液,溶液pH变化如图所示。下列叙述错误的是

A. a点:c(CH3COOH)+2c(H+)=c(CH3COO-)+2c(OH-)
B. b点:c(Na+)=c(CH3COOH)+c(CH3COO-)
C. C点:c(OH-)=c(CH3COOH)+c(H+)
D. d点:2c(Na+)=3[c(CH3COOH)+c(CH3COO-)]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A. 凡能发生银镜反应的有机物一定是醛
B. 在氧气中燃烧时只生成CO2和H2O的物质一定是烃
C. 苯酚有弱酸性,俗称石炭酸,因此它是一种羧酸
D. 75%(体积分数)的乙醇溶液常用于医疗消毒
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】改变0.1mol·L-1二元弱酸H2A溶液的pH,溶液中的H2A、HA-、A2-的物质的量分数∮(X)随pH的变化如图所示[已知:∮(X)=  ]。下列叙述错误的是( )
]。下列叙述错误的是( )

A. pH=1.2时,c(H2A)=c(HA-) B. lg[K2(H2A)]=-4.2
C. pH=2.7时,c(HA-)>c(H2A)=c(A2-) D. pH=4.2时,c(HA-)=c(A2-)=c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有三个体积相同的密闭容器,按下图所示投料,并在T℃条件下开始反应,其中容器I保持恒压100kPa。已知:分压=总压×物质的量分数,对于2NO2(g)![]() N2O4(g)ΔH<0,T℃时,标准平衡常数KΘ={p(N2O4)/100kPa}/{[p(NO2)] /100kPa}2=0.75, 式中p(N2O4) 、p(NO2)为气体分压。下列说法正确的是
N2O4(g)ΔH<0,T℃时,标准平衡常数KΘ={p(N2O4)/100kPa}/{[p(NO2)] /100kPa}2=0.75, 式中p(N2O4) 、p(NO2)为气体分压。下列说法正确的是

A. 达平衡时,容器Ⅱ中N2O4转化率小于50%
B. 达平衡时,容器Ⅰ中N2O4分压比容器Ⅲ中的大
C. 达平衡时,容器Ⅰ中N2O4的体积分数比容器Ⅱ中的大
D. 若起始时向容器Ⅲ中充入2molN2O4、2molNO2,达到平衡前v(正)<v(逆)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在C+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2O反应中:
CO2↑+2SO2↑+2H2O反应中:
(1) ______ 元素被氧化,______ 是氧化剂,___________是还原产物。
(2)若有0.6 mol的C参加反应,则被还原的H2SO4的物质的量为______ mol,反应中转移的电子的物质的量为_________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业纯碱中常含NaCl,某活动小组设计如图装置测定工业纯碱中Na2CO3的含量。
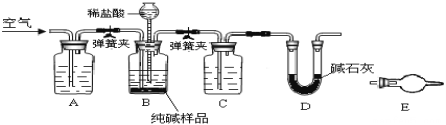
(1)检验装置B气密性方法是:塞紧带长颈漏斗的三孔橡胶塞,夹紧弹簧夹后,从漏斗注入一定量水,使漏斗内水面高于瓶内水面,停止加水后,若___________,说明装置不漏气。
(2)装置A的作用是_______,装置C中的试剂为_______。
(3)某同学认为在D装置后应再连接E装置(装有适当试剂),你认为是否必要?_______(选填“必要”或“不必要”),判断的理由是_____________________。
(4)实验前28.8g样品,实验后测得D装置增重8.8g,则样品中Na2CO3质量分数为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色溶液中,可大量共存的离子组是( )
A.Na+、HCO3-、SO42-、Br-
B.Cu2+、NO3-、Cl-、SO42-
C.H+、Cl-、K+、CO32-
D.K+、Mg2+、SO42-、OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将下列物质按酸、碱、盐分类排列,正确的是( )
A.硫酸、Na2CO3、CaSO4·2H2OB.盐酸、烧碱、CuSO4·5H2O
C.HNO3、乙醇、氯化钠D.H3PO4、熟石灰、苛性钾
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com