
【题目】A、B、C、W均为中学常见的纯净物,它们之间有如下转化关系(其它产物及反应条件已略去,反应可以在水溶液中进行)。
![]()
(1)若A、B、C三种物质的溶液均显碱性,焰色反应均为黄色,C受热分解可转化为B
①则W的化学式为____;B的化学式____。
②A溶液与C溶液反应的化学方程式为____。
(2)若A为黄绿色气体,W为金属单质.B的溶液遇KSCN显红色。
①B与W转化为C的离子反应方程式___。
②C与A转化为B的离子反应方程式____。
【答案】 CO2 Na2CO3 NaOH+NaHCO3=Na2CO3+H2O Fe+2Fe3+=3Fe2+ Cl2+2Fe2+=2Cl-+2Fe3+
【解析】(1)若A、B、C三种物质的溶液均显碱性,焰色反应均为黄色,即含有钠元素。C受热分解可转化为B,则C是碳酸氢钠,B是碳酸钠,A是氢氧化钠,W是CO2。①根据以上分析可知W的化学式为CO2;B的化学式为Na2CO3;②A溶液与C溶液反应的化学方程式为NaOH+NaHCO3=Na2CO3+H2O。(2)若A为黄绿色气体,A是氯气。W为金属单质,B的溶液遇KSCN显红色,W是铁,B是氯化铁,C是氯化亚铁。①B与W转化为C的离子反应方程式为Fe+2Fe3+=3Fe2+;②C与A转化为B的离子反应方程式为Cl2+2Fe2+=2Cl-+2Fe3+。


 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案科目:高中化学 来源: 题型:
【题目】某化合物6.4g在氧气中完全燃烧,只生成8.8g CO2和7.2g H2O.下列说法正确( )
A.该化合物仅含碳、氢两种元素
B.该化合物中碳、氢原子个数比为1:4
C.无法确定该化合物是否含有氧元素
D.该化合物中一定含有氧元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.某钠盐溶液中通入足量氨气,无明显现象.再在所得溶液中通入过量CO2 , 产生大量白色沉淀。
(1)写出氨气的电子式。
(2)该钠盐溶液中一定不可能含有下列哪种微粒(填编号)。
A.Cl﹣
B.Fe2+
C.SiO32﹣
D.AlO2﹣
(3)写出一个通入过量CO2时生成白色沉淀的离子方程式。
(4)Ⅱ.电镀工业中往往产生大量的有毒废水,必须严格处理后才可以排放.某种高浓度有毒的含A离子(阴离子)废水在排放前的处理过程如下: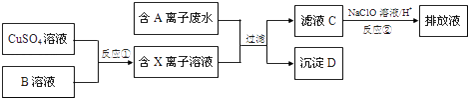
已知:9.0g沉淀D在氧气中灼烧后,产生8.0g黑色固体,反应后的气体通过足量澄清石灰水时,产生10.0g白色沉淀,最后得到的混合气体除去氧气后,还剩余标况下密度为1.25g/L的气体1.12L。
沉淀D的化学式是。
(5)写出沉淀D在氧气中灼烧发生的化学方程式。
(6)滤液C中还含有微量的A离子,通过反应②,可将其转化为对环境无害的物质,试用离子方程式表示该原理。
(7)反应①为制得某种元素的低价X离子,从氧化还原反应的角度分析,(填“能”或“不能”用Na2SO3溶液来代替B溶液,原因是。
(8)设计实验证明所用Na2SO3溶液是否变质。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】做氯化氢喷泉实验后,烧瓶内的液体只占烧瓶容积的三分之一,其原因可能是( )
A.HC1气体没有完全溶解B.装置漏气,进入空气
C.集气时有空气混入D.从胶头滴管挤入烧瓶的水太少
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高炉炼铁中常见的反应为:Fe2O3(s)+3CO(g) ![]() 2Fe(s)+3CO2(g) △H
2Fe(s)+3CO2(g) △H
(1)某实验小组在实验室模拟上述反应。一定温度下,在2L盛有Fe2O3粉末的恒容密闭容器中通入0.1molCO,5min时生成2.24gFe。5min内有CO表示的平均反应速率是mol·L-1min-1;5min时CO2的体积分数为;若将此时反应体系中的混合气体通入100mL0.9mol/L的NaOH溶液中,充分反应后所得溶液中离子浓度由大到小的顺序是 。
(2)上述反应的平衡常数表达式为:K=;下列能说明该反应已经达到平衡状态的是(填序号)。
a.容器内固体质量保持不变
b.容器中气体压强保持不变
c.c(CO)=c(CO2)
d.v正(CO)=v逆(CO2)
(3)已知上述反应的平衡常数K与温度T(单位:K)之间的关系如图所示,其中直线的斜率为- ![]() (气体常数R=8.3×10-3kJ·mol-1·K-1)。
(气体常数R=8.3×10-3kJ·mol-1·K-1)。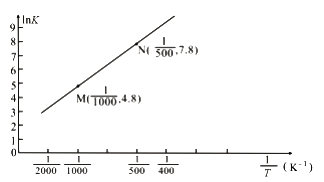
①根据图像可知,该反应的平衡常数随温度升高而(填“增大”、“减小”或“不变”)
②该反应的△H=kJ·mol-1。
(4)结合上述有关信息,写出两条提高CO转化率的措施、。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在足量的NaI溶液中,加入少量氯水及四氯化碳,振荡后静置,出现的现象( )
A.溶液不分层,溶液呈紫红色B.溶液分两层,上层液体呈紫红色
C.溶液分两层,下层液体呈紫红色D.溶液分两层,下层是无色液体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用零价铁(Fe)去除水体中的硝酸盐(NO3﹣)已成为环境修复研究的热点之一.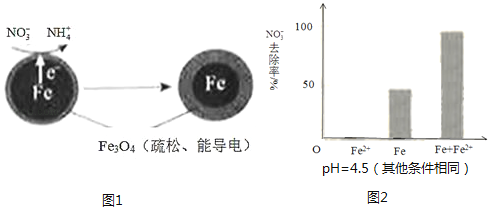
(1)Fe还原水体中NO3﹣的反应原理如图1所示.
①作负极的物质是 .
②正极的电极反应式是 .
(2)将足量铁粉投入水体中,经24小时测定NO3﹣的去除率和pH,结果如下:
初始pH | pH=2.5 | pH=4.5 |
NO3﹣的去除率 | 接近100% | <50% |
24小时pH | 接近中性 | 接近中性 |
铁的最终物质形态 |
|
|
pH=4.5时,NO3﹣的去除率低.其原因是 .
(3)实验发现:在初始pH=4.5的水体中投入足量铁粉的同时,补充一定量的Fe2+可以明显提高NO3﹣的去除率.对Fe2+的作用提出两种假设:
Ⅰ.Fe2+直接还原NO3﹣;
Ⅱ.Fe2+破坏FeO(OH)氧化层.
①做对比实验,结果如图2所示,可得到的结论是 .
②同位素示踪法证实Fe2+能与FeO(OH)反应生成Fe3O4 . 结合该反应的离子方程式,解释加入Fe2+提高NO3﹣去除率的原因: .
(4)其他条件与(2)相同,经1小时测定NO3﹣的去除率和pH,结果如表:
初始pH | pH=2.5 | pH=4.5 |
NO3﹣的去除率 | 约10% | 约3% |
1小时pH | 接近中性 | 接近中性 |
与(2)中数据对比,解释(2)中初始pH不同时,NO3﹣去除率和铁的最终物质形态不同的原因: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某城市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5(直径小于等于25μm的悬浮颗粒物),其主要来源为燃煤、机动车尾气等。因此,对PM2.5、SO2、NOx等进行研究具有重要意义。请回答下列问题:
(1)PM2.5分散在空气中形成的分散系___(填“属于”,“不属于”)胶体。
(2)将PM2.5样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
离子 | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
浓度(mol/L) | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
根据表中数据判断待测试样为___(填酸”、“碱”)性,表示该试样酸碱性的c(H+)或c(OH-)=_______mol/L。
(3)煤燃烧排放的烟气含有SO2和NOx,形成酸雨,污染大气,采用NaClO2溶液在碱性条件下可对烟气进行脱硫,脱硝,效果非常好。完成下列对烟气脱硝过程的离子方程式。
___ClO2-+__NO+____=___Cl-+___NO3-+___,________________
(4)为减少SO2的排放,常采取的措施有:
①将煤转化为清洁气体燃料。写出焦炭与水蒸气反应的化学方程式___________。
②洗涤含SO2的烟气。以下物质可作洗涤剂的是___________。
a.Ca(OH)2 b.Na2CO3 c.CaCl2 d.NaHSO3
(5)汽车尾气中NOx和CO的生成及转化。
①汽车启动后,汽缸温度越高,单位时间内NO排放量越大,写出汽缸中生成NO化学方程式_______________。
②汽车燃油不完全燃烧时产生CO,目前,在汽车尾气系统中装置催化转化器可减少CO和NO的污染,其化学反应方程式为_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com