
【题目】以下材料中,属于硅酸盐材料的是( )
A.铝合金
B.碳纤维
C.普通玻璃
D.塑料
 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案科目:高中化学 来源: 题型:
【题目】工业生产硝酸铵的流程如下图所示: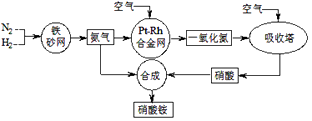
(1)硝酸铵的水溶液呈(填“酸性”、“中性”或“碱性”);其水溶液中各离子的浓度大小顺序为:。
(2)已知N2(g)+3H2(g) ![]() 2NH3(g) △H<0,当反应器中按n(N2):n(H2)=1:3投料,分别在200℃、400℃、600℃下达到平衡时,混合物中NH3的物质的量分数随压强的变化曲线如下图。
2NH3(g) △H<0,当反应器中按n(N2):n(H2)=1:3投料,分别在200℃、400℃、600℃下达到平衡时,混合物中NH3的物质的量分数随压强的变化曲线如下图。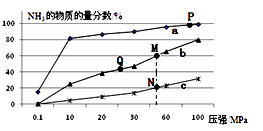
①曲线a对应的温度是。
②关于工业合成氨的反应,下列叙述正确的是。
A.及时分离出NH3可以提高H2的平衡转化率
B.P点原料气的平衡转化率接近100%,是当前工业生产工艺中采用的温度、压强条件
C.上图中M、N、Q点平衡常数K的大小关系是K(M)=K(Q)>K(N)
D.如果N点时c(NH3)=0.2 mol·L-1 , N点的化学平衡常数K≈0.93
(3)尿素(H2NCONH2)是一种非常重要的高效氮肥,工业上以NH3、CO2为原料生产尿素,该反应实际为二步反应:
第一步:2NH3(g)+CO2(g)=H2NCOONH4(s) ΔH=-272 kJ·mol-1
第二步:H2NCOONH4(s)=CO(NH2)2(s)+H2O(g) ΔH=+138 kJ·mol-1
写出工业上以NH3、CO2为原料合成尿素的热化学方程式:
(4)某实验小组模拟工业上合成尿素的条件,在一体积为0.5 L密闭容器中投入4 mol氨和1mol二氧化碳,实验测得反应中各组分随时间的变化如下左图所示: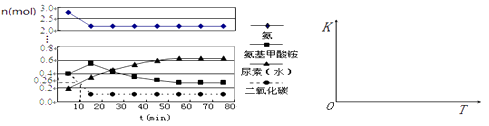
①已知总反应的快慢由慢的一步决定,则合成尿素总反应的快慢由第步反应决定,总反应进行到min时到达平衡。
②反应进行到10 min时测得CO2的物质的量如图所示,则用CO2表示的第一步反应的速率v(CO2)= 。
③在上面右图中画出第二步反应的平衡常数K随温度的变化的示意图 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质发生变化时,所克服的粒子间相互作用属于分子间作用力的是( )
A.酒精受热变为气体
B.氯化铵受热变为气体
C.二氧化硅受热熔化
D.食盐溶解在水中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,等体积、pH均为3的HA和HB溶液分别加水稀释,溶液pH值的变化如下图所示,下列说法正确的是( )
A.向HB溶液中滴加NaOH溶液的过程中,水的电离程度一直增大
B.用pH为11的某碱与pH为3的HB溶液等体积混合后,溶液不可能显碱性
C.氨水与HA溶液混合后的溶液中可能存在:c(NH4+ )>c(A+)>c(H+)>c(OH-)
D.完全中和等体积等pH的HA、HB两溶液时,消耗同浓度NaOH溶液的体积:HA<HB
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂的工业废水中含有大量的FeS04,较多的Cu2+和少量Na+。该工厂计划从废水中回收FeS04和金属铜。根据下列流程图,同答问题。
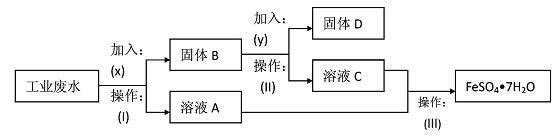
(1)加入的试剂x为____,y为____;
(2)加入试剂y发生反应的离子方程式是_______;
(3)操作(I)为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、W均为中学常见的纯净物,它们之间有如下转化关系(其它产物及反应条件已略去,反应可以在水溶液中进行)。
![]()
(1)若A、B、C三种物质的溶液均显碱性,焰色反应均为黄色,C受热分解可转化为B
①则W的化学式为____;B的化学式____。
②A溶液与C溶液反应的化学方程式为____。
(2)若A为黄绿色气体,W为金属单质.B的溶液遇KSCN显红色。
①B与W转化为C的离子反应方程式___。
②C与A转化为B的离子反应方程式____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“足球烯”C60是一种外形类似足球状的分子,关于C60的说法错误的是( )
A.C60是一种新型的化合物B.C60的相对分子量为720
C.C60和金刚石互为同素异形体D.C60硬度比金刚石小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com