
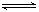 2C(g)������2�����C��Ũ��Ϊ0.6 mo1��L-1���������м���˵����
2C(g)������2�����C��Ũ��Ϊ0.6 mo1��L-1���������м���˵����| A���٢� | B���٢� | C���ڢ� | D���ۢ� |
 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 pC(g)�ﵽƽ���ѹ�����������������A��ת������֮���͡�����˵���У���ȷ���ǣ� ��
pC(g)�ﵽƽ���ѹ�����������������A��ת������֮���͡�����˵���У���ȷ���ǣ� ��| A��m��n�ض�С��p | B��m��n�ض�����p |
| C��m�ض�С��p | D��m�ض�����p |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A������ʯ�ҵ�����Һ���ȣ�����Һ�й����������� |
| B��ʵ�����г����ű���ʳ��ˮ�ķ�ʽ�ռ����� |
| C������ˮƿ�������ݴ���Һ��ð�� |
| D����ϡ�����м�����������ˮ��������������Ũ�Ƚ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 ?nC(��)��Q��һ�������´ﵽƽ��ı�������������ش�
?nC(��)��Q��һ�������´ﵽƽ��ı�������������ش��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2Z(g)��ӦӰ���ʾ��ͼ��ͼ�к������ʾ�¶ȣ��������ʾƽ����������Y���������������������ȷ����(����)
2Z(g)��ӦӰ���ʾ��ͼ��ͼ�к������ʾ�¶ȣ��������ʾƽ����������Y���������������������ȷ����(����)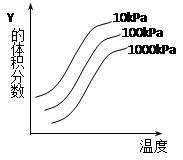
| A�������¶�����Ӧ���ʼ�С���淴Ӧ��������ƽ�������ƶ� |
| B��������Ӧ�ġ�H��0 |
| C��ƽ����ϵ�м���X��Y��ת���ʽ��� |
| D������ѹǿ��ƽ�������ƶ���XΪ��̬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 pC (g) + qD (g)������5���Ӵﵽƽ�⣬��ʱ�����ʵı仯ΪA����Ϊa mol /L��B��ƽ����Ӧ����VB =" a/15" mol/ (L min)��C����2a / 3 mol/L����ʱ������ϵͳѹǿ������A��C�İٷֺ������䣬��m��n��p��qΪ�� ��
pC (g) + qD (g)������5���Ӵﵽƽ�⣬��ʱ�����ʵı仯ΪA����Ϊa mol /L��B��ƽ����Ӧ����VB =" a/15" mol/ (L min)��C����2a / 3 mol/L����ʱ������ϵͳѹǿ������A��C�İٷֺ������䣬��m��n��p��qΪ�� ��| A��3��1��2��2 | B��1��3��2��2 | C��1��3��2��1 | D��1��1��1��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2AB(g) �ﵽƽ��״̬�ı�־��
2AB(g) �ﵽƽ��״̬�ı�־��| A����λʱ������n molA2ͬʱ����n molAB |
| B�������ڵ���ѹǿ����ʱ��仯 |
| C����λʱ������2n molABͬʱ����n molB2 |
| D����λʱ������n molA2ͬʱ����n molB2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
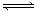 CHCl3+ HCl���˷�Ӧ���и���Ӧ��������CH2Cl2��CH3Cl��CH4�ȡ���֪CCl4�ķе�Ϊ770C��CHCl3�ķе�Ϊ61.20C�����ܱ������У��÷�Ӧ�ﵽƽ�����������ݣ����費���Ǹ���Ӧ��
CHCl3+ HCl���˷�Ӧ���и���Ӧ��������CH2Cl2��CH3Cl��CH4�ȡ���֪CCl4�ķе�Ϊ770C��CHCl3�ķе�Ϊ61.20C�����ܱ������У��÷�Ӧ�ﵽƽ�����������ݣ����費���Ǹ���Ӧ��| ʵ����� | �¶�0C | ��ʼCCl4Ũ��mol/L | ��ʼH2Ũ��mol/L | CCl4��ƽ��ת���� |
| 1 | 110 | 0.8 | 1.2 | A |
| 2 | 110 | 1 | 1 | 50% |
| 3 | 120 | 1 | 1 | B |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
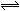 2AB(g)���ﵽƽ��ı�־���ǣ� ��
2AB(g)���ﵽƽ��ı�־���ǣ� ��| A���������������ѹǿ����ʱ��ı仯���仯 |
| B����λʱ������n mol A2���ɣ�ͬʱ����n mol B2���� |
| C����λʱ������n mol A2���ģ�ͬʱ����2n mol AB���� |
| D����λʱ������n mol B2������Ӧ��ͬʱ����2n mol AB�ֽ� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com