
 ?nC(气)+Q在一定条件下达到平衡后,改变下列条件,请回答:
?nC(气)+Q在一定条件下达到平衡后,改变下列条件,请回答:科目:高中化学 来源:不详 题型:填空题
| 温度/℃ | 25 | t1 | t2 |
| 水的离子积常数 | 1×10-14 | a | 1×10-12 |
 5Ca2+(aq)+3PO(aq)+OH-(aq);Ksp=2.5×10-59。进食后,细菌和酶作用于食物,产生有机酸,这时牙齿就会受到腐蚀,其原因是 。
5Ca2+(aq)+3PO(aq)+OH-(aq);Ksp=2.5×10-59。进食后,细菌和酶作用于食物,产生有机酸,这时牙齿就会受到腐蚀,其原因是 。 N2O4(g)的平衡常数K= 。若NO2起始浓度为2 mol/L ,相同条件下,NO2的最大转化率为 。
N2O4(g)的平衡常数K= 。若NO2起始浓度为2 mol/L ,相同条件下,NO2的最大转化率为 。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 C(g)+2D(g);ΔH<0,在一定条件下达到平衡,下列有关叙述正确的是( )
C(g)+2D(g);ΔH<0,在一定条件下达到平衡,下列有关叙述正确的是( )| A.①② | B.④ | C.③ | D.④⑤ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
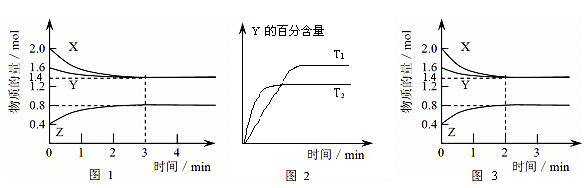
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 C(g)+2D(g)ΔH<0,在一定条件下达到平衡,下列有关叙述正确的是
C(g)+2D(g)ΔH<0,在一定条件下达到平衡,下列有关叙述正确的是| A.①② | B.④ | C.③ | D.④⑤ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
 3C(g) K = 16求A转化为C的转化率为__________。
3C(g) K = 16求A转化为C的转化率为__________。 cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,A的浓度为原平衡的2.1倍,则 a _______ c+d(填“>”、“=”或“<”)。
cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,A的浓度为原平衡的2.1倍,则 a _______ c+d(填“>”、“=”或“<”)。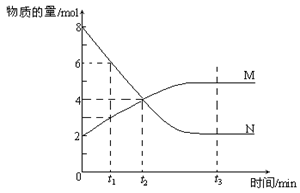
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
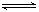 2C(g),若经2秒后测得C的浓度为0.6 mo1·L-1,现有下列几种说法:
2C(g),若经2秒后测得C的浓度为0.6 mo1·L-1,现有下列几种说法:| A.①③ | B.①④ | C.②③ | D.③④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
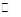 2C(g),现等物质的量的投料反应物A、B于恒温恒容体系I和恒温、恒压体系II中,达平衡时体系I中A的物质的量浓度为M,体系II中A的物质的量浓度为m,则M与m的关系为
2C(g),现等物质的量的投料反应物A、B于恒温恒容体系I和恒温、恒压体系II中,达平衡时体系I中A的物质的量浓度为M,体系II中A的物质的量浓度为m,则M与m的关系为查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

A.反应的化学方程式为:N 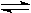 2M 2M |
| B.t2时,反应不再发生 |
| C.t2时,正反应速率等于逆反应速率 |
| D.t3后,反应到达最大限度 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com