
����Ŀ����֪H2S��CO2�ڸ����·�����Ӧ��H2S(g)+CO2(g)COS(g)+H2O(g)��H����Q kJmol��1 (Q��0)�����¶�ΪT1ʱ����0.10molCO2��0.40mol H2S����2.5L �Ŀո�ƿ�У�����4min��Ӧ�ﵽƽ�⣬ƽ��ʱH2O(g)�����ʵ�������Ϊ 2%��������˵������ȷ����( )
A.0��4 min����H2S��ʾ�÷�Ӧ������Ϊ0.001 molL��1min��1
B.CO2��ƽ��ת��������2.5%
C.���������·�Ӧ�ﵽƽ��ʱ�ų�������Ϊ0.01Q kJ
D.�����������䣬���÷�Ӧ���¶�ΪT2 �����½��У��ﵽƽ������ʱ��С��4 min���� T1��T2
���𰸡�B
��������
���ݷ�Ӧ�С�����ʽ����
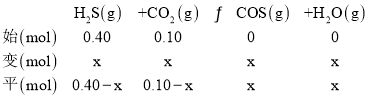
��Ӧƽ���ˮ�����ʵ�������Ϊ0.02����![]() ��0.02��x��0.01��
��0.02��x��0.01��
A��0��4 min ���� H2S ��ʾ�÷�Ӧ�����ʣ�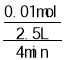 ��0.001 molL��1min��1����A��ȷ��
��0.001 molL��1min��1����A��ȷ��
B��CO2��ƽ��ת���� ����![]() ��100%��10%����B����
��100%��10%����B����
C��H2S(g)+CO2(g)COS(g)+H2O(g)��H����Q kJmol��1�����������·�Ӧ�ﵽƽ��ʱ����0.01molH2S���ų�������Ϊ0.01Q kJ����C��ȷ��
D�������������䣬���÷�Ӧ���¶�ΪT2�����½��У��ﵽƽ������ʱ��С��4min��˵�������˴ﵽƽ���ʱ�䣬�¶ȸ�����˷�Ӧ���ʣ��� T1��T2����D��ȷ��
��ѡ��B��


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ԭ�ӵ��ӻ�������ͺͷ��Ӽ��ι��Ͳ���ȷ���ǣ�������
A.PCl3�� Pԭ��sp3�ӻ���Ϊ������
B.BCl3��Bԭ��sp2�ӻ���Ϊƽ��������
C.CS2��Cԭ��sp�ӻ���Ϊֱ����
D.H2S��Sԭ��sp�ӻ���Ϊֱ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���2L���ܱ������м��뷴Ӧ��N2��H2���������·�Ӧ��N2(g)��3H2(g)![]() 2NH3(g)����Ӧ�����еIJ����������±���ʾ������˵����ȷ����
2NH3(g)����Ӧ�����еIJ����������±���ʾ������˵����ȷ����
���ʵ���/ mol ʱ��/min | n(N2) | n(H2) | n(NH3) |
0 | 1.0 | 1.2 | 0 |
2 | 0.9 | ||
4 | 0.75 | ||
6 | 0.3 |
A. 0��2 min�ڣ�NH3�ķ�Ӧ����Ϊ0.1 mol��L��1��min��1
B. 2 minʱ�� H2�����ʵ���0.3 mol
C. 4 minʱ����Ӧ�Ѵﵽƽ��״̬����ʱ�����淴Ӧ�����ʶ�Ϊ0
D. 4��6 min�ڣ�������������ӵ������ʵ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ҩ���л���AΪһ����ɫҺ�塣��A�����ɷ�������һϵ�з�Ӧ��
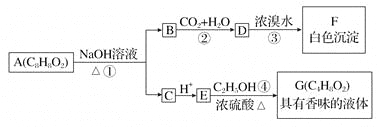
��ش�
��1��д��������F�Ľṹ��ʽ��________________��
��2��д����Ӧ�ٵĻ�ѧ����ʽ��__________________________________________��
��3��д����Ӧ�ܵĻ�ѧ����ʽ��___________________________________________��
��4���л���A��ͬ���칹��ܶ࣬��������������Ļ�����Һ��б����ṹ����________�֡�
��5��E��һ��ͬ���칹��H����֪H���Ժͽ����Ʒ�Ӧ�ų�����������һ�������¿ɷ���������Ӧ����д��H�Ľṹ��ʽ��_________________________________��E����һ��ͬ���칹��R��һ��������Ҳ���Է���������Ӧ�������ܺͽ����Ʒ�Ӧ�ų���������д��R�Ľṹ��ʽ��_____________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ˮ�к��зḻ��þ��Դ��ijͬѧ����˴�ģ�⺣ˮ���Ʊ�MgO��ʵ�鷽����

ģ�⺣ˮ�е�����Ũ��/mol��L��1 | Na�� | Mg2�� | Ca2�� | Cl�� | HCO3�� |
0.439 | 0.050 | 0.011 | 0.560 | 0.001 |
ע����Һ��ij�����ӵ�Ũ��С��1.0��10��5 mol��L��1������Ϊ�����Ӳ����ڣ�ʵ������У�������Һ������䡣Ksp[CaCO3]��4.96��10��9��Ksp[MgCO3]��6.82��10��6��Ksp[Ca(OH)2]��4.68��10��6��Ksp[Mg(OH)2]��5.61��10��12������˵����ȷ���ǣ� ��
A.������XΪCaCO3
B.��ҺM�д���Mg2����������Ca2��
C.��ҺN�д���Mg2����Ca2��
D.�����������Ϊ����4.2 g NaOH���壬������YΪCa(OH)2��Mg(OH)2�Ļ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������������裺�ټ������ܽ� �ڼ��ռ���Һ�ܽ� �۹��� ��ͨ�����![]() ����
����![]() ���� �ݼ���������
���� �ݼ���������![]() �������ɺ��������۵�������ȡ������������������ǡ��������ǣ� ��
�������ɺ��������۵�������ȡ������������������ǡ��������ǣ� ��
A.�ڢۢܢ�B.�ڢۢݢ�C.�٢ۢܢ�D.�ڢݢۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���¶��£��ı䷴Ӧ����n(SO2)���Է�Ӧ2SO2(g)+O2(g)2SO3(g) ��H<0��Ӱ����ͼ��ʾ������˵����ȷ���ǣ� ��
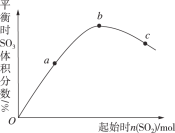
A.��Ӧbc���Ϊƽ��㣬a��δ�ﵽƽ����������Ӧ�������
B.abc�����ƽ�ⳣ��Kb>Kc>Ka
C.����ͼ����Եó�SO2�ĺ���Խ�ߵõ��Ļ��������SO3���������Խ��
D.abc�����У�a��ʱSO2��ת�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ���Դ�ͭΪԭ�ϲ�ȡ��ͼ��ʾ�����Ʊ�����ͭ���塣
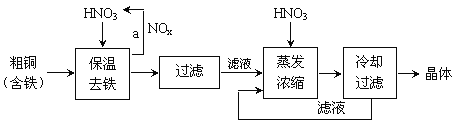
����˵���������
A.����a�л���Ҫ����������������ˮ
B.����ȥ������ˣ���Ԫ����Ҫ��+2�۵ij�����ʽ�����˳�ȥ
C.����Ũ���Ĺ����м����ʵ������ᣬĿ������������ͭ��ˮ��
D.����ͭ��Һ������Ũ�ȴ�С��![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���¶��£���2 L�����ܱ������г���1mol A������A(g) ![]() B(g) + C(g)��Ӧ����Ӧ������c(C)��ʱ��仯����������ͼ��ʾ������˵������ȷ���ǣ� ��
B(g) + C(g)��Ӧ����Ӧ������c(C)��ʱ��仯����������ͼ��ʾ������˵������ȷ���ǣ� ��
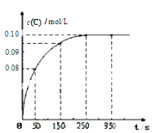
A����Ӧ�� 0 ~50 s ��ƽ������v(C)=1.6��10-3mo1/(L s)
B�����¶��£���Ӧ��ƽ�ⳣ��ֵΪ0.025
C����Ӧƽ������������г���A��B��C��1mol����ʱv(��)<v(��)
D�����������������䣬�����¶ȣ�ƽ��ʱc(B)=0.11mol/L����÷�Ӧ�ġ�H<0
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com