
【题目】有A、B、C、D、E五种短周期主族元素,它们的原子序数依次增大,已知A的L层电子数是K层电子数的两倍,D是短周期元素中原子半径最大的元素,D的单质在高温下与C的单质充分反应,可以得到与E单质颜色相同的淡黄色固态化合物,试根据以上叙述回答:
(1)元素名称:A______;B______;E______;
(2)元素E在周期表中的位置_________,B、C、D、E的原子半径由小到大的顺序为(用元素符号或化学式表示,以下同)____________,D2C2的电子式__________,所含化学键____________.
(3)写出![]() 与
与![]() 反应的化学方程式_______________________.
反应的化学方程式_______________________.
(4)C、E的简单氢化物的沸点较高的是_____________,原因是________________.
(5)用电子式表示化合物D2E的形成过程______________________.
【答案】碳 氮 硫 第三周期ⅥA族 O![]() N
N![]()
![]() 离子键和共价键
离子键和共价键 ![]() H2O 水分之间存在氢键
H2O 水分之间存在氢键 ![]()
【解析】
根据元素周期表结构、核外电子排布规律及物质性质分析元素的种类;根据元素周期律比较原子大小及物质的熔沸点;根据原子间成键特点书写电子式及判断化学键类型;根据物质性质书写相关化学方程式。
有A、B、C、D、E五种短周期主族元素,它们的原子序数依次增大,已知A的L层电子数是K层电子数的两倍,则A为碳;D是短周期元素中原子半径最大的元素,同周期元素原子半径随核电荷数增大而减小,同主族元素原子半径随核电荷数增大而增大,所以D为钠;D的单质在高温下与C的单质充分反应,可以得到与E单质颜色相同的淡黄色固态化合物,则C为氧,E为硫;B在碳、氧中间,则B为氮;
(1)根据上述分析,元素名称为:A为碳;B为氮;E为硫;
(2)元素E为硫,16号元素,在周期表中的位置为第三周期ⅥA族;同周期元素原子半径随核电荷数增大而减小,同主族元素原子半径随核电荷数增大而增大,所以B、C、D、E的原子半径由小到大的顺序为O![]() N
N![]() ;过氧化钠的电子式为:
;过氧化钠的电子式为:![]() ;氧原子间以共价键结合,过氧根和钠离子以离子键结合,所以所含化学键离子键和共价键;
;氧原子间以共价键结合,过氧根和钠离子以离子键结合,所以所含化学键离子键和共价键;
(3)过氧化钠与二氧化碳反应生成碳酸钠和氧气,反应的化学方程式为:![]() ;
;
(4)C的氢化物是H2O,常温常压下为液态,E的氢化物为H2S,常温常压下为气态,的简所以沸点较高的是H2O;原因是水分之间存在氢键;
(5)钠原子失电子形成钠离子,硫原子得电子形成硫离子,阴阳离子通过离子键结合,电子式表示化合物硫化钠的形成过程为:![]() 。
。


科目:高中化学 来源: 题型:
【题目】已知X、Y、Z、W均为中学化学中常见的单质或化合物,它们之间的转化关系如图所示(部分产物已略去)。则W、X不可能是( )

选项 | W | X |
A | 稀硫酸 | NaAlO2溶液 |
B | 稀硝酸 | Fe |
C | CO2 | Ca(OH)2溶液 |
D | Cl2 | Fe |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在某密闭容器中发生反应:2HI(g)![]() H2(g)+I2(g) ΔH>0,若15s内c(HI)由0.1mol·L-1降到0.07mol·L-1,则下列说法正确的是( )
H2(g)+I2(g) ΔH>0,若15s内c(HI)由0.1mol·L-1降到0.07mol·L-1,则下列说法正确的是( )
A. 0~15 s内用I2表示的平均反应速率为v(I2)=0.002 mol·L-1·s-1
B. c(HI)由0.07 mol·L-1降到0.05 mol·L-1所需的反应时间小于10 s
C. 升高温度正反应速率加快,逆反应速率减慢
D. 减小反应体系的体积,化学反应速率加快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机化合物的结构简式为 ,下列关于该化合物的说法不正确的是
,下列关于该化合物的说法不正确的是
A. 该有机物的分子式为C23H24O6
B. 1mol该化合物最多可以与9molH2发生加成反应
C. 既可以使溴的四氯化碳溶液褪色,又可以使酸性KMnO4溶液褪色
D. 既可以与FeCl3溶液发生显色反应,又可以与Na2CO3溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸的消费量是衡量一个国家化工生产水平的重要标志。而在硫酸的生产中,最关键的一步反应为:2SO2(g)+O2(g)![]() 2SO3(g)。
2SO3(g)。
(1)一定条件下,SO2与O2反应10 min后,若SO2和SO3物质的量浓度分别为0.1 mol/L和0.3 mol/L,则10 min内生成SO3的化学反应速率为___________;SO2的转化率为___________。
(2)下列关于该反应的说法正确的是_________。
A.增加O2的浓度能加快反应速率 B.降低体系温度能加快反应速率
C.使用催化剂能加快反应速率 D.一定条件下达到反应限度时SO2全部转化为SO3
(3)在反应过程中若某一时刻SO2、O2、SO3的浓度分别为0.2 mol/L、0.1 mol/L、0.2 mol/L。当反应达到平衡时,可能存在的数据是______。
A.O2为0.2 mol/L B.SO2为0.25 mol/L
C.SO3为0.4 mol/L D.SO2、SO3均为0.15 mol/L
(4)工业制硫酸,用过量的氨水对SO2尾气处理,请写出相关的化学方程式:___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,在2 L密闭容器内,反应2NO2(g)![]() N2O4(g) ΔH=-180 kJ·mol-1,n(NO2)随时间变化如下表:
N2O4(g) ΔH=-180 kJ·mol-1,n(NO2)随时间变化如下表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO2)/mol | 0.040 | 0.020 | 0.010 | 0.005 | 0.005 | 0.005 |
(1)用NO2表示0~2 s内该反应的平均速度___________.在第5 s时,NO2的转化率为_____。根据上表可以看出,随着反应进行,反应速率逐渐减小,其原因是_____________________。
(2)上述反应在第3 s后达到平衡,能说明该反应已达到平衡状态的是______。
a.单位时间内,消耗2 mol NO2的同时生成1 mol的N2O4
b.容器内压强保持不变
c.v逆(NO2)=2v正(N2O4)
d.容器内密度保持不变
(3)在2 s内,该反应_______(“吸收”或“放出”) _______热量。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究人员研制出一种可作为鱼雷和潜艇的储备电源的新型电池——锂水电池(结构如图),使用时加入水即可放电。下列关于该电池的说法不正确的是( )
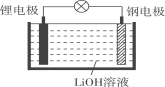
A. 锂为负极,钢为正极B. 工作时负极的电极反应式为Li-e-=Li+
C. 工作时OH-向钢电极移动D. 放电时电子的流向:锂电极→导线→钢电极
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com