
【题目】已知CH3-CH=CH2+![]() →
→![]() +CH2=CH2下列说法不正确的是( )
+CH2=CH2下列说法不正确的是( )
A. 上述四种物质互为同系物
B. 上述反应的四种分子中,所有碳原子均可以共平面
C. 与![]() 结构相似,含有双键和苯环的同分异构体还有5种
结构相似,含有双键和苯环的同分异构体还有5种
D. CH3-CH=CH2 与溴的四氯化碳溶液反应时,只能生成![]()
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】香叶醇是合成玫瑰香油的主要原料,其结构简式如图所示:下列有关香叶醇的叙述正确的是( )
A.香叶醇的分子式为C10H18O
B.不能使溴的四氯化碳溶液褪色
C.不能使酸性高锰酸钾溶液褪色
D.能发生加成反应不能发生取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】废弃物回收利用可变废为宝。某工业固体废物的组成为Al2O3、FeO、Fe2O3等。下图是以该固体废物为原料制取氧化铝、磁性Fe3O4胶体粒子的一种工艺流程:

(1)检验制备Fe3O4胶体粒子成功的实验操作名称是____________________________。
(2)写出由溶液B制备磁性Fe3O4胶体粒子的离子方程式__________________________________。
(3)由溶液B制得Fe3O4胶体粒子的过程中,须持续通入N2。其原因是____________________________。
(4)向溶液C中加入NaHCO3溶液,溶液的pH_________(填“增大”,“不变”或“减小”)。
(5)固体D是Al(OH)3,空温时Al(OH)3溶于NaOH溶液反应的平衡常数等于20,则此时Al(OH)3![]() A1O2-+H++H2O的电离常数K=_______________。
A1O2-+H++H2O的电离常数K=_______________。
(6)用重路酸钾(K2Cr2O7)可测定产物磁性Fe3O4胶体粒子中铁元素的含量,过程如下图。已知,反应中K2Cr2O7被还原为Cr3+。

①写出甲→乙的化学方程式___________________________________。
②写出乙→丙的离子方程式_________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应mA(s)+nB(g)pC(g)△H<0,在一定温度下,平衡时B的体积分数(B%)与压强变化的关系如图所示,下列叙述中一定正确的是( )
①m+n>p ②y点表示的正反应速率小于逆反应速率
③n>p ④x点比y点时的反应速率慢
⑤若降低温度,该反应的平衡常数增大.
A.①②⑤
B.②④⑤
C.只有①③
D.①③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素处于基态时的气态原子获得一个电子成为-1价阴离子时所放出的能量叫做该元素的第一电子亲和能。-1价阴离子再获得一个电子的能量变化叫做第二电子亲和能。下表中给出了几种元素或离子的电子亲和能数据:
元素 | Li | Na | K | O | O- | F |
电子亲和能/kJ·mol-1 | 59.8 | 52.7 | 48.4 | 141 | -780 | 327.9 |
下列说法正确的是( )
A. 电子亲和能越大,说明越难得到电子
B. 一个基态的气态氟原子得到一个电子成为氟离子时放出327.9kJ的能量
C. 氧元素的第二电子亲和能是-780 kJ·mol-1
D. 基态的气态氧原子得到两个电子成为O2-需要放出能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碘及其化合物在合成杀菌剂、药物等方面具有广泛用途.回答下列问题:
(1)大量的碘富集在海藻中,用水浸取后浓缩,再向浓缩液中加MnO2和H2SO4 , 即可得到I2 , 写出该反应的离子方程式 .
(2)一种碘和氧的化合物(I4O9),可以称为碘酸碘,则I4O9中碘元素的化合价是 .
A.﹣1
B.+1
C.+3
D.+5
(3)若IOH是两性化合物,写出IOH的酸式电离的电离方程式 .
(4)已知反应2HI(g)═H2(g)+I2(g)△H=+11kJmol﹣1 , 1mol H2(g)、1mol I2(g)分子中化学键断裂时分别需要吸收436kJ、151kJ的能量,则1mol HI(g)分子中化学键断裂时需吸收的能量为kJ.
(5)Bodensteins研究了下列反应:2HI(g)H2(g)+I2(g).在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如表:
t/min | 0 | 20 | 40 | 60 | 80 | 120 |
x(HI) | 1 | 0.91 | 0.85 | 0.815 | 0.795 | 0.784 |
x(HI) | 0 | 0.60 | 0.73 | 0.773 | 0.780 | 0.784 |
①根据上述实验结果,该反应的平衡常数K的计算式为: .
②上述反应中,正反应速率为υ正=k正x2(HI),逆反应速率为υ逆=k逆x(H2)x(I2),其中k正、k逆为速率常数,则k逆为(以K和k正表示).
③由上述实验数据计算得到υ正~x(HI)和υ逆~x(H2)的关系可用如图表示.当升高到某一温度时,反应重新达到平衡,相应的点分别为(填字母).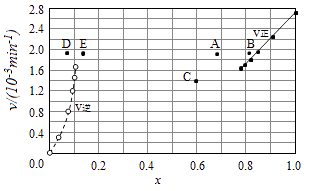
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色济液中,只可能含有以下离子中的若干种:NH4+、K+、Mg2+、Cu2+、Al3+、NO3-、CO32-、SO42-,,现取三份100mL溶液进行如下实验:
①第一份加足量AgNO3溶液后,有白色沉淀产生。
②第二份加足量BaCl2溶液后,有白色沉淀产生,经洗涤、干燥后,沉淀质量为6.99g
③第三份逐滴滴加NaOH溶液,测得沉淀与NaOH溶液的体积关系如图。根据上述实验,试回答下列问题:

(1)该溶液中一定不存在的阴离子有_______。
(2)实验③中NaOH溶液滴至35mL后发生的离子方程式为_______________________________。
(3)原得液确定含Mg2+、Al3+、NH4+,且n(Mg2+)∶n(Al3+)∶n(NH4+)=___________。
(4)实验所加的NaOH溶液的浓度为________。
(5)溶液中存在一种不能确定的阳离子,请设计实验方案加以检验_________________________。
(6)原溶液中NO3-的浓度为c(NO3-)则c(NO3-)的最小浓度为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,回答下列有关问题:
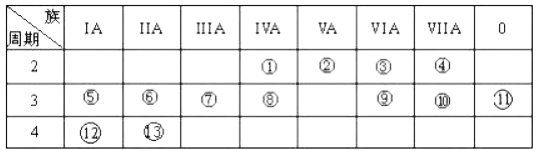
(1)写出下列元素名称:②_________;___________。
(2)在这些元素中,金属性最强的元素是______(用元素符号表示),元素⑨与元素⑩相比,非金属性较强的是___________(用元素符号表示)。下列表述中能证明这一事实的是______________。
a.常温下⑨的单质和⑩的单质状态不同
b. ⑩的氢化物比⑨的氢化物稳定
c.一定条件下⑨和⑩的单质都能与氢氧化钠溶液反应
(3)⑦的最高价氧化物对应水化物与⑩的最高价氧化物对应水化物反应的离子方程式为:______。
(4)②的气态氢化物与HC1在空气中相遇有白烟生成,写出白烟对应物质的电子式_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com