
| A�� | ������������ʱ��ʹ�ø�Ч������������ʹNO��ת�������� | |
| B�� | ƽ��ʱ�������������䣬����NH3��ƽ�������ƶ���NH3��ת�������� | |
| C�� | �����������ܶȲ����ˣ���Ӧ�ﵽ��ѧƽ��״̬ | |
| D�� | ƽ��ʱ�������������䣬�����¶ȿ�ʹ�÷�Ӧ��ƽ�ⳣ������ |
���� A��ʹ�ô���ƽ�ⲻ�ƶ���
B�����ӷ�Ӧ���Ũ�ȣ�ƽ�������ƶ���������ת���ʽ��ͣ�
C�����ݵ���ϵ���������ܶ�һֱ���䣻
D������Ӧ�ķ��ȷ�Ӧ�¶�Խ��KֵԽС��
��� �⣺A��ʹ�ô���ƽ�ⲻ�ƶ�������ʹ�ø�Ч������NO��ת���ʲ��䣬��A��ȷ��
B�����ӷ�Ӧ���Ũ�ȣ�ƽ�������ƶ���������ת���ʽ��ͣ����Գ���NH3��ƽ�������ƶ���NH3��ת���ʼ�С��һ��������ת��������B����
C�����ݵ���ϵ���������ܶ�һֱ���䣬��һ����ƽ��״̬����C����
D������Ӧ�ķ��ȷ�Ӧ�¶�Խ��KֵԽС�����������¶ȿ�ʹ�÷�Ӧ��ƽ�ⳣ����С����D����
��ѡA��
���� ���⿼����������Ի�ѧ��Ӧ���ʵ�Ӱ�졢ƽ��״̬���жϵȣ�����ʱע��ƽ�ⳣ���ı仯�Լ�ƽ��״̬���жϷ�����


 ABC����ȫ�ž�ϵ�д�
ABC����ȫ�ž�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ֱ�ӼӼ������ҺpH��9.6 | |
| B�� | ��������ͭ�ۣ���Fe2+��ԭ���� | |
| C�� | ��������п�ۣ���Fe2+��ԭ���� | |
| D�� | �Ƚ�Fe2+������Fe3+���ٵ���pH��3��4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

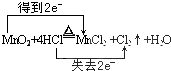 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ϡHNO3�еμ�Na2SO3��Һ��SO32-+2H+�TSO2��+H2O | |
| B�� | ��Na2SiO3��Һ��ͨ�����SO2��SiO32-+SO2+H2O�TH2SiO3��+SO32- | |
| C�� | ��CuSO4��Һ�м���Na2O2��2Na2O2+2Cu2++2H2O�T4Na++2Cu��OH��2��+O2�� | |
| D�� | ��Al2��SO4��3��Һ�м��������NH3•H2O��Al3++4NH3•H2O�TAlO2-+4NH4++2H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1 mol Na2SiO3���NA��Na2O | |
| B�� | ��H2O2+Cl2�T2HCl+O2��Ӧ�У�ÿ����32 g��������ת��NA������ | |
| C�� | ��״���£�������ΪNA��CO��C2H4����������Լ22.4 L������Ϊ28 g | |
| D�� | 4.6 g Na������������ȫ��Ӧ����Na2O��Na2O2����Ӧ��ת�Ƶĵ�����Ϊ0.1NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����������Ϊ40%���ܶ�Ϊ1.43g•cm-3����NaOH��Һ������ˮ��ϣ�������Һ�����ʵ�����������20% | |
| B�� | Ҫ����Ũ��Ϊ0.25mol•L-1��NaOH��Һ480mL��Ӧ����4.8gNaOH��250mL���ձ����ܽ⣬��ȴ����ת�Ƶ�500mL����ƿ�У�ϴ�ӡ�ת�ơ����� | |
| C�� | ����һ�����ʵ���Ũ�ȵ���Һ������ʱ���ӿ̶��ߵ�������Ũ��ƫ�� | |
| D�� | ͨ��Cl2����ȥFe2��SO4��3��Һ�е�FeSO4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 6��1 | B�� | 5��1 | C�� | 1��5 | D�� | 3��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
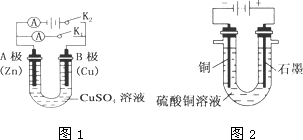 �밴Ҫ��ش��������⣮
�밴Ҫ��ش��������⣮�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com