
【题目】海带中含有丰富的碘。为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:
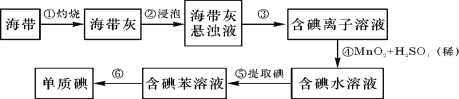
(1)从上述步骤中可知,海带中含有的碘元素的主要存在形式是 (填化学式)。
(2)步骤①灼烧海带时,除需要三脚架、泥三角外,还需要用到的实验仪器是 (从下列仪器中选出所需的仪器,用标号字母填写在空白处)。
A烧杯 B表面皿 C坩埚 D酒精灯 E干燥器
(3)步骤⑥是从含碘苯溶液中分离出单质碘和回收苯,还需经过蒸馏,指列实验装置中的错误之处。
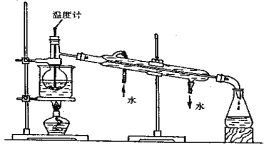
① ;② ;③ ;
进行上述蒸馏操作时,使用水浴的原因是 ;最后晶态碘在 里聚集。
(4)步骤④反应的离子方程式是 。若用碘盐中的KIO3作氧化剂,在酸性溶液中氧化I—,写出反应的离子方程式 。
(5)检验海带中是否含有碘元素,可以在步骤④后进行,检验时可用的试剂是 。
(6)步骤⑤中,某学生选择用苯来提取碘,其实验操作可分解为如下几步:
(A)把盛有溶液的分液漏斗放在铁架台的铁圈中;
(B)把50毫升碘水和15毫升苯加入分液漏斗中,并盖好玻璃塞;
(C)检验分液漏斗活塞和上口的玻璃塞是否漏液;
(D)倒转漏斗用力振荡,并不时旋开活塞放气,最后关闭活塞,把分液漏斗放正;
(E)旋开活塞,用烧杯接收溶液;
(F)将分液漏斗上口倒出上层溶液;
(G)将漏斗上口的玻璃塞打开或使塞上的凹槽或小孔对准漏斗口上的小孔;
(H)静置,分层。
就此实验,完成下列填空:
正确操作步骤的顺序是 → → →A→G→ →E→F
【答案】(1)I—;
(2)C D;
(3)①温度计水银球位置没有放在蒸馏烧瓶的支管口;②冷凝管中的水流方向错误;③加热时在烧杯上没有垫石棉网;使用水浴的原因:受热均匀,容易控制反应温度, 反应温度低于100℃;蒸馏烧瓶;
(4)2I—+4H++MnO2=I2+Mn2++2H2O;5I—+6H++IO3-=3I2+3 H2O
(5)淀粉;
(6)C;B;D;H。
【解析】
试题分析:(1)步骤③得到含碘离子的溶液,故答案为:碘离子;
(2)灼烧固体物质一般使用(瓷)坩埚,而坩埚加热需要用泥三脚支撑然后放在三脚架上,三脚架下面的空间放酒精灯,故答案为:CD;
(3)根据蒸馏的注意事项可知,图中出现以下错误:①温度计水银球的位置错误,应与蒸馏瓶支管下沿平齐;②烧杯下没垫石棉网,否则加热时会受热不均而炸裂;③冷冷凝管中凝水的流向错误,冷水应从下方进,上方出;用酒精灯直接加热温度变化快,而水浴加热试管内试剂受热比较均匀;步骤⑥是从含碘苯溶液中分离出单质碘和回收苯;所以碘在蒸馏烧瓶中聚集;故答案为:①温度计水银球的位置错误,应与蒸馏瓶支管下沿平齐;②烧杯下没垫石棉网,否则加热时会受热不均而炸裂;③冷冷凝管中凝水的流向错误,冷水应从下方进,上方出;受热均匀,容易控制反应温度, 反应温度低于100℃;蒸馏烧瓶;
(4)碘离子在酸性条件下可被MnO2氧化,反应的离子方程式为2I-+MnO2+4H+=Mn2++I2+2H2O;若用碘盐中的KIO3作氧化剂,在酸性溶液中氧化I—生成碘单质,反应的离子方程式为5I—+6H++IO3-=3I2+3 H2O,故答案为:2I-+MnO2+4H+=Mn2++I2+2H2O;5I—+6H++IO3-=3I2+3 H2O;
(5)碘遇淀粉变蓝色,故答案为:淀粉试液;
(6)CCl4从碘水中萃取碘并用分液漏斗分离两种溶液,操作为查漏→装液→振荡→静置→分液,则步骤为C→B→D→A→G→H→E→F,故答案为:C;B;D;H。


科目:高中化学 来源: 题型:
【题目】将金属a放入b(NO3)2溶液中发生如下反应:a+b2+===a2++b,则下列说法正确的是( )
A.常温下,a或b可以与水发生反应
B.a与b用导线连接插入稀H2SO4中,则形成原电池且b极上有H2放出
C.a与b用导线连接插入b(NO3)2溶液中一定构成原电池
D.用惰性电极电解a(NO3)2与b(NO3)2的混合液,在阳极先析出b
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知电极材料:铁、铜、银、石墨、锌、铝;电解质溶液:CuCl2溶液、Fe2(SO4)3溶液、盐酸.按要求回答下列问题:
①电工操作上规定:不能把铜导线和铝导线连接在一起使用.请用电化学知识说明原因 .
②若电极材料选铜和石墨,电解质溶液选硫酸铁溶液,外加导线,能否构成原电池? 能 (填“能”或“不能”),若能,请写出电极反应式, .
③若用石墨作电极,电解1L0.1mol/L盐酸,当转移0.5mol电子时,阳极得到气体的体积(标况)为 L.
(2)被誉为改变未来世界的十大新科技之一的燃料电池具有无污染、无噪音、高效率的特点.如图为氢氧燃料电池的结构示意图,电解质溶液为KOH溶液,电极材料为疏松多孔石墨棒.当氧气和氢气分别连续不断地从正、负两极通入燃料电池时,便可在闭合回路中不断地产生电流.试回答下列问题:
①写出氢氧燃料电池工作时正极电极反应方程式: .
②如果该氢氧燃料电池每转移0.1mol电子,消耗标准状况下氧气 .
③若将此燃料电池改进为直接以甲烷和氧气为原料进行工作时,负极反应式为 .

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有50 mL NaOH溶液,向其中逐渐通入一定量的CO2,随后取此溶液10 mL将其稀释至100 mL,并向此稀释后的溶液中逐滴加入0.1 mol·L-1的HCl溶液,产生CO2气体的体积(标准状况)与所加入盐酸的体积之间的关系如下图所示:
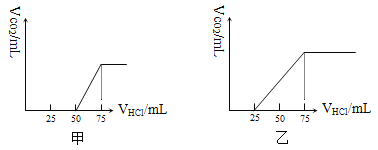
(1)甲溶液中的溶质是_____________,其物质的量之比为__________________。
(2)乙溶液中的溶质是_____________,在标准状况下吸收CO2气体的体积为________。
(3)原NaOH溶液的物质的量浓度为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在两份相同的Ba(OH)2溶液中,分别滴入物质的量浓度相等的H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示。下列分析不正确的是( )
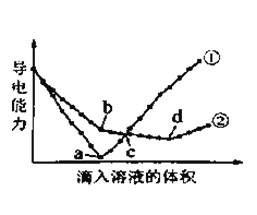
A. ①代表滴加H2SO4溶液的变化曲线
B. b点,溶液中大量存在的离子是Na+、OH–
C. c点,两溶液中含有相同量的OH–
D. a、d两点对应的溶液均显中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向50mLNa2SO4和Na2CO3的混合溶液中加入过量的BaCl2溶液,得到14.51g白色沉淀,向白色沉淀中加入过量的稀HNO3,充分反应后,沉淀减少到4.66g,并有气体产生。
(1)原混合溶液中Na2SO4的物质的量浓度是______________。
(2)产生的气体在标准状况下的体积是______________。
(3)原溶液中Na+物质的量浓度是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关燃料的说法错误的是( )
A.含硫化石燃料的大量燃烧是形成酸雨的主要原因
B.绿色化学的核心就是利用化学原理对工业生产上造成的环境污染进行彻底治理
C.以压缩天然气、液化石油气代替燃油可减少大气污染
D.燃料不完全燃烧排放的CO是大气污染物之一
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据估计,地球上的绿色植物通过光合作用每年能结合来自CO2中的碳1500亿吨和来自水中的氢250亿吨,并释放4000亿吨氧气。光合作用的过程一般可用下式表示:

CO2+H2O+微量元素(P、N等)![]() (蛋白质、碳水化合物、脂肪等)+O2
(蛋白质、碳水化合物、脂肪等)+O2
下列说法不正确的是
A. 某些无机物通过光合作用可转化为有机物
B. 碳水化合物就是碳和水组成的化合物
C. 叶绿素是光合作用的催化剂
D. 增加植被,保护环境是人类生存的需要
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com