
已知下图中物质M是由同一短周期的两种元素组成的离子化合物,焰色反应为黄色,阴离子元素最高正价与它的负价代数和为6。X具有漂白性,Y为碱性气体,W是对空气无污染的气体。试回答下列问题:
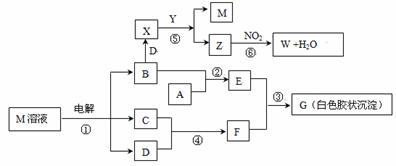
(1)写出电解M溶液①的化学方程式 。
(2)已知工业上制备Y气体,每生成1molY时放出的热量为akJ(该热量已合算成25℃,101KP),请写该反应的热化学方程式 。
(3)若A是一种常见金属,写出反应②的离子方程式 。
(4)若A是某元素的一种常见酸性氧化物,则A的化学式为 ;其用途为 。(写出一种即可)
(5)写出反应⑤的化学方程式 。
(6)标准状况下,反应⑥中生成11.2L W时转移的电子数 。(用NA表示阿伏加德罗常数)
科目:高中化学 来源: 题型:
氧化还原反应中,水可以是氧化剂、还原剂、既是氧化剂又是还原剂、既非氧化剂又非还原剂等。下列反应与Cl2+SO2+2H2O===H2SO4+2HCl相比较,水的作用不相同的是
A.3NO2+H2O===2HNO3+NO B.2Na2O2+2H2O===4NaOH+O2↑
C.4Fe(OH)2+2H2O+O2===4Fe(OH)3 D.3Fe+4H2O(g)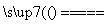 Fe3O4+4H2
Fe3O4+4H2
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,在溶液中可以发生反应:X + 2Y3+ == X2+ + 2Y2+ ,则下列解释正确的是 ( )
①X被氧化 ②X是氧化剂 ③X具有还原性 ④Y2+是氧化产物 ⑤Y2+具有还原性 ⑥Y3+ 的氧化性比X2+强
A、②⑤ B、②④⑥ C、①③④ D、①③⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关热化学方程式的叙述正确的是
| A | 已知2H2O(g)= 2H2(g)+O2(g) △H=+483.6 kJ/mol,则氢气的燃烧热为 △H=﹣241.8kJ/mol | |
| B. | 已知C(石墨,s)= C(金刚石,s) △H>0,则金刚石不如石墨稳定 | |
|
| C. | 已知中和热为△H =﹣57.3kJ/mol,则稀醋酸和稀NaOH溶液反应的热化学方程式为: NaOH(aq)+ CH3COOH(aq)= CH3COONa(aq)+ H2O(l)△H=﹣57.3kJ/mol |
|
| D. | 已知2C(s)+ 2O2(g) = 2CO2 (g) △H1; 2C(s)+ O2 (g) = 2CO(g) △H2,则△H1>△H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列示意图与对应的反应情况符合的是
A.向含0.01mol KOH和0.01mol Ca(OH)2的混合溶液中缓慢通入CO2至过量
B.向NaHSO4溶液中逐滴加入Ba(OH)2溶液至过量
C.向KAl(SO4)2溶液中逐滴加入Ba(OH)2溶液至过量
D.向NaAlO2溶液中逐滴加入盐酸至过量

查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
A.化学反应中的能量变化,只表现为热量的变化 B.煤和石油属于可再生能源
C.汽车排出大量尾气中含有CO会污染大气 D.要使燃料燃烧只需要大量的氧气
查看答案和解析>>
科目:高中化学 来源: 题型:
根据以下3个热化学方程式:
2H2S(g)+3O2(g)=2SO2(g)+2H2O(l) △H=Q1 kJ/mol
2H2S(g)+O2(g)=2S (s)+2H2O(l) △H=Q2 kJ/mol
2H2S(g)+O2(g)=2S (s)+2H2O(g) △H=Q3 kJ/mol
判断Q1、Q2、Q3三者关系正确的是( )
A. Q1>Q2>Q3 B. Q1>Q3>Q2 C. Q3>Q2>Q1 D. Q2>Q1>Q3
查看答案和解析>>
科目:高中化学 来源: 题型:
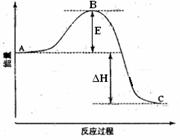
2SO2(g)+O2(g) =2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3(g)的ΔH= —99kJ·mol-1。请回答下列问题:
(1)图中A表示 ,E的大小对该反应的反应热 (填“有”或“无”)影响。该反应通常用V2O5作催化剂,加V2O5会使图中B点 (填“升高”还是“降低”),△H (填“变大”、“变小”或“不变”),理由是
(2)已知单质硫的燃烧热为296 KJ·mol-1,计算由S(s)生成3 molSO3(g)的△H(要求计算过程)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com