
����Ŀ������������ת���У�A��һ�����Σ�D����Է���������C����Է���������16��E���ᣬ��X������ǿ�ỹ��ǿ��ʱ���������µ�ת����ϵ��
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
��X��ǿ��ʱ��A��B��C��D��E����ͬһ��Ԫ�أ���X��ǿ��ʱ��A��B��C��D��E��������ͬһ��Ԫ�ء���ش�
(1)A��________��Y��________��Z��________��
(2)��X��ǿ��ʱ��B��________E��________��д��B����C�Ļ�ѧ����ʽ��_________________��д��C����D�Ļ�ѧ����ʽ��__________________��
(3)��X��ǿ��ʱ��B��________E��________��
���𰸡� (NH4)2S O2 H2O H2S H2SO4 2H2S��3O2![]() 2SO2��2H2O 2SO2��O2
2SO2��2H2O 2SO2��O2![]() 2SO3 NH3 HNO3
2SO3 NH3 HNO3
��������A��һ�����Σ�D����Է���������C����Է���������16����������ͼ֪��YΪ������E���ᣬ��ZΪˮ����X��ǿ��ʱ��A��B��C��D��E����ͬһ��Ԫ������BΪH2S��CΪSO2��DΪSO3��EΪH2SO4��ZΪH2O����X��ǿ��ʱ��A��B��C��D��E��������ͬһ��Ԫ������BΪNH3��CΪNO��DΪNO2��EΪHNO3��ZΪH2O�����AΪ��NH4��2S��
��1����������������AΪ��NH4��2S��YΪO2��ZΪH2O���ʴ�Ϊ����NH4��2S��O2��H2O��
��2����X��ǿ��ʱ����������ķ�����֪��B��H2S��E�� H2SO4��B����C�Ļ�ѧ����ʽΪ2H2S+3O2![]() 2SO2+2H2O��C����D�Ļ�ѧ����ʽΪ2SO2��O2
2SO2+2H2O��C����D�Ļ�ѧ����ʽΪ2SO2��O2![]() 2SO3���ʴ�Ϊ��H2S��H2SO4��2H2S+3O2
2SO3���ʴ�Ϊ��H2S��H2SO4��2H2S+3O2![]() 2SO2+2H2O��2SO2��O2
2SO2+2H2O��2SO2��O2![]() 2SO3��
2SO3��
��3����X��ǿ��ʱ����������ķ�����֪��B��NH3��E�� HNO3���ʴ�Ϊ��NH3��HNO3��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ˮ�ⷴӦ����ʽΪ��HCOOCH3��l��+H2O��l��HCOOH��l��+CH3OH��l����H��0ij�¶��£�V L�����ϵ�и���ֵ���ʼ�����±���HCOOCH3ת�����淴Ӧʱ��t�ı仯��ͼ����������ϵ������䣩������˵����ȷ���ǣ� ��
��� | ���ʵ���/mol |
HCOOCH3 | 1.00 |
H2O | 1.99 |
HCOOH | 0.01 |
CH3OH | 0.52 |
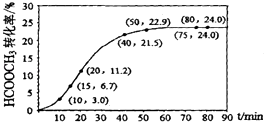
A.�¶����{���÷�Ӧ��ƽ�ⳣ����С
B.010min��HCOOCH3��ƽ����Ӧ����v=0.003molL��1min��1
C.HCOOCH3ˮ��ƽ����Ӧ�������������С����ֲ���
D.�������´ﵽƽ��״̬����Ӧ��ת�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����100mL �����Һ�У�HNO3�� H2SO4�����ʵ���Ũ�ȷֱ���0.1mol/L��0.4mol/L��û��Һ�м��� 2.56gͭ�ۣ����ȴ���ַ�Ӧ��������Һ�� Cu2+�����ʵ���Ũ����mol/L ��������Һ������䣩
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͭ������Һ�м�����ˮ����ͭ����ֽ������ ��
A.����ͭ�����ܽ����ֹͣB.����ͭ����ᾧ����ֹͣ
C.����ͭ����ᾧ���ʵ����ܽ�����D.����ͭ��Һ��Ϊ��������Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ȤС������ͼװ��̽�����Ĵ�������
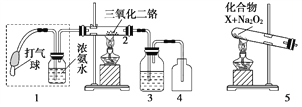
(1)���������Ļ�ѧ����ʽΪ____________________________________��
(2)���Ȳ�����2һ��ʱ���ѹ1�д��������������۲쵽2�����ʳʺ���״̬��ֹͣ���Ⱥ����ܱ��ֺ��ȣ��÷�Ӧ��________��Ӧ(����ȡ����ȡ�)��
(3)Ϊ��֤��װ��4�н��۲쵽����ɫ���壬װ��3Ӧװ��________����ȡ��3����4�н��۲쵽�������̣�ԭ����___________________________________��
(4)Ϊʵ�ְ���������Ҳ����װ��5�滻װ��________(��װ�ô���)��������XΪ________(ֻдһ��)��Na2O2��������_____________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����3L���ܱ������г���2mol A�����2mol B���壬��һ�������·�����Ӧ��2A��g��+B��g��2C��g������ƽ��ʱ������ͬ�¶��²�������ڻ�������ѹǿ�Ƿ�Ӧǰ��0.8������A��ת����Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ָ������������½���ѧ��ת��Ϊ���ܵ�װ�ã��乤��ԭ����ͼ��ʾ�������й������ص�˵��������ǣ� �� 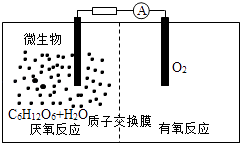
A.������Ӧ����CO2����
B.����ٽ��˷�Ӧ�е��ӵ�ת��
C.����ͨ������Ĥ�Ӹ���������������
D.����ܷ�ӦΪC6H12O6+6O2�T6CO2+6H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijϡ��Һ�к���Fe(NO3)3��Cu(NO3)2��HNO3�����������������ۣ���Һ��Fe2+��Ũ����������۵����ʵ���֮��Ĺ�ϵ��ͼ��ʾ����ϡ��Һ��Fe(NO3)3��Cu(NO3)2��HNO3�����ʵ���Ũ��֮��Ϊ(����)

A. 1��1��4
B. 1��3��1
C. 3��3��8
D. 1��1��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ӱ�컯ѧ��Ӧ���ʵ���Ҫ�����ǣ����¶� ��ѹǿ �۴��� ��Ũ�� �ݷ�Ӧ�ﱾ�������ʣ� ��
A.�٢ڢۢܢ�
B.��
C.�٢�
D.�٢ڢۢ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com