
【题目】现有常温下pH=2的盐酸甲和pH=2的醋酸溶液乙,请根据下列操作回答问题:
(1)常温下0.lmol/L的CH3COOH溶液加水稀释过程,下列表达式的数据一定增大的是__________
A.c(H+) B.c(H+)/c(CH3COOH) C.c(H+)·c(OH-) D.c(OH-)/c(H+)
(2)取10mL乙溶液,加入等体积水,醋酸的电离平衡___________(填“向左”、“向右”或“不”)移动;另取10mL的乙溶液,加入少量无水醋酸钠固体 (假设加入固体前后,溶液体积保持不变),待固体溶解后,溶液中c(H+)/c(CH3COOH)的比值将___________(填“增大”“ 减小”或“无法确定”)。
(3)取等体积的甲、乙两溶液,分别用等浓度的NaOH稀溶液中和,则消耗的NaOH溶液的体积大小关系为:V(甲)___________V(乙) (填“>”、“ <”或“=”)。
(4)已知25℃时,两种酸的电离平衡常数如下:
化学式 | CH3COOH | H2CO3 | HClO |
电离平衡常数K1 | 1.8×l1-5 | 4.3×l0-7 | 3.0×10-8 |
K2 | - - | 5.6×10-11 | - - |
下列四种离子结合H+能力最强的是___________;
A.HCO3- B.CO32- C.ClO- D.CH3COO-
(5)常温下,取甲溶液稀释100倍,其pH=___________;取99mL甲溶液与lrnLlmol/L的NaOH溶液混合(忽略溶液体积变化),恢复至常温时其pH=______________。
【答案】 BD 向右 减小 < B 4 10
【解析】本题主要考查弱电解质的电离平衡。
(1)A.酸性减弱,c(H+)减小;B.稀释过程中水的电离程度增大,水电离产生的H+、OH-增多,所以c(H+)/c(CH3COOH)增大;C.水的离子积不变,所以c(H+)c(OH-)不变;D. c(OH-)增大,c(H+)减小,所以c(OH-)/c(H+)增大,故选BD。
(2)取10mL乙溶液,加入等体积水,稀释促进醋酸电离,醋酸的电离平衡向右移动;另取10mL的乙溶液,加入少量无水醋酸钠固体,待固体溶解后,由于Ka=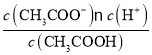 不变,c(CH3COO-)增大,所以c(H+)/c(CH3COOH)的比值将减小。
不变,c(CH3COO-)增大,所以c(H+)/c(CH3COOH)的比值将减小。
(3)取等体积的甲、乙两溶液,分别用等浓度的NaOH稀溶液中和,由于醋酸电离程度很小,醋酸溶液浓度大于盐酸,所以消耗的NaOH溶液的体积大小关系为:V(甲)<V(乙)。
(4)下列四种离子结合H+能力最强的也就是生成物酸性最弱的,故选B;
(5)c(OH-)=![]() =0.0001mol/L,pH=10。
=0.0001mol/L,pH=10。


科目:高中化学 来源: 题型:
【题目】锌电池比铅蓄电池容量更大,而且没有铅污染。其电池反应为:2Zn+O2=2ZnO,原料为锌粉、电解液和空气,则下列叙述正确的是
A. 锌为正极,空气进入负极反应 B. 负极反应为Zn-2e-=Zn2+
C. 正极发生氧化反应 D. 电解液可能是强酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通过观察钠与水(含酚酞)的反应现象,不能得出的结论是
A. 钠的密度比水小 B. 钠是活泼金属,与水反应后溶液呈碱性
C. 钠有良好的延展性 D. 钠的熔点低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是周期表中的一部分,根据A﹣I在周期表中的位置,第(1)~(4)小题用元素符号或化学式回答,(5)~(8)小题按题目要求回答.
族 | I A | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | O |
1 | A | |||||||
2 | D | E | G | I | ||||
3 | B | C | F | H |
(1)表中元素,化学性质最不活泼的是 , 只有负价而无正价的是 , 氧化性最强的单质是 , 还原性最强的单质是 .
(2)最高价氧化物的水化物碱性最强的是 , 酸性最强的是 , 呈两性的是 .
(3)A分别与D,E,F,G,H形成的化合物中,最稳定的 ,
(4)在B,C,E,F,G,H中,原子半径最大的是 ,
(5)A和D组成最简单化合物的电子式 ,
(6)A和E组成化合物的化学式 ,
(7)用电子式表示B和H组成化合物的形成过程: .
(8)B的最高价氧化物的水化物和C的最高价氧化物相互反应的离子方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列电离方程式错误的是
A. Na2CO3=2Na++CO32- B. H2SO4=2H++SO42-
C. MgCl2=Mg2++Cl2- D. Ba(OH)2=Ba2++2OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应X(g)+Y(g)![]() 2Z(g) ΔH<0,一段时间后达到平衡,反应过程中测定的数据如下表:
2Z(g) ΔH<0,一段时间后达到平衡,反应过程中测定的数据如下表:
t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
下列说法正确的是
A. 该温度下此反应的平衡常数K=1.44
B. 其他条件不变,降低温度,反应达到新平衡前ν(逆)>ν(正)
C. 反应前2min的平均速率ν(Z)=2.0×10-3mol·L-1·min-1
D. 其他条件不变,再充入0.2mol Z,平衡时X的体积分数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A. 已知I3-![]() I2+I-,向盛有KI3溶液的试管中加入适量CCl4,振荡静置后CCl4层显紫红色,说明KI3在CCl4中的溶解度比在水中的大
I2+I-,向盛有KI3溶液的试管中加入适量CCl4,振荡静置后CCl4层显紫红色,说明KI3在CCl4中的溶解度比在水中的大
B. 室温下向10mL pH =3的醋酸溶液中加水稀释后,溶液中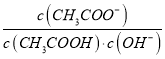 减小
减小
C. 室温时ka(HF)=3.6×10-4,ka(CH3COOH)=1.75×10-5,0.1 mol /L的NaF溶液与0.1 mol /L的CH3COOK溶液相比,一定有c(Na+) -c(F-)<c(K+)-c(CH3COO-)成立
D. 在25℃时,将amol/L的氨水与0.01 mol/L的盐酸等体积混合,充分反应后溶液中c(NH4+)=c(Cl-),则25℃时NH3 H2O的电离常数Kb=![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】给定条件下,下列选项中所示的物质间转化能一步实现的是( )
A.Na ![]() Na2O2
Na2O2 ![]() Na2CO3
Na2CO3
B.MgCO3 ![]() MgCl2溶液
MgCl2溶液 ![]() Mg
Mg
C.Al2O3 ![]() Al(OH)3
Al(OH)3 ![]() AlCl3
AlCl3
D.S ![]() SO3
SO3 ![]() H2SO4
H2SO4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com