
室温下,将20 ml 5.0×10-6 mol/L的盐酸和80 ml 1.0×10-6 mol/L的NaOH溶液混合,充分反应后将溶液稀释至1000 ml,试计算稀释后溶液的PH.
科目:高中化学 来源: 题型:
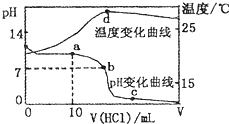 室温下,将1.00mol?L-1盐酸滴入20.00 mL 1.00mol?L-1的氨水中,溶液pH和温度随加入盐酸体积的变化曲线如图所示.下列有关说法中不正确的是( )
室温下,将1.00mol?L-1盐酸滴入20.00 mL 1.00mol?L-1的氨水中,溶液pH和温度随加入盐酸体积的变化曲线如图所示.下列有关说法中不正确的是( )A、a点溶液中离子浓度大小的关系:c(NH
| ||
B、b点溶液中离子浓度大小的关系:c(NH
| ||
C、c点溶液中离子浓度大小的关系:c(NH
| ||
| D、d点时溶液温度达到最高,之后温度略有下降,原因是NH3?H2O电离吸热 |
查看答案和解析>>
科目:高中化学 来源:2013-2014学年福建省漳州市七校高三第二次联考化学试卷(解析版) 题型:选择题
室温下,将0.100 0 mol·L-1盐酸滴入20.00 ml 未知浓度的某一元碱MOH溶液中,溶液pH随加入盐酸体积变化曲线如图。下列有关说法不正确的是

A.该一元碱溶液浓度为0.100 0 mol·L-1
B.a、b、c点的水溶液导电性依次增强
C.室温下,MOH的电离常数Kb=1×10-5
D.b点:c(M+)+c(MOH)=c(Clˉ)
查看答案和解析>>
科目:高中化学 来源:2011-2012学年河南省郑州市高三第一次质量预测化学试卷(解析版) 题型:选择题
室温下,将1.00mol • L-1盐酸滴人20. OO mL 1.OOmol • L-1的氨水中,溶液pH和温度随加入盐酸体积的变化曲线如下图所示。
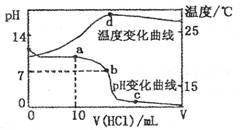
下列有关说法中不正确的是
A.
a点溶液中离子浓度大小的关系:
B.
b点溶液中离子浓度大小的关系:
C.
c点溶液中离子浓度大小的关系:
D. d点时溶液温度达到最高,之后温度略有下降,原因是NH3 • H2O电离吸热
查看答案和解析>>
科目:高中化学 来源:2011-2012学年湖北省高三上学期期中考试化学试卷 题型:填空题
(9分)有A、B、C、D四种短周期元素在周期表中相对位置如右图:
|
A |
|
|
|
|
|
B |
C |
D |
(1)A与D形成的液态化合物是常见的重要有机溶剂,则A、B、C、D四种元素最高价氧化物对应的水化物酸性由强到弱的顺序是:_______>_________>___________>______(用化学式表示),B、C、D三种元素的第一电离能由大到小的顺序是:______________(用元素符号表示)(2)X、Y为C、D两种元素形成的单质。标准状况下,X的密度为3.17 g/L。Z是一种化合物,焰色反应呈紫色(透过蓝色钴玻璃),室温下0.1 mol/L Z水溶液pH=13。X、Y、Z有如图转化关系:
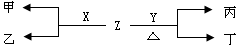
①写出X与Z反应的离子方程式:_____________________________
②已知丙能与稀硫酸反应生成使品红褪色的气体。丁的化学式_______,丁的水溶液pH>7的原因: ___________________________________(用离子方程式表示)
③将20 mL 0.5 mol/L丙溶液逐滴加入20 mL 0.2 mol/L KMnO4溶液(硫酸酸化)中,恰好褪色。写出反应的离子方程式 _________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com