
【题目】下列物质中含有共价键的离子化合物是( )
A. Ba(OH)2 B. CaCl2 C. H2O D. H2
科目:高中化学 来源: 题型:
【题目】短周期元素X和Y可以形成XY4型化合物,若X的原子序数为a,Y的原子序数为b,则a和b的相互关系不可能是( )
A. a-13 = b
B. a +8 = b
C. b-11 = a
D. b+5 = a
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CaCO3与稀盐酸反应生成CO2的量与反应时间的关系如图所示。下列结论不正确的是
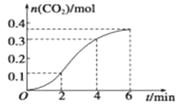
A. 反应在2~4 min内平均反应速率最大
B. 反应开始4 min内温度比浓度对反应速率的影响大
C. 4 min后,反应速率减小的主要原因是c(H+)减小
D. 反应在2~4 min内生成CO2的平均反应速率为v(CO2)=0.1 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列鉴别方法不可行的是
A. 用水鉴别乙醇、甲苯和溴苯
B. 用溴水鉴别已烯、苯和四氯化碳
C. 用酸性高锰酸钾溶液鉴别苯、乙醇和已烷
D. 用碳酸钠溶液鉴别乙醇、乙酸和乙酸乙酯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某种制取纯碱的生产流程如下图所示:
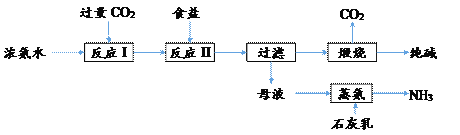
完成下列填空:
(1)N原子核外有_______种不同运动状态的电子,它的最外层电子排布式是________;组成纯碱的元素原子半径从大到小依次为___________________。
(2)氨水是常用氮肥,用氨水施肥时要避开高温、大风天气,原因是_______________。
(3)用离子方程式表示碳酸钠被称为“碱”的原因_____________________________ 。
(4)结合下图用溶解平衡理论解释反应II的反应原理____________________________________。
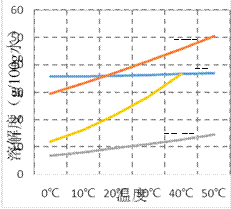
(5)在向母液中通入石灰乳进行蒸氨之前,通常需要先将母液加热。若不加热,加入石灰乳容易产生沉淀堵塞管道,生成的沉淀是________。
(6)上述流程中可以循环利用的物质有________,副产物是______________。
(7)利用化工生产遵循的一般原则分析上述纯碱生产流程,指出不足之处____________________(写一条)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某强酸性溶液X,可能含有Al3+、Ba2+、NH4+、Fe2+、Fe3+、CO32-、SO42ˉ、SiO32ˉ、NO3ˉ中的一种或几种离子,取该溶液进行实验,其现象及转化如图.反应过程中有一种气体是红棕色。
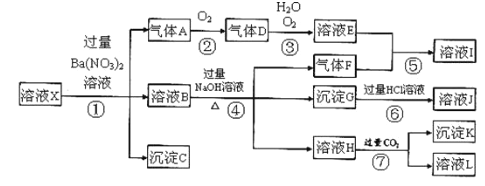
请回答下列问题:
(1)由强酸性条件即可判断溶液X中一定不存在的离子有___________________________。
(2)溶液X中,关于NO3—的判断一定正确的是_____________。
a.一定有 b.一定没有 c.可能有
(3)产生气体A的离子方程式为_________________,并用双线桥表示电子转移的方向和数目。
(4)若转化③中D过量,通常用强碱溶液进行吸收,写出该反应的离子方程式___________________。
(5)对不能确定是否存在的离子,可以另取X溶液,加入下列溶液中的一种,根据现象即可判断,该试剂可选择___________________。
①NaOH溶液 ②KSCN溶液 ③石蕊试剂 ④pH试纸 ⑤KMnO4溶液 ⑥氯水和KSCN的混合溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:[CoCl4]2-(蓝色)与[Co(H2O)6]2+(粉红色)之间存在如下平衡:[CoCl4]2-+6H2O [Co(H2O)6]2++4Cl- △H<0。现有呈现紫色的氯化钴溶液。
(1)甲同学向上述溶液中通入HC1,发现溶液变为___色;
(2)乙同学向上述溶液中加水,平衡___(填“向右”、“向左”或“不”)移动。为使平衡保持该移动方向,还可采取的措施有____(写一种)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,不属于取代反应的是( )
A. CH3Cl+Cl2![]() CH2Cl2+HCl
CH2Cl2+HCl
B. CH4+2O2![]() CO2+H2O
CO2+H2O
C. CH3CH2Br +H2O→CH3CH2OH + HBr
D. CH3CH3+Cl2![]() C2H5Cl+HCl
C2H5Cl+HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学-—选修3:物质结构与性质]东晋《华阳国志南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)闻名中外,曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
(1)镍元素基态原子的电子排布式为_________,3d能级上的未成对的电子数为______。
(2)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。
①[Ni(NH3)6]SO4中阴离子的立体构型是_____。
②在[Ni(NH3)6]2+中Ni2+与NH3之间形成的化学键称为______,提供孤电子对的成键原子是_____。
③氨的沸点(填“高于”或“低于”)膦(PH3),原因是______;氨是_____分子(填“极性”或“非极性”),中心原子的轨道杂化类型为_______。
(3)单质铜及镍都是由______键形成的晶体:元素铜与镍的第二电离能分别为:ICu=1959kJ/mol,INi=1753kJ/mol,ICu>INi的原因是______。
(4)某镍白铜合金的立方晶胞结构如图所示。

①晶胞中铜原子与镍原子的数量比为_____。
②若合金的密度为dg/cm3,晶胞参数a=________nm。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com