
【题目】ClO2是国际上公认安全、无毒的绿色消毒剂,在常温下是一种黄绿色有刺激性气味的气体熔点为-59℃,沸点为11.0℃,易溶于水。ClO2有多种制备方法。
I.某实验小组拟用图示装置模拟工业制取并收集ClO2。
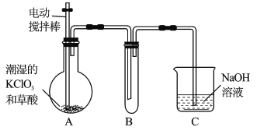
(1)A装置必须添加温度控制装置,除酒精灯外,还需要的玻璃仪器有烧杯、_________。
(2)B装置必须放在冰水浴中,其原因是___________。
II.我国的科学家经过科学探索,发现一种ClO2的制备方法,该方法安全性好,没有产生毒副产品。将经干燥空气稀释的氯气通入填充有固体亚氯酸钠(NaClO2)的反应柱内,即生成ClO2。
(3)化学反应方程式为:___________。
III.以过氧化氢作还原剂,在硫酸介质中还原NaClO3制备ClO2,并将制得的ClO2处理含CN-废水。实验室模拟该过程的实验装置(夹持装置略)如图所示。
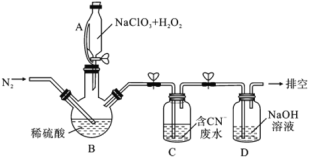
(4)反应容器B应置于30℃左右的水浴中,目的是_________。
(5)通入氮气的目的除了有利于将ClO2排出,还有____________。
(6)ClO2处理含CN-废水的离子方程式为______。装置D的作用是____________。
【答案】温度计 ClO2的沸点为11.0℃,易挥发,应充分冷却以减少挥发 2NaClO2+Cl2=2NaCl+2ClO2 提高化学反应速率,同时防止H2O2受热分解(或答:高于30 ℃会导致H2O2分解,低于30 ℃会导致反应速率较低) 稀释ClO2,防止其发生爆炸 2CN-+2ClO2=2CO2+N2+2Cl- 吸收ClO2等气体,防止污染大气
【解析】
(1)A装置必须添加温度控制装置,需要测量温度,所需仪器为温度计,故本题答案为:温度计;
(2)二氧化氯沸点较低,易挥发,收集二氧化氯,应在较低温度下进行,故本题答案为:ClO2的沸点为11.0℃,易挥发,应充分冷却以减少挥发;
(3)将氯气通入亚氯酸钠(NaClO2)的反应柱内,生成ClO2,化学反应方程式为:2NaClO2+Cl2=2NaCl+2ClO2,故本题答案为:2NaClO2+Cl2=2NaCl+2ClO2;
(4)适当升高温度可以提高化学反应速率,但是注意到,本题中选用的还原剂是过氧化氢,而过氧化氢在温度过高时会分解,所以反应容器B置于30C左右的水浴中的目的是提高化学反应速率,同时防止H2O2受热分解,故本题答案为:提高化学反应速率,同时防止H2O2受热分解(或答:高于30 ℃会导致H2O2分解,低于30 ℃会导致反应速率较低);
(5)由题意可知,ClO2的体积分数在超过10%时易引起爆炸,所以通入氮气的目的除了将ClO2排出外,还可以起到稀释ClO2气体的作用,防止ClO2的体积分数过高从而引起爆炸,故本题答案为:稀释ClO2,防止其发生爆炸;
(6)ClO2具有强氧化性,能够和具有还原性的CN-发生氧化还原反应,根据氧化还原反应的配平规律可得二者反应的离子方程式为:2CN-+2ClO2=2CO2+N2+2Cl-,装置D中盛装的碱性溶液,可以吸收ClO2气体,避免对空气造成污染,故本题答案为:2CN-+2ClO2=2CO2+N2+2Cl-;吸收ClO2等气体,防止污染大气。


科目:高中化学 来源: 题型:
【题目】氟离子电池是一种前景广阔的新型电池,其能量密度是目前锂电池的十倍以上且不会因为过热而造成安全风险。如图是氟离子电池工作示意图,其中充电时F-从乙电极流向甲电极,下列关于该电池的说法正确的是( )

A.放电时,甲电极的电极反应式为Bi-3e-+3F-=BiF3
B.放电时,乙电极电势比甲电极高
C.充电时,导线上每通过1mole-,甲电极质量增加19g
D.充电时,外加电源的正极与乙电极相连
查看答案和解析>>
科目:高中化学 来源: 题型:
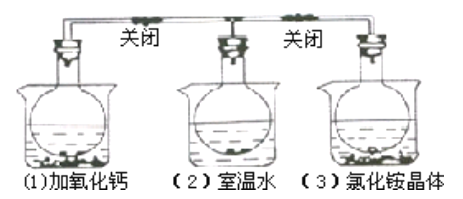
【题目】三个烧瓶中分别充满NO2气体并分别放置在盛有下列物质的烧杯(烧杯内有水)中:在(1)中 加入CaO,在(2)中不加其他任何物质,在(3)中加入NH4Cl晶体,发现(1))中红棕色变深,(3)中红棕色变浅,下列叙述正确的是( )
A. 2NO2![]() N2O4是放热反应
N2O4是放热反应
B. NH4Cl溶于水时放出热量
C. 烧瓶(1)中平衡混合气的平均相对分子质量增大
D. 烧瓶(3)中气体的压强增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组利用NaI溶液中通入少量Cl2得到含碘废液,再利用含碘废液获取NaI固体,实验流程如下:

已知反应②:2I﹣+2Cu2++![]() +H2O
+H2O![]() 2CuI↓+
2CuI↓+![]() +2H+。
+2H+。
回答下列问题:
(1)过滤实验所需要的玻璃仪器有普通漏斗、烧杯、_____________。
(2)反应③中CuI被氧化,还原产物只有NO2,该反应的化学方程式为_________________。当有95.5 g CuI参与反应,则需要标况下______________L的O2才能将生成的NO2在水中完全转化为硝酸。
(3)化合物B中含两种元素,铁原子与另一种元素原子的物质的量之比为3∶8,则化合物B的化学式为_____________。
(4)反应⑤中生成黑色固体和无色气体,黑色固体的俗称为磁性氧化铁,则反应⑤的化学方程式为______。
(5)将足量的Cl2通入含12 g NaI的溶液中,一段时间后把溶液蒸干得到固体的质量为_________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,A(g)+B(g) ![]() C(g) ΔH<0,达到平衡后根据下列图象判断:
C(g) ΔH<0,达到平衡后根据下列图象判断:

(1)升高温度,达到新平衡的是________(填“A”、“B”、“C”、“D”、“E”,下同),新平衡中C的体积分数______(填“增大”、“减小”、“不变”,下同)。
(2)减小压强,达到新平衡的是________,A的转化率________。
(3)减小C的量,达到新平衡的是________。
(4)增加A的量,达到新平衡的是________,此时B的转化率________,A的转化率________。
(5)使用催化剂,达到新平衡的是________,C的质量分数________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种用软锰矿(主要成分MnO2)和黄铁矿(主要成分FeS2)制取MnSO4·H2O并回收单质硫的工艺流程如下:
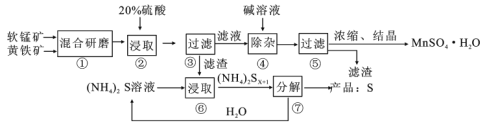
(1)步骤①混合研磨成细粉的主要目的是__________;步骤②浸取时若生成S、MnSO4及Fe2(SO4)3,则反应的离子方程式为___________。
(2)步骤③所得酸性滤液可能含有Fe2+,检验Fe2+的方法是________;除去Fe2+的方法是__________。步骤④是破坏Fe(OH)3胶体并使沉淀颗粒长大,便于过滤分离。步骤⑤所得滤渣为___________(填化学式)。
(3)步骤⑦需在90~100℃下进行,该反应的化学方程式为___________。
(4)硫化铵水解的离子方程式为:S2-+![]() +H2O
+H2O![]() HS-+NH3·H2O,如何判断溶液的酸碱性______。
HS-+NH3·H2O,如何判断溶液的酸碱性______。
(5)测定产品MnSO4·H2O的方法之一是:准确称取a g产品于锥形瓶中,加入适量ZnO及H2O煮沸,然后用c mol·L-1 KMnO4标准溶液滴定至浅红色且半分钟不褪,消耗标准溶液V mL,滴定反应的离子方程式为2![]() +3Mn2++2H2O=5MnO2↓+4H+,产品中Mn2+的质量分数为ω(Mn2+)=___________。
+3Mn2++2H2O=5MnO2↓+4H+,产品中Mn2+的质量分数为ω(Mn2+)=___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学兴趣小组对某品牌牙膏中的摩擦剂成分及其含量进行以下探究:查得资料:该牙膏摩擦剂由碳酸钙、氢氧化铝组成;牙膏中其它成分遇到盐酸时无气体产生。
Ⅰ.摩擦剂中氢氧化铝的定性检验
取适量牙膏样品,加水充足搅拌、过滤。
(1)往滤渣中加入过量 NaOH溶液,过滤。氢氧化铝与NaOH溶液反应的离子方程式是_________________。
(2)往(1)所得滤液中先通入过量二氧化碳,再加入过量稀盐酸,观察到的现象是__________________,通入过量二氧化碳的离子方程式是_________________。
Ⅱ.牙膏样品中碳酸钙的定量测定
利用下图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定C中生成的BaCO3沉淀质量,以确定碳酸钙的质量分数。
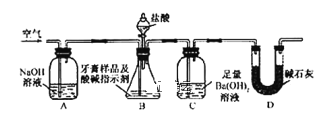
依据实验过程回答下列问题:
(3)实验过程中需持续缓缓通入空气。其作用除了可搅拌B、C中的反应物外,还有:_____。
(4)C中反应生成沉淀的离子方程式是________。
(5)下列各项措施中,不能提高测定准确度的是___(填标号)。
a.在加入盐酸之前,应排净装置内的CO2气体
b.滴加盐酸不宜过快
c.在A-B之间增添盛有浓硫酸的洗气装置
d.在B-C之间增添盛有饱和碳酸氢钠溶液的洗气装置
(6)实验中准确称取8.0g样品三份,进行三次测定,测得BaCO3平均质量为3.94 g。则样品中碳酸钙的质量分数为__________。
(7)有人认为不必测定C中生成的BaCO3质量,只要测定装置C在吸收CO2前后的质量差,一样可以确定碳酸钙的质量分数。实验证明按此方法测定的结果明显偏高,原因是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】屈昔多巴( ![]() )是一种抗帕金森氏病药物。以下是屈昔多巴的一种合成路线(
)是一种抗帕金森氏病药物。以下是屈昔多巴的一种合成路线( ![]() 简写为BnCl,
简写为BnCl, ![]() 简写为CbzCl ):
简写为CbzCl ):

回答下列问题:
(1)反应①的反应类型为_________,其作用为_____________。
(2)屈昔多巴中所含的非含氧官能团名称为_______________,屈昔多巴分子中有_____个手性碳原子。
(3)反应②为加成反应,则有机物X的名称为________________。
(4)![]() 显________性(填“酸”、“中”或“碱”)。
显________性(填“酸”、“中”或“碱”)。
(5)![]() 的同分异构体中,能与NaHCO3溶液反应生成CO2的二取代芳香化合物有_____种,其中核磁共振氢谱为四组峰的结构简式为___________________________。
的同分异构体中,能与NaHCO3溶液反应生成CO2的二取代芳香化合物有_____种,其中核磁共振氢谱为四组峰的结构简式为___________________________。
(6)参照上述合成路线,以对羟基苯甲醛为原料(无机试剂任选),设计制备对羟基苯甲酸的合成路线: __________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知合成氨反应N2(g)+ 3H2(g) ![]() 2NH3(g) △H<0,当反应器中按n(N2): n(H2)=1:3投料后,在不同温度下,反应达到平衡时,得到混合物中NH3的物质的量分数随压强的变化曲线a,b,c如下图所示。下列说法正确的是( )
2NH3(g) △H<0,当反应器中按n(N2): n(H2)=1:3投料后,在不同温度下,反应达到平衡时,得到混合物中NH3的物质的量分数随压强的变化曲线a,b,c如下图所示。下列说法正确的是( )

A. 曲线a对应的反应温度最高
B. 上图中M、N、Q点平衡常数K的大小关系为K(M)=K(Q)<K(N)
C. 相同压强下,投料相同,达到平衡所需时间关系为c>b>a
D. N点时 c(NN3)=0.2 mol/L,则 N点的c(N2): c(NH3)=1:1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com