
����Ŀ��һ�������̿�(��Ҫ�ɷ�MnO2)�ͻ�����(��Ҫ�ɷ�FeS2)��ȡMnSO4��H2O�����յ�����Ĺ����������£�
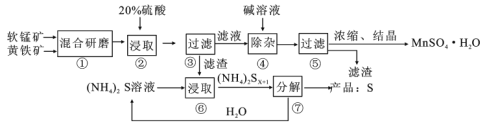
(1)����ٻ����ĥ��ϸ�۵���ҪĿ����__________������ڽ�ȡʱ������S��MnSO4��Fe2(SO4)3����Ӧ�����ӷ���ʽΪ___________��
(2)���������������Һ���ܺ���Fe2+������Fe2���ķ�����________����ȥFe2+�ķ�����__________����������ƻ�Fe(OH)3���岢ʹ�������������ڹ��˷��롣�������������Ϊ___________(�ѧʽ)��
(3)���������90��100���½��У��÷�Ӧ�Ļ�ѧ����ʽΪ___________��
(4)���ˮ������ӷ���ʽΪ��S2-��![]() ��H2O
��H2O![]() HS-��NH3��H2O������ж���Һ�������______��
HS-��NH3��H2O������ж���Һ�������______��
(5)�ⶨ��ƷMnSO4��H2O�ķ���֮һ�ǣ�ȷ��ȡa g��Ʒ����ƿ�У���������ZnO��H2O��У�Ȼ����c mol��L-1 KMnO4����Һ�ζ���dz��ɫ�Ұ���Ӳ��ʣ����ı���ҺV mL���ζ���Ӧ�����ӷ���ʽΪ2![]() ��3Mn2+��2H2O��5MnO2����4H+����Ʒ��Mn2+����������Ϊ��(Mn2+)��___________��
��3Mn2+��2H2O��5MnO2����4H+����Ʒ��Mn2+����������Ϊ��(Mn2+)��___________��
���𰸡���������ȡʱ�Ľ�ȡ�� 3MnO2 +2FeS2+12H+=3Mn2++2Fe3++4S��+6H2O ȡ������Һ���Թ��У�������������Һ����ɫ��ȥ ����H2O2��MnO2 Fe(OH)3 (NH4)2Sx+1=2NH3��+H2S��+xS�� �Ƚ�SH-��![]() ˮ�ⳣ������Դ�С
ˮ�ⳣ������Դ�С ![]() ��100��
��100��
��������
���̿��̿����ĥ��������Ӵ�������ӿ췴Ӧ���ʣ���������ܽ��̣�������轫��Һ��������Ȼ���ڲ��Ͻ����¼���Ŀ���ƻ������������壬ʹ֮�������õ���������Һ����Ũ�����ᾧ�õ�MnSO4��H2O���ݴ˽��
(1)����ٻ����ĥ��ϸ�ۣ���������Ӧ��ĽӴ��������������ȡʱ�Ľ�ȡ�ʣ������ȡ�ķ�Ӧ����ʽΪ��3MnO2 +2FeS2+12H+=3Mn2++2Fe3++4S��+6H2O���ʱ����Ϊ����������ȡʱ�Ľ�ȡ�ʣ�3MnO2 +2FeS2+12H+=3Mn2++2Fe3++4S��+6H2O��
(2)�������Ӿ��н�ǿ�Ļ�ԭ�ԣ����Ժ�����ط�Ӧ���ʼ����������ӣ��ɼӸ�����أ�����ɫ��ɫ�������������ӣ�Ҫ��ȥ�������ӣ����Լ�����������ȥ��Ҳ���Լ���������̽�������������Ϊ�����ӣ�������轫��Һ��������Ȼ���ڲ��Ͻ����¼�������pH4~5���ټ������һ��ʱ�䣬���������"��Ŀ���ƻ������������壬ʹ֮���������ڹ��˷��룬��˲������������Ϊ�����������ʱ����Ϊ��ȡ������Һ���Թ��У�������������Һ����ɫ��ȥ������H2O2��MnO2��Fe(OH)3��
(3)���������90~100���½��У���Ӧ�Ļ�ѧ����ʽΪ(NH4)2Sx+1=2NH3��+H2S��+xS�����ʱ����Ϊ��(NH4)2Sx+1=2NH3��+H2S��+xS����
(4) S2-��NH4+������ˮ�⣬NH4+ˮ������ԣ�S2-ˮ��ʼ��ԣ���Һ�������ȡ�����������백ˮ���볣������Դ�С���ʱ����Ϊ���Ƚ�SH-��NH4+ˮ�ⳣ������Դ�С��
(5)��֪��ʵ�������£����������Һ����������Һ��ϲ����������̣���Ӧ�����ӷ���ʽΪ
2![]() ��3Mn2+��2H2O��5MnO2����4H+��
��3Mn2+��2H2O��5MnO2����4H+��
n(KMnO4)=c mol/L��v��10-3L=cV��10-3mol����Ʒ��Mn2+����������Ϊ(1.5cv��10-3mol��55g/mol)/ag��100��=![]() ��100�����ʱ����Ϊ��
��100�����ʱ����Ϊ��![]() ��100����
��100����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������c���Ʊ�ԭ�����£�
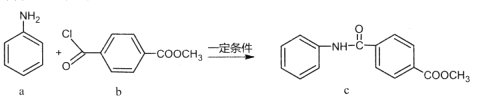
����˵����ȷ����
A.�÷�ӦΪ�ӳɷ�ӦB.������a������ԭ��һ����ƽ��
C.������C��һ�ȴ�������Ϊ5��D.������b��c������NaOH��Һ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��COCl2(g)![]() CO(g)��Cl2(g) ��H>0������Ӧ�ﵽƽ��ʱ�����д�ʩ�������� ������ͨ��������� ������COŨ�� ����ѹ ���Ӵ��� ����ѹͨ��������壬�����COCl2ת���ʵ���
CO(g)��Cl2(g) ��H>0������Ӧ�ﵽƽ��ʱ�����д�ʩ�������� ������ͨ��������� ������COŨ�� ����ѹ ���Ӵ��� ����ѹͨ��������壬�����COCl2ת���ʵ���
A. �٢ܢ�B. �٢ڢ�C. �ڢۢ�D. �ۢݢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ����ѧ��ѧ�г�������֮���һЩ��Ӧ��ϵ�����в��ֲ���δд����������X�ǹ��壬B��G��Һ�壬�����Ϊ���塣������ͼ��ϵ�ƶϣ�

(1)д����ѧʽ��X_______��A________��B_______��
(2)ʵ�����ռ�����D��F�ķ���������_______����________����
(3)д��C��E�Ļ�ѧ����ʽ��____________��
(4)��д��A��E��Ӧ����D�Ļ�ѧ����ʽ��_______________
(5)��������A�ķ�����������________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ClO2�ǹ����Ϲ��ϰ�ȫ��������ɫ���������ڳ�������һ�ֻ���ɫ�д̼�����ζ�������۵�Ϊ��59�����е�Ϊ11.0����������ˮ��ClO2�ж����Ʊ�������
I.ijʵ��С������ͼʾװ��ģ�ҵ��ȡ���ռ�ClO2��
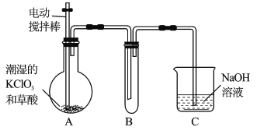
(1)Aװ�ñ��������¶ȿ���װ�ã����ƾ����⣬����Ҫ�IJ����������ձ���_________��
(2)Bװ�ñ�����ڱ�ˮԡ�У���ԭ����___________��
II.�ҹ��Ŀ�ѧ�Ҿ�����ѧ̽��������һ��ClO2���Ʊ��������÷�����ȫ�Ժã�û�в���������Ʒ�������������ϡ�͵�����ͨ������й�����������(NaClO2)�ķ�Ӧ���ڣ�������ClO2��
(3)��ѧ��Ӧ����ʽΪ��___________��
III.�Թ�����������ԭ��������������л�ԭNaClO3�Ʊ�ClO2�������Ƶõ�ClO2������CN-��ˮ��ʵ����ģ��ù��̵�ʵ��װ��(�г�װ����)��ͼ��ʾ��
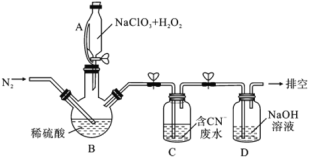
(4)��Ӧ����BӦ����30�����ҵ�ˮԡ�У�Ŀ����_________��
(5)ͨ�뵪����Ŀ�ij��������ڽ�ClO2�ų�������____________��
(6)ClO2������CN-��ˮ�����ӷ���ʽΪ______��װ��D��������____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ�У�����ȡ����Ӧ����(����)
��CH3CH===CH2��Br2![]() CH3CHBrCH2Br
CH3CHBrCH2Br
��CH3CH2Br��NaOH![]() CH2===CH2����NaBr��H2O
CH2===CH2����NaBr��H2O
��C6H6��HNO3![]() C6H5NO2��H2O
C6H5NO2��H2O
��CH3COOH��CH3CH2OH![]() CH3COOCH2CH3��H2O
CH3COOCH2CH3��H2O
A.�٢�B.�ۢ�C.�٢�D.�ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ������CH4ȼ�պ�õ��IJ�����CO��CO2��H2O(g),�˻���������Ϊ49.6 g,���仺��ͨ����������ˮCaCl2ʱ������������25.2 g,��������CO������Ϊ( )��
A. 24.4 gB. 13.2 gC. 12.5 gD. 11.2 g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ǰ�(NH2OH)��ˮ��Һ�еĵ��뷽��ʽΪ��NH2OH+H2O![]() NH3OH++OH-����0.1mol/L����ζ�20mL0.1mol/L NH2OH��Һ���㶨25��ʱ���ζ���������ˮ���������OH-Ũ�ȵĸ���������������Ĺ�ϵ��ͼ��ʾ������˵��������ǣ� ��
NH3OH++OH-����0.1mol/L����ζ�20mL0.1mol/L NH2OH��Һ���㶨25��ʱ���ζ���������ˮ���������OH-Ũ�ȵĸ���������������Ĺ�ϵ��ͼ��ʾ������˵��������ǣ� ��
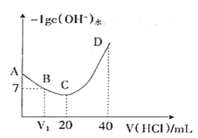
A.A��D��Һ�У�NH2OH���볣������
B.��A��D��ˮ�������c(OH-)��С
C.B���Ӧ����Һ��c(Cl-)=c(NH3OH+)
D.C���Ӧ����Һ��c(H+)=c(OH-)+ c(NH2OH)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��G��ҩ��ϳɵ��м��壬�䲿�ֺϳ�·�����£�
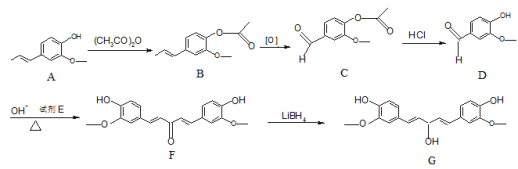
��֪��RCHO + CH3COR1 ![]() RCH=CHCOR1 + H2O
RCH=CHCOR1 + H2O
��ش��������⣺
(1)C��D�ķ�Ӧ����Ϊ_______________��
(2)�Լ�E������Ϊ_____________��G�ķ���ʽΪ_______________��
(3)д��A��B�Ļ�ѧ����ʽ__________________________________��
(4)���A��B�����Ŀ����__________________ ��
(5)�����廯����T��D��ͬ���칹�壬�������������Ľṹһ����___ �֡�
���ܷ���������Ӧ��
����FeCl3��Һ��������ɫ��Ӧ������ϡ�����е�ˮ�����֮һ��FeCl3��Һ�ܷ�����ɫ��Ӧ��
���ں˴Ź���������������壻
(6)�Ի�������![]() Ϊԭ�ϣ��ϳ�
Ϊԭ�ϣ��ϳ�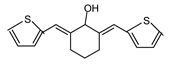 ��·��Ϊ__________________________��
��·��Ϊ__________________________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com