
X、Y、Z、W、Q五种前四周期元素,原子序数依次增大。已知五种元素中只有一种为金属元素, XW2是通常呈液态的有机物,元素W的原子序数等于元素Z的原子序数加8,Q的最外层电子数为1,次外层电子数等于Y和W2 - 最外层电子数之和。根据以上信息回答下列问题:(用元素符号或化学式等化学用语回答)
(1)XW2的电子式为 。
(2)Y原子中电子运动状态有 种, Z的气态氢化物在同主族元素气态氢化物中最高是因为 。
(3)Q在周期表中的位置 ,其基态原子简化电子排布式为 。交警可以用H2SO4酸化的K2 Cr2O7溶液检测驾驶员是否酒驾,其产物为乙酸、Q3+等。
请写出此原理的离子方程式 。
(4)含W的两种元素种类相同的酸式铵盐溶液反应的离子方程式
。
(5)某种燃料电池一极通乙醇的最简单同系物蒸气,一极通Z2,以NaOH溶液为电解液。请写出该原电池负极的电极反应式 。
(1) 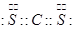
(2) 7 H2O分子间易形成氢键
(3)第四周期 第VIB族 [Ar]3d54s1
2Cr2O72—+3C2H5OH+16H+=4Cr3++3CH3COOH+11H2O
(4)H++HSO3―=H2O+SO2↑
(5)CH3OH—6e—+8OH—=CO32—+6H2O
解析试题分析: 据题意五种元素中只有一种为金属元素,Q的最外层电子数为1可知Q为金属元素。再有XW2是通常呈液态的有机物可联想到CS2故X为碳,W为硫。元素W的原子序数等于元素Z的原子序数加8,可知Z的原子序数为8,即Z为氧元素。再由交警可以用H2SO4酸化的K2Q2O7溶液检测驾驶员是否酒驾,其产物为乙酸、Q3+等。可知Q为Cr元素。Q的最外层电子数为1,次外层电子数等于Y和W2 - 最外层电子数之和,铬的次外层电子数为13,可知Y的最外层电子数为5.所以Y为氮元素。
考点:考查元素周期表的相关知识点。


科目:高中化学 来源: 题型:单选题
下列叙述中,正确的是 ( )
| A.两种微粒,若核外电子排布完全相同,则其化学性质一定相同 |
| B.凡单原子形成的离子,一定具有稀有气体元素原子的核外电子排布 |
| C.两原子,如果核外电子排布相同,则一定属于同种元素 |
| D.阴离子的核外电子排布一定与上一周期稀有气体元素原子的核外电子排布相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
把A、B、C、D四块金属泡在稀H2SO4中,用导线两两相连可以组成各种原电池。若A、B相连时,A为负极;C、D相连,D上有气泡逸出;A、C相连时A极减轻;B、D相连,B为正极。则四种金属的活泼性顺序由大到小排列为
A. A>B>C>D B. A>C>B>D C. A>C>D>B D. B>D>C>A
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
英国化学家戴维(Davy)用电解法成功地制出了金属钾和钠。他临终前在医院养病期间,一位朋友去看他,问他一生中最伟大的发现是什么,他绝口未提自己发现的众多化学元素中的任何一个,却说:“我最大的发现是一个人——法拉第!”钠(Na)在周期表中的位置是
| A.第二周期第IA族 | B.第二周期第IIA族 |
| C.第三周期第IA族 | D.第三周期第IIA族 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
短周期元素X、Y、Z、W的原子序数依次增大,X原子的最外层电子数是其内层电子总数的3倍,Y原子的最外层只有2个电子,Z单质可制成半导体材料,W与X属于同一主族。下列叙述正确的是( )
| A.原子半径的大小顺序: Y<Z<W<X |
| B.化合物YX、ZX2、WX3中化学键的类型相同 |
| C.非金属性的强弱顺序:X>W>Z |
| D.元素W的最高价氧化物对应水化物的酸性比Z的弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(9分)下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列
问题: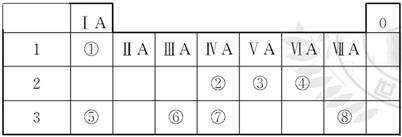
(1)④、⑤、⑥的原子半径由大到小的顺序是____________。
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是____________。
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:_____________________________________。
(4)由表中两种元素的原子按1∶1组成的常见液态化合物的稀溶液易被催化分解,可使用的催化剂为(填序号)_______________________________________。
a.MnO2 b.FeCl3 c.Na2SO3 d.KMnO4
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(每空1分,共6分)
A、B、C、D、E、F为六种短周期主族元素,它们的原子序数依次增大;A元素的原子半径最小;B元素原子的最外层电子数是次外层电子数的3倍;C与A同主族,且与E同周期;E元素的最外层电子数是次外层电子数的0.75倍,D既可与C的最高价氧化物的水化物反应,也可与E的最高价氧化物的水化物反应,均有A元素的单质生成。
请回答下列问题:
(1)写出F元素原子结构示意图 ,元素B在周期表中的位置 。
(2)判断C、D、E原子半径的大小顺序 (填写元素符号,下同),比较B和E的气态氢化物的稳定性大小 。
(3)写出单质D与C的最高价氧化物的水化物反应的离子方程式 。
(4)由A、B、C、E四种元素共同构成的两种化合物在溶液中相互间可发生化学反应,试写出该反应的离子方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(6分)A、B、C三种元素的原子具有相同的电子层数,而B的核电荷数比A大1,C原子的电子总数比B原子的电子总数多4; 1molA的单质跟足量盐酸反应,可置换出标准状况下22.4L的H2,这时A转变为与氖原子具有相同电子层结构的离子。请回答:
(1)用电子式表示A和C组成的化合物的形成过程为______________________;
(2)B离子的电子式是 ,与B的离子具有相同电子数的分子中,有一种分子
可与盐酸化合生成盐,该分子的电子式是 ;
周期表中与C上下相邻的同族元素形成的气态氢化物中,沸点最高的是 ,(填
氢化物化学式),原因是 ;
写出B最高价氧化物的水化物和C最高价氧化物的水化物之间反应的离子方程式(本
题涉及的含C元素的物质均易溶于水): 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(14分)下图是元素周期表的一部分
| ① | | | | | | | | | | | | | | | | | |
| | ② | | | | | | | | | | | | ③ | ④ | ⑤ | | |
| ⑥ | | | | | | | | | | | | ⑦ | | | | ⑧ | |
| | | | ⑨ | | | | ⑩ | | | | | | | | | | |
| 元素代号 | I1 | I2 | I3 | I4 |
| Q | 2080 | 4000 | 6100 | 9400 |
| R | 500 | 4600 | 6900 | 9500 |
| S | 740 | 1500 | 7700 | 10500 |
| T | 580 | 1800 | 2700 | 11600 |
| U | 420 | 3100 | 4400 | 5900 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com