
【题目】在一次有机化学课堂小组讨论中,某同学设计了下列合成路线,你认为不可行的是( )
A.用氯苯合成环己烯: ![]()
B.用甲苯合成苯甲醇: ![]()
C.用乙烯合成乙酸: C2H4![]() CH3CH2OH
CH3CH2OH![]() CH3CHO
CH3CHO![]() CH3COOH
CH3COOH
D.用乙烯合成乙二醇: H2C=CH2![]() CH3CH3
CH3CH3![]() CH2ClCH2Cl
CH2ClCH2Cl![]() HOCH2CH2OH
HOCH2CH2OH
 提分百分百检测卷系列答案
提分百分百检测卷系列答案 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案科目:高中化学 来源: 题型:
【题目】汉黄芩素是传统中草药黄芩的有效成分之一,对肿瘤细胞的杀伤有独特作用。下列有 关汉黄芩素的叙述正确的是
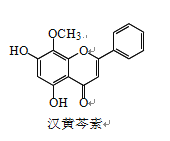
A. 汉黄芩素的分子式为 C16H13O5
B. 该物质遇 FeCl3 溶液显色
C. 1 mol 该物质与溴水反应,最多消耗 1 mol Br2
D. 与足量 H2 发生加成反应后,该分子中官能团的种类减少 1 种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用镁和稀硫酸反应,不仅可以测定1mol氢气的体积,装置如下左图,也可以测定镁带中镁的质量分数(杂质与酸反应不产生气体),装置如图。
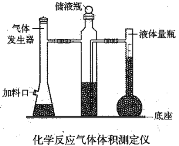
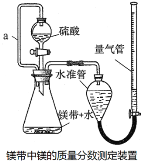
(1)用离子方程式表示测定实验的反应原理____________________________________。
(2)硫酸必须过量的目的是__________________________________________________。
(3)用“化学反应气体体积测定仪”测定1mol氢气的体积时,要三次用到注射器,其中两次是抽气调压,还有一次是___________________________________________。
(4)a(g)镁和足量稀硫酸反应,镁完全反应后,测得氢气在常温时的体积为V(L),则常温下l mol氢气的体积为_________________L。
(5)某学生在测定1molH2体积时,镁中混有少量铝,测定结果将_______________(填:偏大、偏小或没有变化)。
(6)若用“化学反应气体体积测定仪”也可以测定1mol二氧化碳气体的体积,那么储液瓶中应盛放________________________溶液。
(7)在“镁带中镁的质量分数测定装置”中,导管a的作用是______________________。
(8)“镁带中镁的质量分数测定”中,读取量气管的读数时,要使装置内外压强保持一致,具体操作为_________________________________________________________。
(9)在“镁带中镁的质量分数测定”中,如果实验的测定结果偏高,可能的原因是____________(选填编号)。
a.装置漏气 b.未冷却至室温即读数
c.镁带中含有氧化镁 d.末读数时量气管的液面低于水准管
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】纳米TiO2是一种重要的光催化剂。以钛酸酯Ti(OR)4为原料制备纳米TiO2的步骤如下:
①组装装置如图所示,保持温度约为65℃,先将30mL钛酸四丁酯[Ti(OC4H9)4]加入盛有无水乙醇的三颈烧瓶,再加入3mL乙酰丙酮,充分搅拌;
②将含水20%的乙醇溶液缓慢滴入三颈烧瓶中,得到二氧化钛溶胶;
③将二氧化钛溶胶干燥得到二氧化钛凝胶,灼烧凝胶得到纳米TiO2。
已知:钛酸四丁酯能溶于除酮类物质以外的大部分有机溶剂,遇水剧烈水解;Ti(OH)4不稳定,易脱水生成TiO2。回答下列问题:
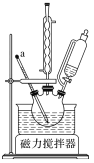
(1)仪器a的名称是__,冷凝管的作用是__。
(2)加入的乙酰丙酮可以减慢水解反应的速率,其原理可能是__(填字母)。
A.增加反应的焓变
B.增大反应的活化能
C.减小反应的焓变
D.降低反应的活化能
制备过程中,减慢水解反应速率的措施还有_。
(3)步骤②中制备二氧化钛溶胶的化学方程式为__。如图所示实验装置中,可用于灼烧二氧化钛凝胶的是__(填字母)。

(4)测定样品中TiO2纯度的方法是:精确称取0.2000g样品放入锥形瓶中,加入硫酸和硫酸铵的混合溶液,加强热使其溶解。冷却后,加入一定量稀盐酸得到含TiO2+的溶液。加入金属铝,将TiO2+全部转化为Ti3+。待过量的金属铝完全溶解并冷却后,加入指示剂,用0.1000mol·L-1NH4Fe(SO4)2溶液滴定至终点。重复操作2次,消耗0.1000mol·L-1NH4Fe(SO4)2溶液的平均值为20.00mL(已知:Ti3++Fe3++H2O=TiO2++Fe2++2H+)。
①加入金属铝的作用除了还原TiO2+外,另一个作用是__。
②滴定时所用的指示剂为__(填字母)。
a.酚酞溶液 b.KSCN溶液 c.KMnO4溶液 d.淀粉溶液
③样品中TiO2的质量分数为__%。(Ti相对分子质量为48)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的产物中一定不存在同分异构体的是( )
A.CH2=CHCH3 与HBrB.![]() 与NaOH 乙醇溶液共热
与NaOH 乙醇溶液共热
C.1,3-丁二烯与溴以 1:1 反应D.![]() 与NaHCO3 溶液
与NaHCO3 溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一份NaOH溶液在空气中放置较长时间后,与另一份新配制相同浓度的氢氧化钠溶液分别滴定相同体积、相同浓度的盐酸,能正确反映滴定过程中溶液pH变化曲线的是(虚线表示放置较长时间后的NaOH溶液,实线表示新配制的NaOH溶液)( )
A.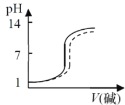 B.
B.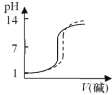 C.
C.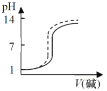 D.
D.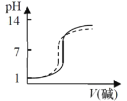
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用已知浓度的酸滴定未知浓度的碱时,会导致待测碱液的浓度偏低的操作是
①酸式滴定管用蒸馏水洗后,未用标准液润洗
②碱式滴定管用蒸馏水洗后,未用待测液润洗
③配制碱液时,称量的固体吸潮
④滴定前酸式滴定管尖嘴部分未充满溶液
⑤滴定中不慎将锥形瓶内液体摇出少量于瓶外
A.①③④B.②⑤C.②③⑤D.①③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关叙述卟啉配合物叶绿素的说法不正确的是( )
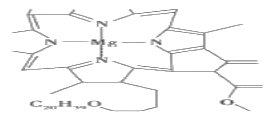
A.该配合物的配位数为4
B.该化合物所包含元素的非金属性:O>N>C>H>Mg
C.Mg单质晶体结构符合A3型最密堆积
D.化合物中C元素的杂化方式sp2、sp3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列操作中不能使指定物质或粒子的浓度增大的是( )
A.向AgCl悬浊液中加入少量Na2S固体,使溶液中Cl-浓度增大
B.向新制氯水中加入少量大理石,使HClO浓度增大
C.压缩平衡体系2NO2![]() N2O4的体积,使NO2浓度增大
N2O4的体积,使NO2浓度增大
D.向Fe(NO3)2溶液中,加入少量盐酸抑制Fe2+的水解,使Fe2+浓度增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com