
��13�֣�
��1��25��ʱ��0.1 mol/L��HA��Һ��c(H+)/c(OH-)��1010����ش��������⣺
��HA�� (�ǿ����ʡ���������ʡ�)��
���ڼ�ˮϡ��HA��Һ�Ĺ����У�����ˮ�������Ӷ�������� (����ĸ)��
A��c(H+)/c(HA) B��c(HA)/(A-) C��c(H��)��c(OH��)�ij˻� D��c(OH��)
��2����֪����CH4(g)��H2O(g)��CO(g)��3H2(g) ��H��+206.2kJ��mol��1
��CH4(g)��CO2(g)��2CO(g)��2H2(g) ��H��-247.4 kJ��mol��1
CH4(g)��H2O(g)��Ӧ����CO2(g)��H2(g)���Ȼ�ѧ����ʽΪ ��
��3����ͼ�����ü���ȼ�ϵ�ص��50 mL 2 mol/L���Ȼ�ͭ��Һ��װ��ʾ��ͼ��
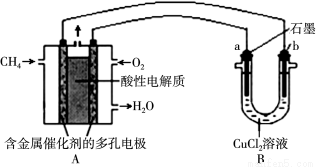
��ش�
�� ����ȼ�ϵ�صĸ�����ӦʽΪ ��
�� ����·����0.6mol����ͨ��ʱ��B���������������Ϊ g��
��1����������� ��A��D;
��2��CH4(g)��2H2O(g) ��CO2(g) ��4H2(g) ��H��+659.8 kJ��mol��1;
��3��CH4-8e-+2H2O=CO2+8H+�� 10.3��
��������
�����������1��25��ʱ��0.1 mol/L��HA��Һ��c(H+)/c(OH-)��1010��c(H+)��c(OH-)��101-14����c (H+)=0.01mol/L<c(HA)�����Ԣ�HA��������ʣ�������Һ�д��ڵ���ƽ�⣺HA H++A-���ڼ�ˮϡ��HA��Һ�Ĺ����У�����ˮ��������c(H+)��c(HA)����С������ƽ�������ƶ�������c(H+)��С�ı���С��c(HA)��С�ı��������c(H+)/c(HA)����,ѡ��A��ȷ�� c(HA)��С�ı������� c(A-)��С�ı��������c(HA)/(A-)��С��������ϡ�͵Ĺ����У�c(H+)��С��������ˮ��Һ�д���ˮ�ĵ���ƽ�⣬�����¶Ȳ��䣬����c(H��)��c(OH��)�ij˻����䣬�Ǹ�������ѡ��C����������ˮ�д���ˮ�ĵ���ƽ�⣬c(H��)��c(OH��)=Kw, c(H+)��С,��c(OH��)����ѡ��D��ȷ����1���١�1���ڣ������ɵ�CH4(g)��2H2O(g)��CO2(g)��4H2(g) ��H��+659.8 kJ/ mol����3���� �ڼ���ȼ�ϵ����ͨ��ȼ�ϼ���ĵ缫Ϊ��������Ϊ�����Ե���ʣ������ڵ�صĸ�����ӦʽΪCH4-8e-+2H2O=CO2+8H+���� ��B�����ȷ�����Ӧ��CuCl2
H++A-���ڼ�ˮϡ��HA��Һ�Ĺ����У�����ˮ��������c(H+)��c(HA)����С������ƽ�������ƶ�������c(H+)��С�ı���С��c(HA)��С�ı��������c(H+)/c(HA)����,ѡ��A��ȷ�� c(HA)��С�ı������� c(A-)��С�ı��������c(HA)/(A-)��С��������ϡ�͵Ĺ����У�c(H+)��С��������ˮ��Һ�д���ˮ�ĵ���ƽ�⣬�����¶Ȳ��䣬����c(H��)��c(OH��)�ij˻����䣬�Ǹ�������ѡ��C����������ˮ�д���ˮ�ĵ���ƽ�⣬c(H��)��c(OH��)=Kw, c(H+)��С,��c(OH��)����ѡ��D��ȷ����1���١�1���ڣ������ɵ�CH4(g)��2H2O(g)��CO2(g)��4H2(g) ��H��+659.8 kJ/ mol����3���� �ڼ���ȼ�ϵ����ͨ��ȼ�ϼ���ĵ缫Ϊ��������Ϊ�����Ե���ʣ������ڵ�صĸ�����ӦʽΪCH4-8e-+2H2O=CO2+8H+���� ��B�����ȷ�����Ӧ��CuCl2 Cu+ Cl2����n(CuCl2)= 0.050 L ��2 mol/L=0.1mol,�������ʵ����ȫʱ������ת��0.2mol,��������������0.1mol,����������ˮ����ⷽ��ʽ�ǣ�2H2O
Cu+ Cl2����n(CuCl2)= 0.050 L ��2 mol/L=0.1mol,�������ʵ����ȫʱ������ת��0.2mol,��������������0.1mol,����������ˮ����ⷽ��ʽ�ǣ�2H2O O2��+ 2H2��,�����������պϻ�·�е���ת����Ŀ��ȣ�����·����0.6mol����ͨ��ʱ�����ˮת�Ƶ��ӵ����ʵ�����0.4mol����ʱ�������������ʵ�����0.1mol��������B���������������Ϊ0.1mol��71g/mol+0.1mol��32g/mol=10.3g��
O2��+ 2H2��,�����������պϻ�·�е���ת����Ŀ��ȣ�����·����0.6mol����ͨ��ʱ�����ˮת�Ƶ��ӵ����ʵ�����0.4mol����ʱ�������������ʵ�����0.1mol��������B���������������Ϊ0.1mol��71g/mol+0.1mol��32g/mol=10.3g��
���㣺�������ʵ�ǿ�����жϡ�����ϡ����������Ũ�ȵı仯���Ȼ�ѧ����ʽ����д��ԭ��غ͵��صķ�Ӧԭ����Ӧ�õ�֪ʶ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���Ĵ�ʡ��һ10���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��FeO��Fe2O3��Fe3O4��ɵĻ������������Ԫ�غ���Ԫ�ص�������Ϊ21/8�������ֻ������FeO ��Fe2O3��Fe3O4�����ʵ���֮�ȿ���Ϊ
A��1��2��1 B��2��1��1 C��1��1��1 D��1��2��3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���Ĵ��ɶ�����Э����ѧ�߶�10�½��Կ��Ի�ѧ�Ծ��������棩 ���ͣ������
��12�֣����ɽ��������������е�Ӧ��ʮ�ֹ㷺��
��CrԪ���γɵ��Ȼ�����(CrO2Cl2)����Ҫ��;�����л��ϳ��п������������Ȼ��������������л��ﷴӦ��
��Cu���γɶ�����������������Ϣ�ش����⣺
��1����ʢ������ͭˮ��Һ���Թ�����μ��백ˮ�����ȳ�����ɫ�����������μӰ�ˮ����ɫ�����ܽ⣬�õ�����ɫ������Һ����д���Ⱥ��������ӷ���ʽ
��
��
����ɫ��Һ�������ӵ����幹��Ϊ ��
��2����������ɫ����Һ�����Ҵ�����������ɫ�ľ��塣����ɫ����Ļ�ѧʽΪ ��
��3����������ʵ����̣��ж�NH3��H2O��Cu2+����λ������NH3 H2O(�>������=����<��)��
��Ni(CO)6Ϊ��������ṹ�����е���ԭ��λ��������������ģ���λ��CO��������������������������ϡ�
��4��������������CO��λ�廻�� NH3 �õ��µ����������������л�Ϊͬ���칹����� ��(����ĸ��ţ�����һ�顣ͼ�кڵ�ΪNH3��ԲȦΪCO��Ni��ȥ)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���Ĵ��ɶ�����Э����ѧ�߶�10�½��Կ��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
ijԪ�ص�ԭ��������Ӳ��Ų���5s2 5p1,��Ԫ�ػ��仯���ﲻ���ܾ��е�������
A����Ԫ�ص����ǵ��� B����Ԫ�ص�����һ���������������ᷴӦ
C����Ԫ�ص��������ˮ�����Լ��� D����Ԫ�ص�����ϼ۳�+5��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���Ĵ��ɶ�����Э����ѧ�߶�10�½��Կ��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
���б仯��Ҫ������������
A��1s22s22p63s1��1s22s22p6 B��3s23p5��3s23p6
C��2p2x2p1y2p1z��2p1x2p1y2p2z D��2H��H��H
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�꼪��ʡ�������¸��������п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
���б�ʾ��Ӧ��ѧ��Ӧ�����ӷ���ʽ��ȷ����
A��NaHSO4��Һ��Ba(OH)2��Һ��Ӧ�����ԣ�2H++SO42-+Ba2++2OH- =BaSO4��+2H2O
B����FeCl2��Һ��ͨ��������Fe2+ + Cl2 = Fe3+ + 2Cl-
C����Ca(ClO)2��Һ��ͨ�������SO2��C1O- + SO2 + H2O=HClO + HSO3-
D��FeSO4������Һ�м�H2O2��2Fe2++H2O2=2Fe3++2OH-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�꼪��ʡ�������¸��������п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
������װ�ý���ʵ�飬�����ȷ���ܴﵽʵ��Ŀ�ĵ���
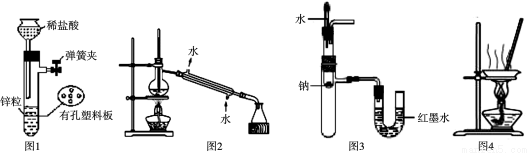
A����ͼ1��ʾװ����ȡ����H2
B����ͼ2��ʾװ�÷���Na2CO3��Һ��CH3COOC2H5�Ļ����
C����ͼ3��ʾװ����֤Na��ˮ��ӦΪ���ȷ�Ӧ
D����ͼ4��ʾװ������NH4Cl������Һ�Ʊ�NH4Cl����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�꼪��ʡ���������ѧУ�߶���ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵����ȷ����
A������������������������ͭ���ɺ�ɫ��������ͭ(Cu2O)
B�����顢�����Ҵ���������һ�������¶��ܷ���ȡ����Ӧ
C����ë����˿�����������Ȼ�߷��Ӳ��ϵ���Ҫ�ɷֶ��ǵ�����
D������ͼ���������Ϊͬ���칹��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�꼪��ʡ�߶���ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ʵ����
��14�֣���50mL0.50mol/L������50mL0.55mol/LNaOH��Һ����ͼ��ʾ��װ���н����кͷ�Ӧ��ͨ���ⶨ��Ӧ���������ų��������ɼ����к��ȡ��ش��������⣺
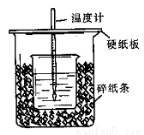
��1����ʵ��װ���Ͽ���ͼ����ȱ�ٵ�һ�ֲ�����Ʒ�� ��
��2���ձ���������ֽ���������� ��
��3�����ձ����粻��Ӳֽ�壬��õ��к�����ֵ (�ƫ��ƫС����Ӱ�족)
��4�������60mL0.50mol/L������50mL0.55mol/LNaOH��Һ���з�Ӧ��������ʵ����ȣ����ų������� (���ȡ�����ȡ�)�������к��� (���ȡ�����ȡ�)����������
��5������ͬŨ�Ⱥ�����İ�ˮ��NH3��H2O������NaOH��Һ��������ʵ�飬��õ��к��ȵ���ֵ�� �����ƫ����ƫС��������Ӱ�족����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com