
����Ŀ���ں�����ߺ�DZˮͧ�п��ù���������Ϊ����������ѡ���ʵ��Ļ�ѧ�Լ���ʵ����Ʒ������ͼ�е�ʵ��װ�ý���ʵ�飬֤���������ƿ�����������

��1��A����ȡCO2��װ�ã�д��A�з�����Ӧ�Ļ�ѧ����ʽ___________________��
��2����д���пո�
���� | �����Լ� | ������Լ���Ŀ�� |
B | ����NaHCO3��Һ | ��ȥ������̼�е��Ȼ��� |
C | ____________ | ____________ |
D | NaOH��Һ | ____________ |
��3��д��C�з�����Ӧ�Ļ�ѧ����ʽ��___________________��
��4���Թ�F���ռ����������һ��ʵ������ǰ�E�еĵ����Ƴ�ˮ�棬�رշ�Һ©����������Ĵָ��ס�Թܿڣ�ȡ���Թܣ�������_____________________����֤���Թ����ռ���������������
���𰸡�CaCO3+2HCl=CaCl2+H2O+CO2�� �������ƹ��� �������̼��Ӧ ���ն�����̼���� 2Na2O2+2CO2=2Na2CO3+O2 �����ǵ�ľ���쵽�Թ�F�ڣ����ľ����ȼ
��������
��1��ʵ������̼��ƺ����ᷴӦ��ȡ������̼����Ӧ����ʽΪ��CaCO3+2HCl=CaCl2+H2O+CO2����
��2���������ƺͶ�����̼��Ӧ����̼���ƺ�����������U�ι���ʢ�ŵ��ǹ������ƹ��壬Ŀ�����������̼��Ӧ��D������������Һ���������ն���Ķ�����̼���Եõ��ϴ������������ʴ�Ϊ��
C | �������ƹ��� | �������̼��Ӧ |
D | NaOH��Һ | ���ն�����̼���� |
��3���������ƺͶ�����̼��Ӧ����̼���ƺ���������Ӧ����ʽΪ��2Na2O2+2CO2=2Na2CO3+O2 ��
��4���Թ�F���ռ����������һ��ʵ������ǣ��Ѵ����ǵ�ľ���쵽�Թ�F�ڣ����ľ����ȼ��˵�����������������̼��Ӧ����������������������


 ͬ��������ϰϵ�д�
ͬ��������ϰϵ�д� �ο�ͨ�γ̱�˼ά����������ѵ��ϵ�д�
�ο�ͨ�γ̱�˼ά����������ѵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼװ���У��������ڳ���0.1 mol NO���塣�������װ��һ����Na2O2����A������ͨ��CO2���塣�����£��������л���������D�������ƶ���������C��ʱ�������������С��Ϊԭ���9/10������������ʵ�����������2.24 g������CO2�ļ���ͨ�룬�������������ƶ�������˵������ȷ����

A. ������D���ƶ���C���Ĺ����У�ͨ���CO2����Ϊ2.24 L(��״��)
B. NO2ת��ΪN2O4��ת����Ϊ20%
C. ��������NO�ѷ�Ӧ��
D. ��������C������ͨ��a mol CO2����ʱ����ǡ�û���D������aС��0.01
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڳ����£���0.1000 mol/L������ζ�25 mL 0.1000 mol/L Na2CO3��Һ�����õζ���������ͼ��ʾ�������йصζ���������Һ�����Ũ�ȼ�Ĺ�ϵ����ȷ����
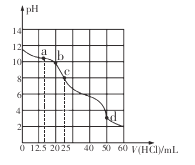
A. a�㣺c( HCO3-)>c(Cl-)>c(C032-)
B. b�㣺c(Na+)+c(H+)=c(Clһ)+c(HCO3-)+c��CO32-��+c��OH-��
C. c�㣺c(OH-)+c(CO32-)=c(H+)+c(H2CO3)
D. d�㣺c��Cl-��=c(Na+)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڰ���ӵ�����(NA)��˵���д������(����)
A. �����ʵ�����CH4��H2O���������������Ϊ10NA
B. 12��NaHSO4��MgSO4�Ĺ��������к���������Ϊ0.1NA
C. ��Ӧ2NH4ClO4![]() N2��+Cl2��+2O2��+4H2O��ÿ����1molO2ת�Ƶ�����Ϊ7NA
N2��+Cl2��+2O2��+4H2O��ÿ����1molO2ת�Ƶ�����Ϊ7NA
D. 100g��������Ϊ46%C2H5OH��Һ�У�����ԭ����Ϊ12NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ȤС����������װ�ã�������������ص�ʵ�顣
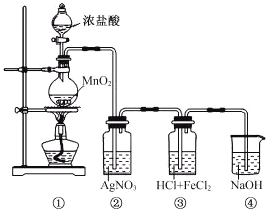
(1)װ�â���NaOH��Һ��������___________��
(2)ʵ�������ȡװ�â��е���Һ��������Ũ������ȴ�ᾧ�����ˡ�ϴ�ӡ�����õ�FeCl3��6H2O���塣������Ũ�������У�����Ҫ��������___________��
A�������� B��©�� C�������� D���ƾ���
(3)װ�â��г��ְ�ɫ�������ݴ������ܷ��Ʋ�װ�â�������Cl2___________________����˵������_______________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������йط�Ӧ�ͷ�Ӧ���Ͳ��������
A. ����Ũ���ᡢŨ�����ϼ�����ȡ������(ȡ����Ӧ)
B. ��һ�������£����������������Ȼ�����(�ӳɷ�Ӧ)
C. ����Ȳ(![]() )��ȡ����ϩ(CH2=CHCl) (������Ӧ)
)��ȡ����ϩ(CH2=CHCl) (������Ӧ)
D. �ڴ���������������ϩ��ȡ������(�ӳɷ�Ӧ)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ�����ӵ�������ֵ������������ȷ���ǣ� ��
A. ����£�224 L H2O���еķ�����Ϊ10NA
B. 1 mol�κ�����������ԭ������ΪNA
C. 28 g CO�����ķ�����ΪNA
D. ����£�NA�����ӵ����Ϊ22.4 L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£� 0.1 mol/L��ij��Ԫ�� H2A ��Һ�У����ܴ��ڵ����к� A ���ӵ����ʵ���������pH �仯�Ĺ�ϵ��ͼ��ʾ������˵����ȷ����

A. H2A �ĵ��뷽��ʽ��H2A![]() H+ + HA��
H+ + HA��
B. pH = 5 ʱ����NaHA��Na2A�Ļ����Һ�У� c��HA���� : c��A2����= 1 : 100
C. �����ʵ���Ũ�ȵ�NaHA��Na2A��Һ�������ϣ�����Ũ�ȴ�С��ϵΪ��c��Na+����c��HA������c��A2����
D. NaHA��Һ�Լ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��Ӧ��10AgF��5Cl2��5H2O��9AgCl��AgClO3��10HF��O2���Իش�
��1����Ӧ���������ͻ�ԭ�������ʵ���֮����_____��
��2����ת��1 mol����ʱ����������Cl2�����ʵ�����___��
��3��ÿ����1 mol O2ʱ������Ԫ�ػ�ԭ��Cl2�����ʵ�����_____��
��4����Ӧ���ĵ�ˮ����_____��
A.ȫ�������� B.ȫ������ԭ C.![]() ������ D.
������ D.![]() ����ԭ
����ԭ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com