
【题目】下表为元素周期表的一部分。
碳 | 氮 | Y | |
X | 硫 | Z |
回答下列问题:
(1)Z元素在周期表中的位置为__________________。
(2)表中Y,硫和Z三种元素的简单离子半径由大到小的顺序是(填离子符号)____________。
(3)下列事实能说明Y元素的非金属性比S元素的非金属性强的是__________;
a.Y单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1mol Y单质比1mol S得电子多
c.Y和S两元素的简单氢化物受热分解,前者的分解温度高
(4)碳与镁形成的1mol化合物Q与水反应,生成2mol Mg(OH)2和1mol气态烃。该烃分子中碳氢质量比为9∶1,烃的电子式为__________________,Q与水反应的化学方程式为__________________________。
【答案】 第三周期第ⅦA族 S2->Cl->O2- ac 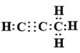 Mg2C3+4H2O=2Mg(OH)2+C3H4↑
Mg2C3+4H2O=2Mg(OH)2+C3H4↑
【解析】根据元素在周期表中的位置可判断X是S,Y是O,Z是Cl,则
(1)Cl元素在周期表中的位置为第三周期第ⅦA族。(2)离子的核外电子层数越多,离子半径越大,核外电子排布相同时离子半径随原子序数的增大而减小,则表中Y,硫和Z三种元素的简单离子半径由大到小的顺序是S2->Cl->O2-。(3)a.Y单质与H2S溶液反应,溶液变浑浊,说明置换出单质S,因此可以说明氧元素非金属性强于硫,a正确;b.非金属性强弱与得电子多少没有关系,只与难易程度有关系,b错误;c.Y和S两元素的简单氢化物受热分解,前者的分解温度高,说明氢化物稳定性强,因此可以说明氧元素非金属性强于硫,c正确;答案选ac;(4)该烃分子中碳氢质量比为9∶1,则原子个数之比是9/12:1=3:4,由于Q是Mg2C3,所以根据原子守恒可知烃的分子式为C3H4,电子式为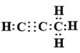 ,Q与水反应的化学方程式为Mg2C3+4H2O=2Mg(OH)2+C3H4↑。
,Q与水反应的化学方程式为Mg2C3+4H2O=2Mg(OH)2+C3H4↑。


科目:高中化学 来源: 题型:
【题目】已知分解1mol H2O2放出热量98kJ。在含有少量I![]() 的溶液中,H2O2分解的机理为: H2O2+I-
的溶液中,H2O2分解的机理为: H2O2+I-![]() H2O+IO- 慢 ; H2O2+IO-
H2O+IO- 慢 ; H2O2+IO-![]() H2O+O2+I- 快
H2O+O2+I- 快
下列有关该反应的说法正确的是( )
A. 反应速率与I![]() 浓度有关 B. IO
浓度有关 B. IO![]() 也是该反应的催化剂
也是该反应的催化剂
C. H2O2分解生成1mol O2释放的热量为98kJ D. ν(H2O2)=ν(H2O)=ν(O2)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 0.1mol/LpH为4的NaHB溶液中:c (HB-)>c(H2B)>c(B2-)
B. 如图表示25℃时,用0.1mol·L-1盐酸滴定20mL0.1mol·L-1NaOH溶液时,溶液的pH随加入酸体积的变化

C. 在pH=2的NaHSO4溶液中c(H+)=c(OH-)+ c(SO42-)
D. pH=2的两种一元酸x和y,体积均为100 mL,稀释过程中pH与溶液体积的关系如图所示,分别滴加NaOH溶液(c=0.1mol·L-1)至pH=3,消耗NaOH溶液的体积为Vx、Vy,则x为强酸,y为弱酸且Vx>Vy

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室需纯净的NaCl晶体,但现有的NaCL晶体中混有少量的Na2SO4和NH4HCO3 , 为除去杂质,甲同学设计了如下实验:(已知NH4HCO3 ![]() NH3+H2O+CO2 )
NH3+H2O+CO2 ) 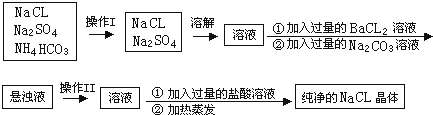
(1)上述操作I、II的名称分别为、 .
(2)进行操作“加入过量的BaCL2溶液”时,如何判断BaCL2溶液已过量,其方法是 .
(3)操作“加入过量的Na2CO3溶液”的目的是 .
(4)操作“加入过量的盐酸溶液”的目的是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A. 1 mol CO2的质量为44g·mol-1
B. CO2的摩尔质量为44g
C. 6.02×1022个CO2分子的质量为4.4g
D. 1mol任何物质的质量等于该物质的相对分子质量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.我国流通的硬币材质是金属单质
B.所有的不锈钢都只含有金属元素
C.黄铜的熔点高于金属铜,故应用广泛
D.镁合金的硬度和机械强度均高于纯镁
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将5mol/L的Mg(NO3)2溶液a mL稀释至b mL,稀释后溶液中NO3﹣的物质的量浓度为( )
A.5a/b mol/L
B.10a/b mol/L
C.b/5a mol/L
D.a/b mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为除去粗盐中的Ca2+、Mg2+、SO42﹣以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量): 称取粗盐 ![]()
![]()
![]()
![]()
![]() 滤液
滤液 ![]()
![]() 精盐
精盐
(1)第①步中,操作A是 , 第⑤步中,操作B是 .
(2)第④步中,写出相应的化学方程式(设粗盐溶液中Ca2+的主要存在形式为CaCl2) .
(3)若先加入盐酸再过滤,将对实验结果产生影响,其原因是 .
(4)判断Na2CO3已过量的方法是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com