
【题目】下列叙述正确的是
A. 1 mol CO2的质量为44g·mol-1
B. CO2的摩尔质量为44g
C. 6.02×1022个CO2分子的质量为4.4g
D. 1mol任何物质的质量等于该物质的相对分子质量
科目:高中化学 来源: 题型:
【题目】同体积同物质的量浓度的AgNO3溶液中分别加入同体积的NaCl、MgCl2、AlCl3溶液,恰好使Cl-完全转化为沉淀,则三种溶液的物质的量浓度之比为
A. 1:1:1 B. 1:2:3 C. 1:4:9 D. 6:3:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2L密闭容器中进行反应:mX(g)+nY(g)![]() pZ(g)+qQ(g),式中m、n、p、q为化学计量数。在0~3min内,各物质物质的量的变化如下表所示:
pZ(g)+qQ(g),式中m、n、p、q为化学计量数。在0~3min内,各物质物质的量的变化如下表所示:
物质 | X | Y | Z | Q |
起始/mol | 0.7 | 1 | ||
2min末/mol | 0.8 | 2.7 | 0.8 | 2.7 |
3min末/mol | 0.8 |
已知:2min内,ν(Q)=0.075mol·L-1·min-1,ν(Z)∶ν(Y)=1∶2。
(1)方程式中m=______,n=______,p=______,q=______。
(2)2.5min内,Q的转化率为______________。
(3)对于该反应,能增大正反应速率的措施是___________
A.增大容器体积 B.移走部分Q C.通入大量X D.升高温度
(4)该反应达到化学平衡状态时___________
A.容器内气体压强保持不变 B.容器内气体密度保持不变
C.容器内气体平均摩尔质量保持不变 D.正反应速率与逆反应速率相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分。
碳 | 氮 | Y | |
X | 硫 | Z |
回答下列问题:
(1)Z元素在周期表中的位置为__________________。
(2)表中Y,硫和Z三种元素的简单离子半径由大到小的顺序是(填离子符号)____________。
(3)下列事实能说明Y元素的非金属性比S元素的非金属性强的是__________;
a.Y单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1mol Y单质比1mol S得电子多
c.Y和S两元素的简单氢化物受热分解,前者的分解温度高
(4)碳与镁形成的1mol化合物Q与水反应,生成2mol Mg(OH)2和1mol气态烃。该烃分子中碳氢质量比为9∶1,烃的电子式为__________________,Q与水反应的化学方程式为__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组按如下实验流程探究海带中碘的制取。
步骤(一)

步骤(二)

已知:①3I2+6NaOH=5NaI+NaIO3+3H2O;②常温下,碘单质微溶于水,易溶于CCl4。
请回答:
(1)步骤(一)中的仪器名称:仪器A______________, 仪器 B_______________。
(2)①分液漏斗使用前须检漏,检漏方法为__________________________。
②步骤X中,萃取后分液漏斗内观察到的现象是_______________________。
③下列有关步骤Y的说法,正确的是_______________。
A.应控制NaOH溶液的浓度和体积 B.将碘转化成离子进入水层
C.主要是除去海带浸取原液中的有机杂质 D.NaOH溶液可以由乙醇代替
④步骤(二)中操作Z的名称是_____________。
(3)方案甲中采用蒸馏不合理,理由是_____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】使相同体积的NaCl、CaCl2、AlCl3溶液中的Cl﹣全部沉淀,用去同浓度的AgNO3溶液的体积分别为3V、2V、V,则NaCl、CaCl2、AlCl3溶液的物质的量浓度之比为( )
A.6:3:2
B.3:2:1
C.9:3:1
D.1:2:3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CH4、NH3、H2O、H2S、NH4NO3和ZnS是中学化学常见的六种化合物。回答下列问题:
(1)基态S原子有__________种不同能量的电子,与Zn同属ds区且同周期的元素基态原子核外电子排布式为____________________。
(2)H2O和H2S中,沸点较高的是__________,原因是___________________________________。
(3)CH4、NH3和H2O3种氢化物中,键角由大到小的顺序为_______________,其中NH3的VESEPR模型名称为____________。
(4)NO3-离子的几何构型为__________,NO3-离子的电子体有_____________(任写一种)。
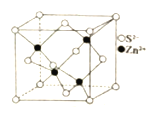
(5)ZnS晶体结构有多种,其中一种晶体的晶胞结构如图所示,晶体中与S2-等距离且最近的S2-有_____个。已知该晶体的晶胞参数为anm,其密度为 ρg·cm-3,则阿伏加德罗常数的数值为____________________________(用含字母a、ρ的表达式表示,列出计算式即可)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com