
【题目】目前世界上用量最大,用途最广的合金是( )
A.铝合金
B.青铜
C.钢铁
D.塑钢
科目:高中化学 来源: 题型:
【题目】利用酸解法制钛白粉产生的废液[含有大量FeSO4、H2SO4和少量Fe2(SO4)3、TiOSO4],生产铁红和补血剂乳酸亚铁。其生产步骤如下:

已知:TiOSO4可溶于水,在水中可以电离为TiO2+和SO42-,TiOSO4水解成TiO2xH2O沉淀为可逆反应;乳酸结构简式为CH3CH(OH)COOH。
请回答:
(1)步骤①中分离硫酸亚铁溶液和滤渣的操作是________________________。
(2)加入铁屑的目的一是还原少量Fe2(SO4)3;二是使少量TiOSO4转化为TiO2xH2O滤渣,用平衡移动的原理解释得到滤渣的原因___________________________。
(3)硫酸亚铁在空气中煅烧生成铁红和三氧化硫,该反应中氧化剂和还原剂的物质的量之比为____________________________。
(4)用离子方程式解释步骤⑤中加乳酸能得到乳酸亚铁的原因_________________。
(5)步骤④的离子方程式是_________________________________________。
(6)步骤⑥必须控制一定的真空度,原因是有利于蒸发水以及___________________。
(7)为测定步骤②中所得晶体中FeSO4·7H2O的质量分数,取晶体样品a g,溶于稀硫酸配成100.00 mL溶液,取出20.00 mL溶液,用KMnO4溶液滴定(杂质与KMnO4不反应)。若消耗0.1000 molL-1 KMnO4溶液20.00 mL,所得晶体中FeSO4·7H2O的质量分数为______(用a表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】V mLAl2(SO4)3溶液中含有Al3+ a g,取![]() V mL溶液稀释到4V mL,则稀释后溶液中S042-的物质的量浓度是
V mL溶液稀释到4V mL,则稀释后溶液中S042-的物质的量浓度是
A. ![]() mol/L B.
mol/L B. ![]() mol/L
mol/L
C. ![]() mol/L D.
mol/L D. ![]() mol/L
mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表中实线是元素周期表的部分边界,其中上边界并未用实线标出。

根据信息回答下列问题。
(1)周期表中基态Ga原子的最外层电子排布式______________。
(2)Fe元素位于周期表的________区;Fe与CO易形成配合物Fe(CO)5,原子数目和价电子总数相同的微粒互为等电子体,等电子体具有相似的结构特征,与CO分子互为等电子体的分子和离子分别为________和________(填化学式)。
(3)在CH4和C2H2中,碳原子采取sp3杂化的分子是_________________。
(4)根据VSEPR理论预测ED4-离子的空间构型为________。
(5)B、C、D、E原子相互形成的常见化合物分子中,所有原子都满足最外层8电子稳定结构的分子的电子式为______________________(任写1种)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)1个NH4+离子含有________个质子,________个电子。
(2)2molH3PO4含有___________个分子,_________mol O,_________个原子。
(3)含有6.02×1023个H的CH4的物质的量为________mol。
(4)含有相同氧原子数的CO、CO2、O3的物质的量之比为______________。
(5)相同物质的量的SO2和SO3,分子数之比为_________;原子数之比为_________;电子数之比为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】易混易错题组
有机物的命名与结构式结构简式的书写
Ⅰ、官能团能体现有机物的特殊性质,认识下列有机物的官能团。
(1)![]() 的物质类别是_______________
的物质类别是_______________
(2)![]() 中的官能团名称是_______________
中的官能团名称是_______________
(3) 非诺洛芬 中的官能团的结构简式是__________
中的官能团的结构简式是__________
Ⅱ、给下列有机物命名或写出其结构简式:
(1) ______________________________________
______________________________________
(2) _______________________________
_______________________________
(3) ______________________________________
______________________________________
(4)2甲基4乙基庚烷______________________________________________
(5)2,4,6三硝基甲苯___________________________________________
(6)C4H9Cl的核磁共振氢谱表明其只有一种化学环境的氢,则A的化学名称为_________________。
(7)![]() _____________________________
_____________________________
III.写出下列化学方程式
(1)2-丁烯与溴水____________________________________
(2)CaC2→乙炔_____________________________________
(3)苯的溴代________________________________________
(4)2-溴丙烷的消去反应_________________________________
(5)苯乙烯加聚_________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质发生状态变化所克服的粒子间作用力属于同种类型的是
A.HCl和蔗糖溶于水B.水晶和干冰熔化
C.硫单质的升华与H2S的分解D.NaF和氧化钠分别受热熔化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢能是一种极具发展潜力的清洁能源。
(1)氢气的制取与储存是氢能源利用领域的研究热点.
已知:①CH4的燃烧热为890KJ·mol-1; ②H2的热值为50.2kJ·g-1
则甲烷部分氧化生成CO2和H2的热化学方程式为___________________________________;该反应自发进行的条件是___________。
(2)Bodensteins研究了如下反应:2HI(g)![]() H2(g)+I2(g)△H=+11kJ/mol在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如下表:
H2(g)+I2(g)△H=+11kJ/mol在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如下表:
t/min | 0 | 20 | 40 | 60 | 80 | 120 |
X(HI) | 1.00 | 0.910 | 0.850 | 0.815 | 0.795 | 0.784 |
X(HI) | 0.00 | 0.600 | 0.730 | 0.773 | 0.780 | 0.784 |
①根据上述实验结果,该反应的平衡常数K的计算式为:___________。
②上述反应中,正反应速率为v正=k正x2(HI),逆反应速率为v逆=k逆x(H2)x(I2),其中k正、k逆为速率常数,若k正=9.00min-1,在t=20min时,v逆=__________min-1(保留三位有效数字)
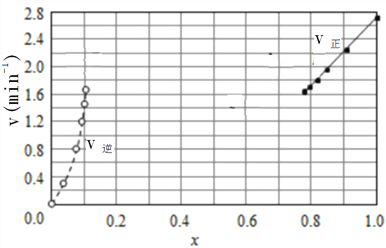
③由上述实验数据计算得到v正~x(HI)和v逆~x(H2)的关系可用下图表示。在上述平衡基础上,缓慢升高到某一温度,反应重新达到平衡,请在下图中画出此过程的趋势图。______________
(3)一种可超快充电的新型铝电池,充放电时AlCl4-和Al2Cl7-两种离子在Al电极上相互转化,其它离子不参与电极反应,放电时负极Al的电极反应式为______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在水玻璃中通入少量的CO2气体,充分反应后加热蒸干,再高温充分灼烧,冷却后所得的固体物质为()
A. Na2SiO3 B. Na2SiO3与Na2CO3
C. SiO2与Na2CO3 D. SiO2、Na2SiO3及Na2CO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com