
【题目】下表中实线是元素周期表的部分边界,其中上边界并未用实线标出。

根据信息回答下列问题。
(1)周期表中基态Ga原子的最外层电子排布式______________。
(2)Fe元素位于周期表的________区;Fe与CO易形成配合物Fe(CO)5,原子数目和价电子总数相同的微粒互为等电子体,等电子体具有相似的结构特征,与CO分子互为等电子体的分子和离子分别为________和________(填化学式)。
(3)在CH4和C2H2中,碳原子采取sp3杂化的分子是_________________。
(4)根据VSEPR理论预测ED4-离子的空间构型为________。
(5)B、C、D、E原子相互形成的常见化合物分子中,所有原子都满足最外层8电子稳定结构的分子的电子式为______________________(任写1种)。
【答案】 4S24P1 d N2 NO+(C22- 或 CN- 等其它合理答案也可以) CH4 正四面体形 ![]() (
( 等其它合理答案也可以)
等其它合理答案也可以)
【解析】(1)31号元素Ga原子基态的最外层电子排布式为4s24p1。(2)26号元素Fe元素在周期表的位于第四周期第Ⅷ族,位于周期表的d区。Fe与CO易形成配合物Fe(CO)5,在Fe(CO)5中铁的化合价为0价。与CO分子互为等电子体的分子是N2,离子为CN-。(3)在CH4、CO2、CH3OH中,碳原子采取sp3杂化的分子有CH4、CH3OH;CO2中的C原子的杂化方式为sp杂化。(4)根据表格中各种元素的相对位置可以看出:A是H;B是C;C是N;D是O;E是Cl。根据VSEPR理论预测ClO4-离子的空间构型为正四面体型。(5)在C、N、O、Cl原子相互化合形成的分子中,所有原子都满足最外层8电子稳定结构的分子有CO2、NCl3、CCl4,其电子式为![]() (
(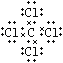 等)。
等)。


 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案科目:高中化学 来源: 题型:
【题目】以铬铁矿为原料![]() 可制备K2Cr2O7和金属铬。实验流程如下:
可制备K2Cr2O7和金属铬。实验流程如下:
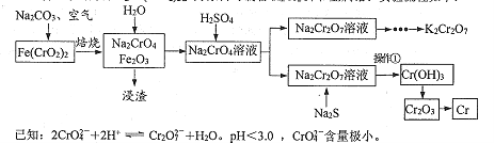
(1)写出铬铁矿焙烧转化为NazCrO4的化学反应方程式:__________________。焙烧时不能使用陶瓷容器的原因是___________________。
(2)加入稀硫酸后所得Na2Cr2O7溶液的pH 应小于3.0,可用 ____测定溶液pH。
(3)操作①包括过滤和洗涤。实验室洗涤沉淀的操作是_________________。
(4) Na2S的作用是调节溶液的酸碱度和__
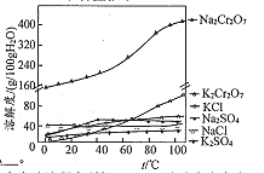
(5)Fe3+在pH为3.7时可完全转化为Fe(OH)3。在上述流程中所得NazCrz07溶液中含有少量Fe3+。请结合上图有关物质的溶解度曲线,设计由Na2Cr2O7液制备K2Cr2O7固体的实验方案(实验中须选用的试剂:硫酸、NaOH溶液、KCl固体、蒸馏水):_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列既是氧化还原反应,又是吸热反应的是
A.灼热的炭与水蒸气的反应B.Ba(OH)2·8H2O与NH4Cl的反应
C.铝片与稀盐酸反应D.甲烷(CH4)在O2中的燃烧反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将20.0 g 14%的NaCl溶液与30.0 g 24%的NaCl溶液混合,混合后得到密度为 1.17 g·cm-3的溶液。请计算:
(1)混合后的溶液中NaCl的质量分数是多少?___________
(2)混合后的溶液的物质的量浓度为多少?_________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质中,所含氧原子的物质的量相同的是( )
A. 0.3molO2和0.3molH2O B. 0.1molH2SO4和3.01×1023个H2O
C. 0.1molMgSO4.7H2O和0.1molC12H22O11 D. 6.02×1023个CO2和0.1molKMnO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室配制 500mL 0.2mol/L 的 NaOH溶液,在下图所示仪器中,配制上述溶液肯定不需要的是____(填序号),除图中已有仪器外, 配制上述溶液还需要的玻璃仪器是____。

具体过程如下:
①计算需要称量 NaOH 固体的质量_____;
②用少量蒸馏水洗涤烧杯内壁 2~3 次,洗涤液也都注入容量瓶,轻轻晃动容量瓶,使溶液混合均匀;
③用托盘天平称量 NaOH 固体;
④将 NaOH 溶液沿玻璃棒注入_____中;
⑤将称好的 NaOH 固体放入烧杯中,用适量蒸馏水溶解,并____________;
⑥盖好瓶塞,反复上下颠倒,摇匀;
⑦将蒸馏水注入容量瓶,液面离刻度线下_____cm 时,改用_______滴加蒸馏水至液面于刻度线相切;
试回答下列问题:
(1)填写上述过程中的空白;
(2)上述过程的正确顺序为___________(填步骤序号);
(3)使用容量瓶前必须进行的一步操作是____________;
(4)经精确测量,最后所得溶液物质的量浓度为 0.192mol/L,原因可能是____________。
A、使用滤纸称量 NaOH 固体;
B、未冷却直接转移至容量瓶,立即配好;
C、容量瓶中原来有少量蒸馏水;
D、称量时所用的砝码生锈;
E、溶解 NaOH 后的烧杯未经多次洗涤;
F、定容时俯视刻度。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与人类的发展密不可分,以下不属于化学对人类贡献的是( )
A.药物和保健品的研制
B.指南针的发明与应用
C.新型高分子化合物的合成
D.合金材料的生产
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com