


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��2 mol A+1 mol B |
| B��6 mol C+2 mol D |
| C��3 mol C+1 mol D |
| D��4 mol A+2 mol B+3 mol C |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Al����NaOH��Һ��Ӧ Al+2OH-=AlO-2+H2�� |
| B����ʾϡ�������������ϡ��Һ���Ȼ�ѧ����ʽ HCl+NaOH=NaCl+H2O����H=-57.3 kJ/mol |
| C��������ˮԭ�������ӷ���ʽ Al3++3H2O=Al��OH��3+3H+ |
| D�������Ũ��Һ����������Ũ��Һ��ϵ����ӷ���ʽNH4++OH-=NH3��+H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����֬�������� |
| B����Ȼ��֬û�й̶����ۡ��е� |
| C���Ǹ�֬����ĸ����� |
| D����֬������ʹ��ˮ��ɫ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��2�� | B��3�� | C��4�� | D��5�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
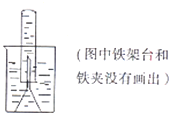 ijͬѧȡһ���������������һЩС�ף�Ȼ��ȡһҩ�������Ʒ�ĩ�����������ã�������ͼ��ʾװ�õ��۵�©���У�
ijͬѧȡһ���������������һЩС�ף�Ȼ��ȡһҩ�������Ʒ�ĩ�����������ã�������ͼ��ʾװ�õ��۵�©���У��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��̼��ȼ����Ϊ110.5 kJ/mol |
| B��1mol̼���ȼ�շų�����������110.5kJ |
| C��Ũ������ϡNaOH��Һ��Ӧ����1 molˮ���ų�������Ϊ57.3 kJ |
| D��ϡ������ϡNaOH��Һ��Ӧ����1 molˮ���ų�������Ϊ57.3 kJ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���٢� | B���٢� | C���ڢ� | D���ۢ� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com