
【题目】工业上用丁烷催化脱氢侧备丁烯:C4H10(g)![]() CH4(g)+H2(g)(正反应吸热)。将丁烷和氢气以一定的配比通过填充有催化剂的反应器(氢气的作用是活化催化剂),反应的平衡转化率、产率与温度、投料比有关。下列判断不正确的是
CH4(g)+H2(g)(正反应吸热)。将丁烷和氢气以一定的配比通过填充有催化剂的反应器(氢气的作用是活化催化剂),反应的平衡转化率、产率与温度、投料比有关。下列判断不正确的是
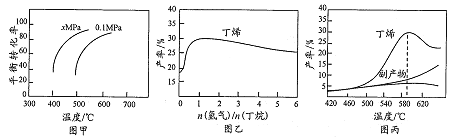
A. 由图甲可知,x小于0.1
B. 由图乙可知,丁烯产率先增大后减小,减小的原因是氢气是产物之一,随着n(氢气)/n(丁烷)增大,逆反应速 率减小
C. 由图丙可知产率在590℃之前随温度升高面增大的原因可能是溫度升高平衡正向移动
D. 由图丙可知,丁烯产率在590℃之后快速降低的主要原因为丁烯高温分解生成副产物
科目:高中化学 来源: 题型:
【题目】溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:按以下合成步骤回答问题:
已知:C6H6(苯)+Br2(溴)→C6H5Br(溴苯)+HBr↑(需要铁粉作催化剂);
液溴、溴化氢均可与氢氧化钠反应;苯、溴苯不与氢氧化钠反应;溴化氢易溶于水。

苯 | 溴 | 溴苯 | |
密度/g·cm-3 | 0.88 | 3.10 | 1.50 |
沸点/℃ | 80 | 59 | 156 |
水中溶解度 | 微溶 | 微溶 | 微溶 |
(1)仪器c的名称_________。
(2)在a中加入15 mL无水苯和少量铁屑。在b中小心加入4.0 mL 液态溴。向a中滴入几滴溴,有白雾产生,是因为生成了__________气体,继续滴加至液溴滴完。装置d的作用是____________________。
(3)液溴滴完后,经过下列步骤分离提纯:
①向a中加入10 mL水,然后过滤除去未反应的铁屑;
②滤液依次用10 mL水、8 mL10%的NaOH溶液、10 mL水洗涤。NaOH溶液洗涤的作用是_____________________,第二次水洗的目的为________________。
③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤。加入氯化钙的目的是______。
(4)经过上述分离操作后,粗溴苯中还含有部分杂质,要进一步提纯,选择的装置为___(填入正确选项前的字母)。

(5)在该实验中,a的容积最适合的是________(填入正确选项前的字母)。
A.25 mL B.50 mL C.250 mL D.500 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. 分子式CF2Cl2、C3H8、C2H4、C2H2均只对应一种化合物
B. 1mol C4HmO完全燃烧,最多消耗O2 6mol
C. 甲苯与氯气在光照下反应主要生成2-氯甲苯或4-氯甲苯
D. 分子式为C10H14,能使酸性KMnO4溶液褪色的一元取代苯共有3种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的数值,下列说法正确的是( )
A. 常温常压下,8 g O2含有4NA个电子
B. 1 L 0.1 mol·L-1的氨水中有0.1NA个NH4+
C. 标准状况下,22.4 L盐酸含有NA个HCl分子
D. 0.05 mol液态KHSO4中含有0.1NA个阳离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】重要的化工原料F(C5H8O4)有特殊的香味,可通过如图所示的流程合成:

已知:①X是石油裂解气主要成分之一,与乙烯互为同系物;
② ;
;
③C、E、F均能与NaHCO3生成气体
(1)D中所含官能团的名称是_______________。
(2)反应②的化学方程式为_____________,反应类型是________;反应⑥的化学方程式为______________。
(3)F的同分异构体很多,其中一种同分异构体只含有一种官能团,在酸性或碱性条件下都能水解生成两种有机物,该同分异构体的结构简式是____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】羟甲香豆素是一种治疗胆结石的药物。合成其的两种中间体及羟甲香豆素的结构如下:
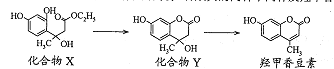
下列有关说法正确的是
A. 化合物X和Y分子各含有1个手性碳原子
B. 化合物Y能发生加成反应、取代反应和消去反应
C. 1mol羟甲香豆素最多可与2molNaOH反应
D. 化合物X和羟甲香豆素分别与溴水反应,最多消耗的Br2的物质的量之比为1:l
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以菱锰矿(主要成分![]() 还含有
还含有![]()
![]() 等杂质)为原料制各二氧化锰的工艺流程如下:
等杂质)为原料制各二氧化锰的工艺流程如下:
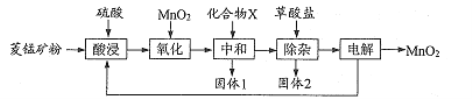
已知草酸钙、草酸镁不溶于水。
(1)写出“氧化”时发生反应的离子方程式:____。
(2)“中和”的目的是将铁、铝元素转化为沉淀除去,化合物X可用 ____(写一种物质的化学式)。
(3)该工艺流程中固体l和固体2均需用水洗涤,目的是________。
(4)“除杂”时,除去的金属离子有___。
(5)“电解”原理如下图所示,阳极的电极反应式为___
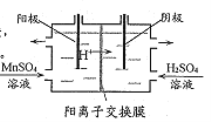
(6)该流程中可以循环使用的物质有 ___ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式不正确的是( )
A. 向CuSO4溶液中加入Na2O2:2 Na2O2+2Cu2++2H2O=4Na++2Cu(OH)2↓+O2↑
B. 离子方程式2Ca2+ + 3HCO3– + 3OH–= 2CaCO3↓ + CO32– + 3H2O可以表示Ca(HCO3)2与NaOH溶液的反应
C. Fe(OH)3溶于HI溶液:Fe(OH)3+3H+=Fe3++3H2O
D. 向NaAlO2溶液中滴入NaHCO3溶液产生白色沉淀:AlO2-+HCO3-+H2O=Al(OH)3↓+CO![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为一些物质之间的转化关系,其中部分反应中反应物或生成物未列全。已知A、I、K均为家庭厨房中的常见物质,其中A是食品调味剂,H是消毒剂的有效成分,I、K可用作食品发泡剂。B是一种有机酸盐,E、F、G均为氧化物,L是红褐色沉淀。
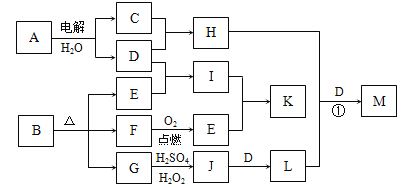
根据以上信息,回答下列问题:
(1)B的组成元素为________________________________。
(2)G→J的离子方程式为_________________________。
(3) M是含氧酸盐,反应①中H、L、D的物质的量之比为3∶2∶4,则M的化学式为_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com