
【题目】用高分子吸附树脂提取卤水中的碘(主要以 I-形式存在)的工艺流程如下,说法不正确的是
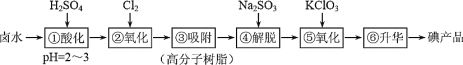
A.流程②的反应说明 I 的非金属性弱于 Cl
B.经①和④所得溶液中,I-的浓度后者大于前者
C.氯元素的相对原子质量是 35.5, 则存在的 35Cl 、37Cl 的丰度比约为 3:1
D.若在流程②和⑤中要得到等量的 I2,则需消耗的 n(Cl2) :n(KClO3) = 5:2
科目:高中化学 来源: 题型:
【题目】硫化钠是重要的化工原料,大多采用无水芒硝(Na2SO4)—炭粉还原法制备,原理为Na2SO4+2C![]() Na2S+2CO2↑。其主要流程如下:
Na2S+2CO2↑。其主要流程如下:

(1) Na2S溶液显碱性,写出相关反应的方程式(主要)______,上述流程中采用稀碱液比用热水更好,理由是___________。
(2)常温下,等体积、等物质的量浓度的NaHS溶液与Na2S溶液混合,混合溶液中c(S2-)_____c(HS-) (填“大于”、“小于”或“等于”)。若混合溶液的pH=10,则c(HS-)+3c(H2S)-c(S2-)= ___________________
(3)已知:I2+2S2O32-=2I-+S4O62-。上述所制得的Na2S·9H2O晶体中含有Na2S2O3·5H2O等杂质。为测定产品的成分,进行下列实验,步骤如下:
a. 取试样10.00 g配成500.00 mL溶液。
b. 取所配溶液25.00 mL于碘量瓶中,加入过量ZnCO3悬浊液除去Na2S后,过滤,向滤液中滴入2~3滴淀粉溶液,用0.050 00 mol·L-1I2溶液滴定至终点,用去5.00mL I2溶液。
c. 再取所配溶液25.00 mL于碘量瓶中,加入50.00 mL 0.050 00 mol·L-1的I2溶液,并滴入2~3滴淀粉溶液,振荡。用标准Na2S2O3溶液滴定多余的I2,用去15.00 mL 0.100 0 mol·L-1 Na2S2O3溶液。
①步骤b中用ZnCO3除去Na2S的离子方程式为________。
②判断步骤c中滴定终点的方法为______________。
③计算试样中Na2S·9H2O和Na2S2O3·5H2O的质量分数_________(写出计算过程)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物的结构可用“键线式”表示,如:CH3CH=CHCH3可简写为![]() ,有机物X的键线式为
,有机物X的键线式为![]() ,下列说法不正确的是( )
,下列说法不正确的是( )
A.X的化学式为C8H10
B.有机物Y是X的同分异构体,且属于芳香烃,则Y的结构简式为![]()
C.X能使酸性高锰酸钾溶液褪色
D.X与足量的H2在一定条件下反应可生成环状的饱和烃Z,Z的一氯代物有2种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】所有超市、商场、集贸市场等商品零售场所实行塑料购物袋有偿使用制度,一律不得免费提供塑料购物袋。在全国范围内禁止生产、销售、使用厚度小于0.025毫米的塑料购物袋(简称超薄塑料购物袋)。下列说法不正确的是( )
A.在所有超市、商场、集贸市场等商品零售场所实行塑料购物袋有偿使用制度,主要目的是控制塑料制品的使用,减少“白色污染”
B. 的单体是苯乙烯
的单体是苯乙烯
C.聚氯乙烯塑料强度大,抗腐蚀性强,可以用来包装需长时间保存的食品
D.用于食品包装的塑料制品,属于热塑性塑料,可回收再利用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,体积为1L的密闭容器中,0.3molX和0.2molY进行反应:2X(g)+Y(s) ![]() Z(g),经10s达到平衡,生成0.1molZ。下列说法正确的是( )
Z(g),经10s达到平衡,生成0.1molZ。下列说法正确的是( )
A. 若增加Y的物质的量,则V正大于V逆平衡正向移动
B. 以Y浓度变化表示的反应速率为0.01mol·L-1·s-1
C. 该反应的平衡常数为10
D. 若降低温度,X的体积分数增大,则该反应的△H<0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列问题涉及前 20 号元素,请按要求用相应的化学用语作答:
(1)族序数等于周期数 2 倍的元素_____
(2)最外层电子数是内层电子数的一半且单质可作为电极材料的元素, 其在周期表中的位置是_____
(3)原子半径最大的短周期元素和地壳中含量最多的元素形成原子个数比为 1:1 的化合物,其阴离子符号为________________________________
(4)最高正价与最低负价代数和为零的短周期元素,其最高价氧化物与短周期元素中最稳定的气态氢化物的水溶液间发生反应的化学方程式___________________________
(5)第三周期元素中,简单离子半径最小的元素,其离子结构示意图为_____
(6)简单离子 Xn+与 Yn-具有相同的电子层结构,X n+的焰色为淡紫色,则 Y 的最高价氧化物对应水化物的名称为_____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】探究![]() 反应的速率影响因素,设计了以下实验。下列说法正确的是
反应的速率影响因素,设计了以下实验。下列说法正确的是
锥形瓶标号 |
| 蒸馏水 |
| 反应温度 | 浑浊出现时间 | 备注 |
1 |
| 0 mL | 10 mL |
| 10s | |
2 | 10mL | 5mL | 5 mL |
| 16 s | |
3 | 10mL | 0mL | 10 mL |
| 5 s | 第10s开始浑浊不再增多 |
4 | 10mL | 6mL | 4mL |
| 8s |
A.该反应也可通过测![]() 的体积变化来表示化学反应速率的快慢
的体积变化来表示化学反应速率的快慢
B.3号瓶用![]() 来表示速率为
来表示速率为![]()
C.由2号瓶和3号瓶实验结果可得温度越高反应速率越快
D.由1号瓶和4号瓶实验结果可得温度越高反应速率越快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】配制一定物质的量浓度的NaOH溶液时,造成所配制溶液浓度偏高的原因可能是( )
A.所用NaOH已潮解
B.定容时,俯视刻度线
C.用带游码的托盘天平称量NaOH固体质量时,误将砝码放在左盘,被称量物放在右盘
D.托盘天平的左右托盘上各放一张纸,调整天平至平衡后,将NaOH固体放在纸上称量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组微粒的空间构型相同的是( )
①NH3和H2O ②![]() 和H3O+ ③NH3和H3O+ ④O3和SO2 ⑤CO2和BeCl2 ⑥
和H3O+ ③NH3和H3O+ ④O3和SO2 ⑤CO2和BeCl2 ⑥![]() 和
和![]() ⑦BF3和Al2Cl6
⑦BF3和Al2Cl6
A.全部B.除④⑥⑦以外C.③④⑤⑥D.②⑤⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com