
| A.生铁抗腐蚀能力比纯铁强 |
| B.钢瓶在储存液氯前彻底干燥可减缓腐蚀 |
| C.水库铁闸与直流电源正极相连可减缓腐蚀 |
| D.常温下浓硝酸比浓盐酸更易使铁腐蚀 |
科目:高中化学 来源:不详 题型:单选题
 2PbSO4(s)+2H2O(l),下列说法正确的是
2PbSO4(s)+2H2O(l),下列说法正确的是| A.放电时,负极的电极反应式为:Pb – 2e-=Pb2+ |
| B.放电时,正极得电子的物质是PbO2 |
| C.充电时,电解质溶液中硫酸浓度减小 |
| D.充电时,阴极的电极反应式为:PbSO4 – 2e- +2H2O=PbO2+4H++SO42- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
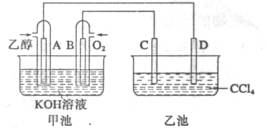
| A.甲池的电解池,乙池是原电池 |
| B.通入乙醇的铂电极反应式为C2H5OH+16OH-+12e-=2CO32-+11H2O |
| C.反应一段时间后,两池溶液的pH均未变化 |
| D.假如乙池中加入NaI溶液,则在乙池反应过程中,可以观察到C电极周围的溶液呈现棕黄色,反应完毕后,用玻璃棒搅拌溶液,则下层溶液呈现紫红色,上层接近无色 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
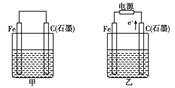
| A.若甲烧杯中盛有NaCl溶液,则石墨棒上的电极反应式为O2+2H2O+4e-= 4OH- |
| B.若乙烧杯中盛有则乙中的总反应为 |
| C.若甲烧杯中盛有CuSO4溶液,则甲中铁棒上的电极反应式为Fe-2e-=Fe2+ |
| D.若起始时乙中盛有200 mL pH=5的CuSO4溶液,一段时间后溶液的pH变为1,若要使溶液恢复到电解前的状态,可向溶液中加入0.6 g CuO |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2PbSO4+2H2O
2PbSO4+2H2O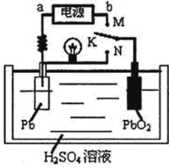
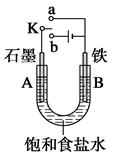
| A.实验室用铅蓄电池作电源电解饱和食盐水制取氯气,若制得氯气2.24L,则电池内消耗的H2SO4的物质的量是0.2mol |
| B.K与N相接时,H+向正极区迁移 |
| C.K与M连接时,所用电源的b极为负极 |
| D.K与M相接时,阳极附近的pH逐渐增大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
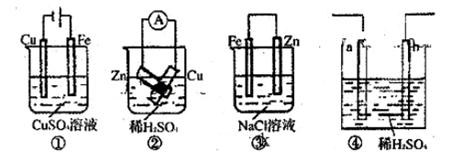
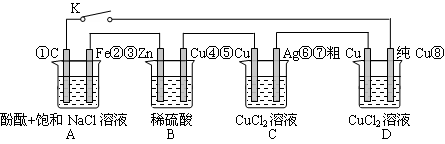
| A.图①连接好并放置片刻后,铁片会镀上一层铜 |
| B.图②连接好导线后(片与片相接触),电流表会发生明显偏转 |
| C.图③连接好并放置片刻后,在Zn片附近加一滴酚酞溶液,溶液变为红色 |
| D.图④发生反应为Fe+2H+=Fe2++H2↑时,a、b可能是同种材料的电极 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com