
 Pb2+(aq)+2I-(aq),加入KI溶液,下列说法正确的是 ( )
Pb2+(aq)+2I-(aq),加入KI溶液,下列说法正确的是 ( )| A.溶液中Pb2+和I-浓度都增大。 | B.溶度积常数Ksp增大 |
| C.沉淀溶解平衡向左移动 | D.浓度商Qc增大 |
科目:高中化学 来源:不详 题型:计算题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.澄清石灰水中加入盐酸:Ca(OH)2+2H+==2H2O+Ca2+ |
| B.硫酸氢钠溶液中逐滴加入氧氧化钡溶液,至溶液恰好呈中性: Ba2++OH-+SO42-+H+==BaSO4↓+H2O |
| C.少量Cl2加入FeBr2溶液中:2Fe2+ +Cl2==2Fe3++2Cl- |
| D.向AlCl3溶液中滴加过量氨水:Al3++4NH3·H2O=AlO2-+4NH4++2H2O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 Fe2+(aq)+S2-(aq),常温下Ksp = [Fe2+]·[ S2-]=8.1×10-17 mol2/L2。由此请回答:
Fe2+(aq)+S2-(aq),常温下Ksp = [Fe2+]·[ S2-]=8.1×10-17 mol2/L2。由此请回答:查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.难溶电解质在水中存在沉淀溶解平衡,且是一种动态平衡 |
| B.Ksp只与难溶电解质的性质和温度有关,而与沉淀的量和溶液中离子的浓度无关 |
| C.Ksp反映了物质在水中的溶解能力,可直接根据Ksp的数值大小比较电解质在水中的溶解能力大小 |
| D.可以通过浓度商(Qc)和Ksp的相对大小,来判断沉淀溶解平衡的移动方向 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
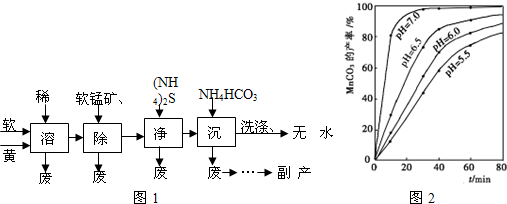
| Fe2+ | Fe3+ | Cu2+ | Mn2+ | |
| 开始沉淀的pH | 7.5 | 3.2 | 5.2 | 8.8 |
| 完全沉淀的pH | 9.7 | 3.7 | 7.8 | 10.4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.xy2 | B.xy | C.xy2 | D.4xy2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com