
【题目】现有7种元素的性质如下表所示,它们位于第二或第三周期,下列判断错误的是( )

A.编号为⑥的元素比编号为②的元素金属性强,所以⑥的单质能从②形成的盐溶液中置换出②的单质
B.编号为④⑤的原子之间可形成共价化合物
C.编号为⑦的元素的最低价氢化物与最高价氧化物对应的水化物能反应生成盐
D.编号为⑥的单质一般保存在煤油中
【答案】A
【解析】
元素①化合价只有-2,①是O元素;元素⑤化合价为+7、-1,⑤是Cl元素;元素③⑥的化合价都是+1,且⑥的半径大于③,所以③是Li元素、⑥是Na元素;元素④⑦的化合价都是+5、-3,且④的半径大于⑦,所以④是P元素、⑦是N元素;②的化合价是+2,半径大于Li,所以②是Mg元素。
A.⑥是Na、②是Mg,Na元素金属性强比Mg强,由于Na能与水反应,所以Na不能从镁盐溶液中置换出Mg,故A错误;
B. ④是P元素、⑤是Cl元素,原子之间可形成共价化合物PCl3、PCl5,故B正确;
C. ⑦是N元素,最低价氢化物是NH3,最高价氧化物对应的水化物是HNO3,NH3、HNO3能反应生成NH4NO3,故C正确;
D. ⑥是Na元素,金属钠性质活泼,密度比煤油大,所以一般保存在煤油中,故D正确;
选A。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】如图是几种烷烃的球棍模型,试回答下列问题:

(1) A、B、C 三者的关系是_______________
(2) A 的分子式为_______________,C 的名称为______________
(3)写出C 的同分异构体的结构简式______________
(4) B 是 2008 年北京奥运会火炬燃料的主要成分,若 22g B 气体完全燃烧,生成 CO2 气体和液态水,放出 1108 kJ 热量,则其燃烧的热化学方程式为_____________________________________________________________________________________.
(5)D 为六个碳的烷烃,且其一氯代物只有两种,写出 D 的结构简式_______________
查看答案和解析>>
科目:高中化学 来源: 题型:
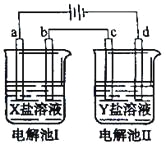
【题目】下图所示的电解池I和II中,a、b、c和d均为Pt电极。电解过程中,电极b和d上没有气体逸出,但质量均增大,且增重b﹤d。符合上述实验结果的盐溶液是
选项 | X | Y |
A. | MgSO4 | CuSO4 |
B. | AgNO3 | Pb(NO3)2 |
C. | FeSO4 | Al2(SO4)3 |
D. | CuSO4 | AgNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家在月球表面的土壤里发现了一种非常珍贵的资源—![]() He,它是可控核聚变的原料,关于:
He,它是可控核聚变的原料,关于:![]() He的叙述正确的是( )
He的叙述正确的是( )
A.![]() He核内中子数比质子数多l
He核内中子数比质子数多l
B.![]() He和
He和![]() He互为同位素
He互为同位素
C.He元素的相对原子质量就是3
D.![]() He和
He和![]() He属于同种元素,所以物理性质和化学性质都相同
He属于同种元素,所以物理性质和化学性质都相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W是原子序数依次增大的短周期元素,且X、Z原子序数之和是Y、W原子序数之和的1/2。甲、乙、丙、丁是由这些元素组成的二元化合物,M是某种元索对应的单质,乙和丁的组成元素相同,且乙是一种“绿色氧化剂”,化合物N是具有漂白性的气体(常温下)。上述物质间的转化关系如图所示(部分反应物和生成物省略)。下列说法正确的是

A. 原于半径:r(Y)>r(Z)>r(W)
B. 化合物N、乙烯使溴水褪色的原理相同
C. 含W元素的盐溶液可能显酸性、中性或碱性
D. Z与X、Y、W形成的化合物中,各元素均满足8电子结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素a、b、c、d的原子序数依次增大,X、Y、Z均是由这些元素组成的二元化合物,它们存在转化关系:M![]() X↑+Y↑+Z,组成化合物X的原子个数比为1:3,且液态X常用作制冷剂,Y的排放是形成酸雨的主要原因,且Y的组成元素位于同一主族且原子序数相差8,常温常压下Z为无色液体。下列说法错误的是( )
X↑+Y↑+Z,组成化合物X的原子个数比为1:3,且液态X常用作制冷剂,Y的排放是形成酸雨的主要原因,且Y的组成元素位于同一主族且原子序数相差8,常温常压下Z为无色液体。下列说法错误的是( )
A.原子半径:d>b>c>a
B.b的最低价氢化物能使湿润的蓝色石蕊试纸变红
C.M既能与强酸溶液反应,又能与强碱溶液反应
D.b2c5、dc3均为酸性氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学兴趣小组设计“乙醇催化氧化实验”来探究催化剂的催化机理并对反应后的产物进行分析,装置(夹持装置等已省略)如图所示。试回答以下问题:
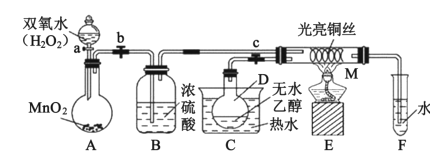
(1)C中热水的作用是___;在装入实验药品之前,应进行的操作是___。
(2)装入实验药品后,关闭活塞a、b、c,在铜丝的中间部分加热片刻,M处铜丝由红变黑,反应的化学方程式为___,然后打开活塞a、b、c,通过控制活塞a和b,间歇性地通入气体,即可在M处观察到受热部分的铜丝交替出现变红、变黑的现象。铜丝由黑变红时,发生反应的化学方程式为___。通过实验,可以得出结论:该实验过程中催化剂___(填“参加”或“不参加”)化学反应。
(3)反应进行一段时间后,试管F中能收集到的有机物主要有___、___。
(4)若试管F中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还有___。要除去该物质,可先在混合液中加入___(填字母),然后通过___即可(填操作名称)。
A.氯化钠溶液 B.苯 C.碳酸氢钠溶液 D.四氯化碳
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】往FeBr2溶液中通入Cl2时,随参加反应Cl2物质的量的变化,溶液中某些离子的浓度变化情况如图所示。下列说法不正确的是

A.当n(Cl2)<M mol时,发生的离子反应:2Fe2++Cl2=2Fe3++2Cl―
B.当n(Cl2)=M mol时,离子浓度关系:c(Fe3+)︰c(Br-)︰c(Cl-)=1︰2︰2
C.当n(Cl2)=2M mol时,离子浓度大小关系:c(Cl-)>c(Br-)
D.当Br―开始被氧化时,通入Cl2的物质的量小于原FeBr2的物质的量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分析如图所示的四个原电池装置,其中结论正确的是( )
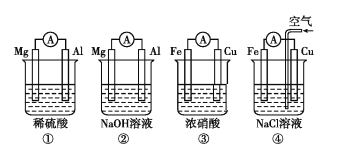
A.①②中Mg作负极,③④中Fe作负极
B.②中Mg作正极,电极反应式为6H2O+6e-=6OH-+3H2↑
C.③中Fe作负极,电极反应式为Fe-3e-=Fe3+
D.④中Cu作正极,电极反应式为2H++2e-=H2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com