

 ,故答案为:
,故答案为: ;
;
| ||


 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案科目:高中化学 来源: 题型:
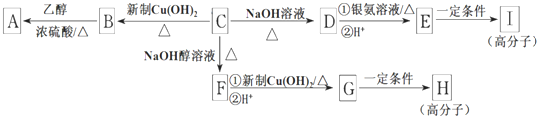
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、pH=1的溶液中:Fe2+、NO3-、Na+ |
| B、氨水中:Al3+、SO42-、Mg2+ |
| C、容器底部有硫粉:Fe3+、Cu2+、Cl- |
| D、NaNO3溶液中:Al3+、AlO2- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 甲 | K2SO4、BaCl2、NH4NO3 |
| 乙 | NaCl、Ca(OH)2、K2CO3 |
| 丙 | HCl、Na2SO4、NaCl |
| 丁 | K2SO4、Na NO3、KCl |
| A、甲 | B、乙 | C、丙 | D、丁 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验步骤 | 有关问题 |
| ①计算所需NaCl的质量 | |
| ②称量NaCl固体 | 用托盘天平需要称量NaCl的质量. |
| ③将NaCl加入100mL烧杯中,并加入适量水 | 为了加快溶解速率,可以采取哪些措施: 用玻璃棒不断搅拌. |
| ④将烧杯中溶液转移至250mL容量瓶中 | 为了防止溶液溅出,应采取什么措施:用玻璃棒引流. |
| ⑤向容量瓶中加蒸馏水至刻度线 | 在进行此操作时当加水至刻度线1-2厘米处应如何操作:改用胶头滴管加水至刻度线. |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Cl-、Ba2+、Mg2+、ClO- |
| B、Cl-、SO42-、Cu2+、Mg2+ |
| C、Cl-、SO42-、K+、Na+ |
| D、HCO3-、NO3-、Na+、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、HIO与HCN均为含有极性键的直线形极性分子 |
| B、SiO2与C02均为每摩含有4×6.02×1023对共用电子对的酸性氧化物 |
| C、Na2S浓溶液与稀盐酸分别滴加到饱和AgCl溶液中均一定有沉淀产生 |
| D、明矾与离子交换树脂均能将海水进行淡化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com