
【题目】下列反应中生成物总能量高于反应物总能量的是( )
A. 铝粉与氧化铁粉末反应 B. 乙醇燃烧
C. 碳酸钙受热分解 D. 氧化钙溶于水
 小学期末标准试卷系列答案
小学期末标准试卷系列答案科目:高中化学 来源: 题型:
【题目】今有0.1 mol·L-1Na2SO4溶液300mL,0.1 mol·L-1MgSO4溶液200mL和0.1 mol·L-1Al2(SO4)3溶液100mL,这三种溶液中硫酸根离子浓度之比是
A. 1︰1︰1 B. 3︰2︰1 C. 1︰1︰3 D. 3︰2︰3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】纳米技术制成的金属燃料、非金属固体燃料、氢气等已应用到社会生活和高科技领域。单位质量的A和B的单质燃烧时均放出大量热,可用作燃料。已知A和B为短周期元素,其原子的第一至第四电离能如下表所示:
电离能/(kJ·mol-1) | I1 | I2 | I3 | I4 |
A | 932 | 1 821 | 15 390 | 21 771 |
B | 738 | 1 451 | 7 733 | 10 540 |
(1)某同学根据上述信息,推断B的核外电子排布如下图所示,该同学所画的电子排布图违背了________。
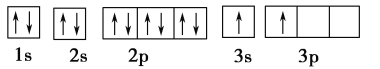
(2)ACl2分子中A原子的杂化类型为________。
(3)氢气作为一种清洁能源,必须解决它的储存问题,C60可用作储氢材料。已知金刚石中的C—C键的键长大于C60中C—C键的键长,有同学据此认为C60的熔点高于金刚石,你认为是否正确________(填“是”或“否”),并阐述理由______________________________。
(4)科学家把C60和钾掺杂在一起制造了一种富勒烯化合物,其晶胞如图所示,该物质在低温时是一种超导体。写出基态钾原子的价电子排布式______________,该物质的K原子和C60分子的个数比为________。
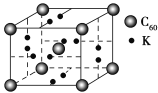
(5)继C60后,科学家又合成了Si60、N60等,C、Si、N元素的电负性由大到小的顺序是______________________________,NCl3分子的VSEPR模型为________。Si60分子中每个硅原子只跟相邻的3个硅原子形成共价键,且每个硅原子最外层都满足8电子稳定结构,则一个Si60分子中π键的数目为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)化学与生活密切相关,下列说法不正确的是 _________
A. 抗酸药能中和胃里过多的盐酸,缓解胃部不适
B. 柠檬因为有酸味,所以属于酸性食品
C. 目前加碘食盐中碘元素以KIO3形式存在
D. 利用油脂在碱性条件下的水解,可以制甘油和肥皂
(2)化学与生活息息相关。下列叙述正确的是 _________
A. 土豆的淀粉经水解可变成酒 B. 油脂经水解可变成葡萄糖
C. 鲜榨橙汁遇到碘水会变蓝 D. 馒头越嚼越甜
(3)纤维素被称为“第七营养素”。食物中的纤维素虽然不能被消化,但能刺激肠道蠕动和分泌消化液,有助于食物的消化和废物的排泄。在化学分类中,纤维素属于_________
A.蛋白质 B.脂肪 C.多糖
(4)某种食品的配料标签如图所示:

①其中,富含蛋白质的物质是______,富含油脂的物质是______,有防腐作用的是______。
②用于包装该食品的聚乙烯塑料包装属于______(填字母)。
A.有机高分子材料 B.无机非金属材料 C.金属材料
③大量使用塑料包装,会造成“____污染”,这种包装袋属于______(可回收资源 / 不可回收资源)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,电解质溶液的性质与变化是多样的,下列说法正确的是( )
A.pH相等的①CH3COONa ②NaClO ③NaOH三种溶液c(Na+)大小:①>②>③
B.往稀氨水中加水,溶液中的![]() 值变小
值变小
C.pH=4的H2S溶液与pH=10的NaOH溶液等体积混合,存在下列等式:c(Na+)+c(H+)=c(OH-)+2c(S2-)
D.Ca(ClO)2溶液中通入少量CO2,ClO-水解程度增大,溶液碱性增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从南方往北方长途运输水果时,常常将浸泡有高锰酸钾溶液的硅藻土放置在盛放水果的容器中,其目的是( )
A.利用高锰酸钾溶液吸收水果产生的乙烯,防止水果早熟
B.利用高锰酸钾溶液吸收水果周围的氧气,防止水果腐烂
C.利用高锰酸钾溶液的氧化性,催熟水果
D.利用高锰酸钾溶液杀死水果周围的细菌,防止水果霉变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】瑞典皇家科学院10月3日宣布2018诺贝尔化学奖一半颁给美国科学家弗朗西斯·阿诺德,奖励她实现了酶的定向转化,阿诺德研究的酶可以用于更加环保地制造化学产品,比如药物,还能生产可再生的燃料,让交通运输更加绿色环保。其中酶属于
A. 无机物 B. 单质 C. 氧化物 D. 有机物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸镁晶体(MgSO4·7H2O)是一种重要的化工原料,可用作制革、炸药、造纸、瓷器等。以菱镁矿(主要成分是碳酸镁,含少量FeCO3和不溶性杂质)为原料制取硫酸镁晶体的流程如下:

已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
阳离子 | Mg2+ | Fe2+ | Fe3+ |
开始沉淀 | 9.1 | 7.6 | 1.9 |
完全沉淀 | 11.1 | 9.7 | 3.2 |
(1) “氧化”步骤中,加入H2O2溶液的目的是________(用离子方程式表示)。“沉淀”步骤中,用氨水调节pH的范围是________。
(2) “过滤”所得滤液中含有的阳离子为Mg2+、________。
(3) “结晶”步骤中需蒸发浓缩滤液,使用的实验仪器有铁架台(含铁圈)、酒精灯、玻璃棒、____________________。
(4) 测定硫酸镁晶体样品中MgSO4·7H2O的含量常采用下列实验方法:
Ⅰ. 称取待测硫酸镁晶体样品1.500 g加入过量的EDTA,配成100 mL pH在9~10之间的溶液A。
Ⅱ. 移取25.00 mL溶液A于锥形瓶中,用0.1000 mol·L-1 Zn2+标准溶液与过量的EDTA反应,消耗Zn2+标准溶液20.00 mL。
Ⅲ. 另移取25.00 mL溶液A于另一只锥形瓶中,调节pH为5~6,用0.100 0 mol·L-1 Zn2+标准溶液与之充分反应,消耗Zn2+标准溶液35.00 mL。
已知:①pH为9~10时,Mg2+、Zn2+均能与EDTA(H2Y2-)反应:Mg2++H2Y2-===MgH2Y Zn2++H2Y2-===ZnH2Y
②pH为5~6时,Zn2+除与EDTA反应,还能与MgH2Y反应:Zn2++MgH2Y===ZnH2Y+Mg2+
③样品中杂质不参与反应。
计算硫酸镁晶体样品中MgSO4·7H2O的质量分数________。(写出计算过程)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com