
【题目】(1)化学与生活密切相关,下列说法不正确的是 _________
A. 抗酸药能中和胃里过多的盐酸,缓解胃部不适
B. 柠檬因为有酸味,所以属于酸性食品
C. 目前加碘食盐中碘元素以KIO3形式存在
D. 利用油脂在碱性条件下的水解,可以制甘油和肥皂
(2)化学与生活息息相关。下列叙述正确的是 _________
A. 土豆的淀粉经水解可变成酒 B. 油脂经水解可变成葡萄糖
C. 鲜榨橙汁遇到碘水会变蓝 D. 馒头越嚼越甜
(3)纤维素被称为“第七营养素”。食物中的纤维素虽然不能被消化,但能刺激肠道蠕动和分泌消化液,有助于食物的消化和废物的排泄。在化学分类中,纤维素属于_________
A.蛋白质 B.脂肪 C.多糖
(4)某种食品的配料标签如图所示:

①其中,富含蛋白质的物质是______,富含油脂的物质是______,有防腐作用的是______。
②用于包装该食品的聚乙烯塑料包装属于______(填字母)。
A.有机高分子材料 B.无机非金属材料 C.金属材料
③大量使用塑料包装,会造成“____污染”,这种包装袋属于______(可回收资源 / 不可回收资源)。
【答案】 B D C 鸡蛋 棕榈油 苯甲酸钠 A 白色 可回收资源
【解析】(1)A.抗酸药能中和胃里过多的盐酸,如抗酸药“胃舒平”、“斯达舒”主要成分都为Al(OH)3,缓解胃部不适原理为3HCl+Al(OH)3═AlCl3+3H2O,故A正确;B.柠檬、桔子等有酸味的水果,含钾、钠、钙、镁等元素,在人体内代谢后生成碱性物质,属于碱性食物,故B错误;C.碘酸钾稳定性高,不易被氧化,所以目前加碘食盐中含碘元素的物质主要是KIO3,故C正确;D.油脂在碱性条件下水解生成甘油和硬脂酸钠,俗称皂化反应,可用来制肥皂,故D正确;答案为B。
(2)A.土豆中的淀粉经水解生成葡萄糖,故A错误;B.油脂是高级脂肪酸甘油酯,水解生成高级脂肪酸和甘油,故B错误;C.鲜榨橙汁不含淀粉,遇到碘水不会变蓝,故C错误;D.唾液中含有淀粉酶,可将淀粉水解为葡萄糖,故馒头越嚼越甜,故D正确;故选D。
(3)纤维素属于糖类中的多糖,能水解生成葡萄糖,故答案为C;
(4)①瘦肉类、蛋类、豆类富含蛋白质,因此鸡蛋富含蛋白质,植物油和动物脂肪富含油脂,因此棕榈油富含油脂;苯甲酸钠是防腐剂有防腐作用;
②用于包装该食品的聚乙烯是一种聚合物,属于有机高分子化合物,故答案为A;
③大量使用塑料包装,会造成“白色污染”,这种包装袋属于可回收资源 。


科目:高中化学 来源: 题型:
【题目】解释下列事实的方程式正确的是
A. 向Na2SiO3溶液中通入过量CO2:SiO32-+ CO2+ H2O= H2SiO3(胶体)+ CO32-
B. 用醋酸溶液除水垢中的CaCO3:CaCO3+2H+=Ca2++H2O+CO2↑
C. 向煤中加入石灰石可减少煤燃烧时SO2的排放:2CaCO3+O2+2SO2![]() 2CO2+2CaSO4
2CO2+2CaSO4
D. 碳酸氢钠溶液与少量澄清石灰水混合出现白色沉淀:CO32﹣+Ca2+=CaCO3↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中Cl元素全部被氧化的是
A.KClO3+6HCl=KCl+3Cl2↑+3H2O
B.2NaCl电解2Na+Cl2↑
C.H2+Cl2光照2HCl
D.2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常教,下列叔述正确的是( )
A. 常温常压下,9.2gNO2气体中.分子数为0.2NA
B. pH=2的硫酸溶液中,H+数目为0.01NA
C. 将0.05molFeCl3全部转化为Fe(OH)3胶体,则胶粒数目为0.05NA
D. 20gD2O中含有的质子数为10NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某共价化合物含C,H,N 3种元素,已知其分子内的4个氮原子排列成内空的四面体结构,且每2个氮原子之间都有1个碳原子,分子中无C﹣C,C═C,C≡C键,则此化合物的化学式是( )
A.C6H12N4
B.C4H8N4
C.C6H10N4
D.C6H8N4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列所示装置正确且能完成相关实验的是( )
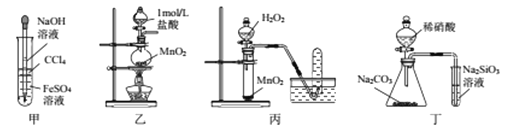
A. 用甲所示装置制取并观察Fe(OH)2 B. 用乙所示装置制取少量Cl2
C. 用丙所示装置制取O2 D. 用丁所示装置比较N、C、Si的非金属性强弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知16 g固体硫完全燃烧时放出148.4 kJ的热量,该反应的热化学方程式是________________________
(2)如图是某温度下,N2与H2反应过程中能量变化的曲线图。
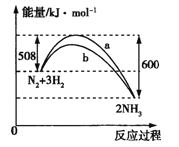
a、b两条曲线产生区别的原因很可能是________________。
(3)在101 kPa时,H2在1.00 mol O2中完全燃烧生成2.00 mol H2O(l)时放出571.6 kJ热量,则H2的热值为________
(4)已知:Fe2O3(s)+3C(石墨)===2Fe(s)+3CO(g) ΔH=489.0 kJ·mol-1
CO(g)+![]() O2(g)===CO2(g) ΔH=-283.0 kJ·mol-1
O2(g)===CO2(g) ΔH=-283.0 kJ·mol-1
C(石墨)+O2(g)===CO2(g) ΔH=-393.5 kJ·mol-1
由Fe(s)和O2(g)反应生成Fe2O3(s)的热化学方程式为_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由W、X、Y、Z四种金属按下列装置进行实验。下列说法不正确的是

A. 装置甲中X电极附近有气泡产生
B. 装置乙中Y电极上的反应式为Cu2++2e-=Cu
C. 装置丙中溶液的pH增大
D. 四种金属的活动性强弱顺序为W>X>Y>Z
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com