
固体单质A和气体单质B在容积一定的密闭容器中完全反应生成气体C,相同温度下测得容器内压强不变,若产物气体C的密度是原气体密度的4倍,则判断正确的是( )
|
| A. | 两种单质A、B的摩尔质量之比是1:4 |
|
| B. | 反应前后的气体质量之比一定是1:4 |
|
| C. | 在生成物C中,A的质量分数为50% |
|
| D. | C中A、B两元素的原子个数比为3:1 |
| 阿伏加德罗定律及推论.. | |
| 专题: | 阿伏加德罗常数和阿伏加德罗定律. |
| 分析: | 根据阿伏加德罗定律可知,容器的体积固定,相同温度下测得容器内压强不变,则反应前后气体的物质的量相同,若产物气体C的密度是原气体密度的4倍,则气体的质量是反应前气体质量的4倍,化学反应遵循质量守恒定律,则A的质量为B的质量的3倍,在生成物中A的质量分数为75%,由于不能确定A和B的物质的量的关系,则不能确定A、B的摩尔质量和原子个数之间的关系. |
| 解答: | 解:A、由于不能确定A和B的物质的量的关系,则不能确定A、B的摩尔质量,故A错误; B、容器的体积固定,若产物气体C的密度是原气体密度的4倍,则气体的质量是反应前气体质量的4倍,所以反应前后的气体质量之比一定是1:4,故B正确; C、根据阿伏加德罗定律可知,相同温度下测得容器内压强不变,则反应前后气体的物质的量相同,反应前后的气体质量之比为1:4,化学反应遵循质量守恒定律, 则A的质量为B的质量的3倍,在生成物中A的质量分数为75%,故B错误; D、由于不能确定A和B的物质的量的关系,则不能确定C中A、B两元素的原子个数比,故D错误. 故选B. |
| 点评: | 本题考查阿伏加德罗定律及推论的应用,题目难度中等,注意根据题意只能确定气体的物质的量关系和质量关系,但不能确定固体与气体的物质的量的关系. |


 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案科目:高中化学 来源: 题型:
选用正确的试剂和分离方法,除去下列物质中所含少量杂质(括号内为杂质):
例: 乙醇(水)生石灰,蒸馏
(1)苯(苯酚) ;(2)甲烷(乙烯) ;(3)乙酸乙酯(乙酸) 。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)17℃、1.01×105Pa,密闭容器中N2O4和NO2的混合气体达到平衡时,c(NO2)=0.0300 mol·L-1、c(N2O4)=0.0120 mol·L-1。计算反应2NO2(g) N2O4(g)的平衡常数K。(写出计算过程)
N2O4(g)的平衡常数K。(写出计算过程)
(2)现用一定量的Cu与足量的浓HNO3反应,制得1.00L已达到上述平衡时的N2O4和NO2的混合气体(17℃、1.01×105Pa),理论上至少需消耗Cu多少克?(写出计算过程)
查看答案和解析>>
科目:高中化学 来源: 题型:
等物质的量的钠、镁、铝分别与足量稀盐酸反应,在同温同压下放出H2的体积比为( )
|
| A. | 1:2:3 | B. | 1:1:1 | C. | 3:2:1 | D. | 2:3:6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
当溶液中XO42﹣ 和SO32﹣的离子数之比为1:2时,恰好完全发生氧化还原反应,X在还原产物中的化合价为( )
|
| A. | +1 | B. | +2 | C. | +3 | D. | +4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列氧化还原反应中,实际参加反应的氧化剂与还原剂的物质的量之比正确的是( )
①KClO3+6HCl(浓)═KCl+3Cl2↑+3H2O;5:1
②Fe2O3+2Al Al2O3+2Fe;1:2
Al2O3+2Fe;1:2
③4HC1(浓)+MnO2 MnC12+C12↑+2H2O;1:2
MnC12+C12↑+2H2O;1:2
④3NO2+H2O═2HNO3+NO;2:1.
|
| A. | ①②③ | B. | ②③ | C. | ②④ | D. | ①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
在托盘天平右盘上放一个盛有100mL3mol•L﹣1NaOH溶液的烧杯,左盘上放一个盛有100mL3mol•L﹣1盐酸的烧杯,调节天平至平衡,然后在两烧杯中各加入等质量的铝片,反应完全后,则天平可能出现的情况是( )
|
| A. | 左盘下沉 | B. | 右盘下沉 | C. | 仍保持平衡 | D. | 无法判断 |
查看答案和解析>>
科目:高中化学 来源: 题型:
如图是某化学学习小组用来探究钠与水反应的实验装置。该装置可以集反应、收集、检验气体于一体。图中钠块是用大头针叉住的。请填空:
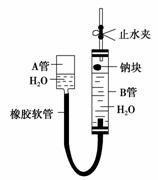
(1)钠块的位置靠近B管上的胶塞,为了尽可能收集到纯净的气体,应先________(填“打开”或“关闭”)止水夹,然后慢慢提升A管,待B管中钠块与水接触时,应立即________(填“打开”或“关闭”)止水夹,所以A管的作用是________
________________________________________________________________________。
(2)钠与水反应的化学方程式是__________________________________________。
(3)为了安全,钠与水反应产生的气体在点燃前应该__________,而该方法中可以直接点燃这种气体,其原因是______________________点燃该实验中产生的气体的操作方法是先用明火靠近导气管口,然后打开止水夹,可以观察到气体的燃烧,该气体燃烧的化学方程式是__________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com