
如图是某化学学习小组用来探究钠与水反应的实验装置。该装置可以集反应、收集、检验气体于一体。图中钠块是用大头针叉住的。请填空:
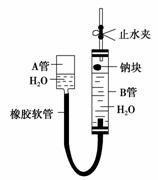
(1)钠块的位置靠近B管上的胶塞,为了尽可能收集到纯净的气体,应先________(填“打开”或“关闭”)止水夹,然后慢慢提升A管,待B管中钠块与水接触时,应立即________(填“打开”或“关闭”)止水夹,所以A管的作用是________
________________________________________________________________________。
(2)钠与水反应的化学方程式是__________________________________________。
(3)为了安全,钠与水反应产生的气体在点燃前应该__________,而该方法中可以直接点燃这种气体,其原因是______________________点燃该实验中产生的气体的操作方法是先用明火靠近导气管口,然后打开止水夹,可以观察到气体的燃烧,该气体燃烧的化学方程式是__________________________。
科目:高中化学 来源: 题型:
固体单质A和气体单质B在容积一定的密闭容器中完全反应生成气体C,相同温度下测得容器内压强不变,若产物气体C的密度是原气体密度的4倍,则判断正确的是( )
|
| A. | 两种单质A、B的摩尔质量之比是1:4 |
|
| B. | 反应前后的气体质量之比一定是1:4 |
|
| C. | 在生成物C中,A的质量分数为50% |
|
| D. | C中A、B两元素的原子个数比为3:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
美国一个海军航空站安装了一台250 kW的MCFC型燃料电池。该电池可同时供应电和蒸汽,其燃料为H2,电解质为熔融的K2CO3,工作温度为600~800 ℃。已知该电池的总反应为2H2+O2 2H2O,负极反应为H2+CO32--2e-
2H2O,负极反应为H2+CO32--2e- H2O+CO2。下列推断正确的是
H2O+CO2。下列推断正确的是
A.正极反应为4OH--4e- O2↑+2H2O B.放电时, CO32-向负极移动
O2↑+2H2O B.放电时, CO32-向负极移动
C.电池供应1 mol水蒸气,转移的电子的物质的量为4 mol D.放电时CO32-向正极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
前四周期原子序数依次增大的六种元素A、B、C、D、E、F中,A、B属于同一短周期元素且相邻,A元素所形成的化合物种类最多,C、D、E、F是位于同一周期的金属元素,基态C、F原子的价电子层中未成对电子均为1个,且C、F原子的电子数相差为10,基态D、E原子的价电子层中未成对电子数分别为4、2,且原子序数相差为2。
(1)六种元素中第一电离能最小的是 (填元素符号,下同),电负性最大的是 。
(2)黄血盐是由A、B、C、D四种元素形成的配位化合物C4[D(AB)6],易溶于水,广泛用作食盐添加剂(抗结剂)。请写出黄血盐的化学式 ,1 mol AB-中含有π键的数目为 ,黄血盐晶体中各种微粒间的作用力不涉及 (填序号)。
a.离子键 b.共价键 c.配位键
d.金属键 e.氢键 f.分子间的作用力
(3)E2+的价层电子排布图为 ,很多不饱和有机物在E催化下可与H2发生加成反应:如①CH2=CH2、②HC≡CH、③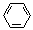 、④HCHO。其中碳原子采取sp2杂化的分子有 (填物质序号),HCHO分子的立体结构为 形,它加成产物的熔、沸点比CH4的熔、沸点高,其主要原因是(须指明加成产物是何物质) 。
、④HCHO。其中碳原子采取sp2杂化的分子有 (填物质序号),HCHO分子的立体结构为 形,它加成产物的熔、沸点比CH4的熔、沸点高,其主要原因是(须指明加成产物是何物质) 。
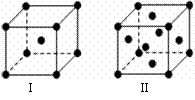 (4)金属C、F晶体的晶胞结构如右图(请先判断对应的图),C、F两种晶体晶胞中金属原子的配位数之比为 。金属C的晶胞中,若设该晶胞的密度为a g/cm3,阿伏加得罗常数为NA,C原子的摩尔质量为M,则表示C原子半径的计算式为 。
(4)金属C、F晶体的晶胞结构如右图(请先判断对应的图),C、F两种晶体晶胞中金属原子的配位数之比为 。金属C的晶胞中,若设该晶胞的密度为a g/cm3,阿伏加得罗常数为NA,C原子的摩尔质量为M,则表示C原子半径的计算式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于Na2CO3和NaHCO3性质的说法错误的是( )
A.热稳定性:NaHCO3<Na2CO3
B.与同浓度盐酸反应的剧烈程度:NaHCO3<Na2CO3
C.相同温度时,在水中的溶解性:NaHCO3<Na2CO3
D.等物质的量浓度溶液的pH:NaHCO3<Na2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
在Na2SO4、NaCl、NaOH的混合溶液中,含有Na+、SO42-、OH-的个数比是8:1:2,则溶液中Na2SO4、NaCl、NaOH的物质的量之比是( )
A.1:1:1 B.1:4:2 C.1:2:4 D.1:3:2
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室需要0.1 mol/L NaOH溶液450 mL和0.5 mol/L硫酸溶液450 mL.根据这两种溶液的配制情况回答下列问题:

(1) 根据计算得知,所需质量分数为98%、密度为1.84 g/cm3的浓硫酸的体积为 ____ mL(计算结果保留一位小数,下同)。
(2)如图所示的仪器中配制溶液肯定不需要的是 (填序号),仪器C的名称是 ,本实验所需玻璃仪器E的名称为
(3)在配制NaOH溶液实验中,其他操作均正确。若定容时仰视刻度线,则所配制溶液浓度 ______0.1 mol/L(填“大于”“等于”或“小于”,下同)。若NaOH溶液未冷却即转移至容量瓶定容,则所配制溶液浓度__ 0.1 mol/L。
(4) 下列操作不正确的是 (填序号)。[]
A.使用容量瓶前检查它是否漏水
B.容量瓶用蒸馏水洗净后,再用待配液润洗
C.将氢氧化钠固体放在天平托盘的滤纸上,准确称量并放入烧杯中溶解后,立即注入容量瓶中
D.将准确量取的18.4 mol·L-1的硫酸,注入已盛有30 mL水的100 mL的容量瓶中,加水至刻度线
E.定容时不小心水加多了少许,立即用胶头滴管吸出即可
 F.定容后塞好瓶塞,用食指顶住瓶塞,用另一只手的手指托住瓶底,把容量瓶倒转摇匀
F.定容后塞好瓶塞,用食指顶住瓶塞,用另一只手的手指托住瓶底,把容量瓶倒转摇匀
(5)右图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:
①将________升氯化氢(标准状况)通入1.00L水中可得到36.5﹪的浓盐酸,该浓盐酸中HCl的物质的量浓度为
②取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是 。
A.溶液中HCl的物质的量 B.溶液的浓度
C.溶液中Cl-的数目 D.溶液的密度
查看答案和解析>>
科目:高中化学 来源: 题型:
已知下列热化学方程式: ( )
2H2(g)+O2(g)===2H2O(g);ΔH=-483.6 kJ/mol
H2(g)+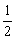 O2(g)===H2O(g);ΔH=-241.8 kJ/mol
O2(g)===H2O(g);ΔH=-241.8 kJ/mol
H2(g)+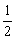 O2(g)===H2O(l);ΔH=-285.8 kJ/mol 则氢气的燃烧热为
O2(g)===H2O(l);ΔH=-285.8 kJ/mol 则氢气的燃烧热为
A.438.6 kJ/mol B.241.8 kJ/mol C.285.8 kJ/mol D.无法确定
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com