
����Ŀ�������������壨FeC2O4��2H2O����Է�������Ϊ180���ʵ���ɫ��������������Ӱ����ijʵ��С����������һϵ��̽����
I.�����������������ȷֽ�����̽����
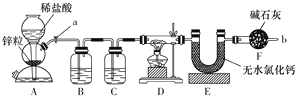
��1���������ɷֵ�̽����С���Ա������ͼװ�ã����ظ�ѡ�ã�����ʵ�飺
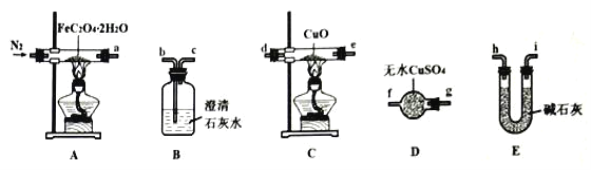
��װ��D������Ϊ____��
�ڰ������������ҵķ�������װ�õ�����˳��Ϊ____��β������װ�ã���ͼ�и������ӿڵ���ĸ��ţ���
��ʵ��ǰ��ͨ��һ��ʱ��N2����Ŀ��Ϊ____��
��ʵ��֤������������к���CO�����ݵ�ʵ������Ϊ_____��
��2���������ɷֵ�̽������ַ�Ӧ��A����Ӧ���в�����ɫ���塣С���Ա���ʵ��֤������ɷ�ֻ��FeO����ʵ�����������Ϊ��___��
��3�����ݣ�1���ͣ�2�����ۣ���֪A����Ӧ���з�����Ӧ�Ļ�ѧ����ʽΪ��___��
��.��������������Ʒ���ȵIJⶨ
��ҵ�ƵõIJ������������г�����FeSO4���ʣ��ⶨ�䴿�ȵIJ������£����ʲ����뷴Ӧ����
����1����ȡ2g��������������Ʒ������ϡH2SO4�У����250mL��Һ��
����2��ȡ������Һ25.00mL�������м���0.01mol��L1KMnO4��Һ��ǡ����ȫ��Ӧʱ���� KMnO4��Һ30mL��
[��֪��FeC2O4+KMnO4+H2SO4��Fe2(SO4)3+CO2��+MnSO4+K2SO4+H2O��δ��ƽ��]
��4����������������Ʒ�Ĵ���Ϊ____��������1������Һʱ����Fe2+����������ⶨ�����____������ƫ��������ƫ������������������
���𰸡������Σ������ agfbchi����ih��de����ed��bc �ž�װ���еĿ�������ֹ����ʱ������ը C����Ӧ���й����ɺڱ�죬���ij���ʯ��ˮ����� ȡ������������ϡ���ᣬ����������˵���������ڣ�ֻ�����������������𰸺������ɣ� FeC2O42H2O![]() FeO+CO��+CO2��+2H2O 45% ƫ��
FeO+CO��+CO2��+2H2O 45% ƫ��
��������
���������ɷֵ�̽������������������װ��A�м��ȷֽ⣬���ɵ�����ͨ��װ��D������ͭ����ˮ�����Ĵ��ڣ�ͨ��װ��B�г���ʯ��ˮ����CO2�����ɣ�ͨ��װ��E���������ͨ��װ��C�к�����ͭ��Ӧ����ͭ�Ͷ�����̼����ͨ��Bװ�ü������ɵĶ�����̼���壬���ڼ���CO�����β��������
��
I (1)��װ��D������Ϊ�������Σ�����ܣ�
���������ɷֵ�̽������������������װ��A�м��ȷֽ⣬���ɵ�����ͨ��װ��D������ͭ����ˮ�����Ĵ��ڣ�ͨ��װ��B�г���ʯ��ˮ����CO2�����ɣ�ͨ��װ��E���������ͨ��װ��C�к�����ͭ��Ӧ����ͭ�Ͷ�����̼����ͨ��Bװ�ü������ɵĶ�����̼���壬���ڼ���CO���������������ҵķ�������װ�õ�����˳��Ϊ��agfbchi����ih��de����ed��bc���������β������װ�ã�
�۲��������ֽ���������CO����O2��ϼ��Ȼᱬը��ʵ��ǰ��ͨ��һ��ʱ��N2����Ŀ��Ϊ���ž�װ���еĿ�������ֹ����ʱ������ը��
��ʵ��֤������������к���CO��CuO��ת��ΪCu������CO2���ɣ����ij���ʯ��ˮ�����ǣ����ݵ�ʵ������Ϊ��C����Ӧ���й����ɺڱ�죬���ij���ʯ��ˮ����ǣ�
(2)��ַ�Ӧ��A����Ӧ���в�����ɫ���塣��ɫ�������ΪFe��FeO��С���Ա���ʵ��֤������ɷ�ֻ��FeO�ķ�����ȡ������������ϡ���ᣬ����������˵���������ڣ�ֻ������������
(3)����(1)��(2)���ۣ���֪A����Ӧ���з�����Ӧ�Dz�����������ֽ���������������һ����̼��������̼��ˮ����Ӧ�Ļ�ѧ����ʽΪ��FeC2O4��2H2O ![]() FeO+CO��+CO2��+2H2O��
FeO+CO��+CO2��+2H2O��
��(4)���ʲ����뷴Ӧ������FeC2O4+KMnO4+H2SO4��Fe2(SO4)3+CO2��+MnSO4+K2SO4+H2O��δ��ƽ����Fe�Ļ��ϼ۴ӣ�2���ߵ���3��C2O42����C�Ļ��ϼ�Ϊ��3�����ϼ����ߵ���4�����ܹ�����3�ۣ�KMnO4��Mn�Ļ��ϼ۴ӣ�7���͵���2������5�ۣ����ϼ������غ㣬����Թ�ϵʽ5FeC2O4��3KMnO4������ɵIJ���������Һ��Ũ��c����![]() �� 3��c(FeC2O4)��25mL=5��0.01mol/L��30mL�����c(FeC2O4)=0.02mol/L����Ʒ��FeC2O4�����ʵ���n=0.02mol/L��0.25L=5��10��3mol����Ʒ����m=nM=5��10��3mol��180g��mol��1=0.9g������������Ϊ
�� 3��c(FeC2O4)��25mL=5��0.01mol/L��30mL�����c(FeC2O4)=0.02mol/L����Ʒ��FeC2O4�����ʵ���n=0.02mol/L��0.25L=5��10��3mol����Ʒ����m=nM=5��10��3mol��180g��mol��1=0.9g������������Ϊ![]() ��100%=45%��
��100%=45%��
������1������Һʱ����Fe2+�������������ĵ�KMnO4ƫС������Ʒ����ƫС���ⶨ���ƫ�͡�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2019��7��1�����Ϻ�������������ǿ��ʱ������������ȵ�Ҳ��ʼʵ���������ࡣ���������ҹ����������ľ��ģ������������뻯ѧϢϢ��أ������й�˵��������ǣ�![]() ��
��
A.�����ľ���ϩ�������ڰ�ɫ����������ʹ��ˮ��ɫ
B.�ɻ��յ��������к�����������ͨ�����������������ȡ
C.�Ͼɵ���к��������ӵ��ؽ�����������������
D.���ޡ��顢˿��ë���ϳ���ά�ķϾ�����ȼ�մ���ʱ��ֻ����CO2��H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������AlCl3��MgSO4�����Һ�������в��ϼ���NaOH��Һ���õ��������������NaOH��Һ�������ͼ��ʾ��ԭ��Һ��Cl����SO42-�����ʵ���֮��Ϊ�� ��
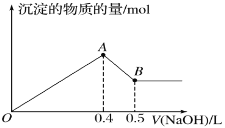
A.3��1B.4��1C.5��1D.6��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ܵĴ洢������Ӧ�õ���Ҫƿ�����������ʹ���������������õ���Ҫ�о�����
(1)Ti(BH4)2��һ�ֹ���Ԫ�����⻯�ﴢ����ϡ�
�ٻ�̬Ti2+�к��еĵ�����Ϊ______������ռ�ݵ�����ܼ���______�����ܼ����е�ԭ�ӹ����Ϊ______��
��BH4-��Bԭ�ӵ��ӻ���ʽ��______��
(2)�����⻯���Ǿ������÷�չǰ���Ĵ�����ϡ�
��LiH�У����Ӱ뾶��Li+______ H-������>������=������<������
��ij��������Ƕ����ڽ���Ԫ��M���⻯�M�IJ��ֵ��������±���ʾ��
I1/kJmol-1 | I2/kJmol-1 | I3/kJmol-1 | I4/kJmol-1 | I5/kJmol-1 |
738 | 1451 | 7733 | 10540 | 13630 |
���⻯��Ļ�ѧʽΪ______��
(3)Һ���Ǹ������ʣ������ܵ��������塣
��NH3����Է�������С��PH3����NH3�ķе�ȴԶ����PH3����ԭ���� ______��
��NH3���ͷ������пչ����BF3��Ӧ�γ��µĻ�����û�����ĽṹʽΪ ______��
(4)2008�꣬Yoon���˷���Ca��C60(���ӽṹ��ͼ1)���ɵ�Ca32C60�ܴ�������H2���ӡ�
��C60���������ڱ���CS2��C60�� ______ ���ӣ����������������Ǽ���������
��1mol C60�����У������� ����ĿΪ ______ ��(�����ӵ�������NA��ʾ)��

(5)ij�����⻯�ﴢ����ϵľ����ṹ��ͼ2��ʾ���ý����⻯��Ļ�ѧʽΪ ______����֪�þ�����ܶ�Ϊagcm-3������Ԫ��R�����ԭ������ΪM�������ӵ�����ΪNA����þ��������Ϊ ______ cm3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ʮ�����ʣ���HCl����NaHCO3����K2SO4��Һ����SiO2�������Ǿ��壻��NaOH���������������壻��NH3��H2O�����������Al2(SO4)3
��1���������������ڵ���ʵ���____(�����)���������ε�������Ģٵ�ˮ��Һ�����ֵ�ʵ��������___��
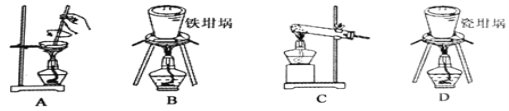
��2���â���ޱ����Ʊ������ƣ��ɲ���ͼ�е�װ��Ϊ____����ѡ���ţ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������(��Ҫ�ɷ�ΪFe2O3��Fe3O4��FeO��SiO2��)����������Ĺ�ҵ���������ۺ����öԻ�������������ʵ���塣���û���������Ϊԭ���Ʊ��ߵ�����������(Fe2O3)���������£�
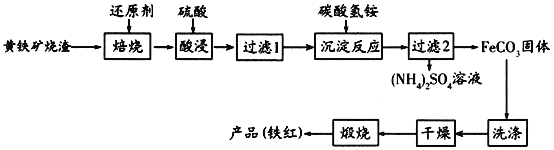
�ش��������⣺
(1)��������ʱ�����ӵ���ѻ�ԭ����________(�����)��
a����̿ b����� c��þ�� d��п��
(2)������1�������Һ�����ʵ���Ҫ�ɷ���________________(�ѧʽ)��
(3)��������Ӧ��ʱ���˻�������������ԭ��Ϊ______________________(�����ӷ���ʽ��ʾ)��
(4)Ϊ����FeCO3�Ƿ�ϴ�Ӹɾ������������һ��ϴ��Һ�еμ�________��Һ��
(5)�ڿ���������FeCO3�����������һ���������Ӧ�Ļ�ѧ����ʽΪ________��
(6)���л���������500t����Ԫ�ص���������Ϊ16.8��������һϵ��ת���õ�90t���죬�ò�Ʒ�IJ���Ϊ________��(��ʾ��![]() )
)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ��������ͼװ�òⶨFeO��Fe2O3����������Fe2O3��������Dװ�õ�Ӳ��˫ͨ�������еĹ���������FeO��Fe2O3�Ļ���
(1)װ��B��������______________ ��װ��C��ʢװ��Һ����______________��
(2)��Ӳ��˫ͨ�������з����Ļ�ѧ��Ӧ����ʽ��_______________________��
(3)��ΪFeO��Fe2O3���ʵ���֮��1��1�Ĺ��������Ӧ��ȫ��U�ܵ���������7.2 g����������Fe2O3������Ϊ______________��
(4)U��E�ұ����Ӹ����F��Ŀ����________________���������F�����Fe2O3��������_____________(����ƫ������ƫС��������Ӱ����)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͬ�����£����и����Ȼ�ѧ����ʽ����Һ�еķ�Ӧ������ϡ��Һ֮����У��У���H2����H1����
A.CO2(s)+C(s)=2CO(g) ��H1 CaO(s)+H2O(l)=Ca(OH)2(s) ��H2
B.NH3 ��H2O(aq)+H+(aq)= NH4+ (aq)+H2O(l) ��H1 H+(aq)+OH-(aq)= H2O(aq) ��H2
C.N2(g)+O2 (g) ![]() 2NO(g) ��H1 N2(g)+O2 (g)
2NO(g) ��H1 N2(g)+O2 (g) ![]() 2NO(g) ��H2
2NO(g) ��H2
D.CH4(g)+2O2(g)= CO2(g)+ 2H2O(l) ��H1 CH4(g)+2O2(g)= CO2(g)+ 2H2O(g) ��H2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�������ȷ���ǣ�������
A.�ɷ�Ӧ��M(s)+N(g) ![]() R(g) ��H1 ��M(g)+N(g)
R(g) ��H1 ��M(g)+N(g) ![]() R(g) ��H2����H 2����H 1
R(g) ��H2����H 2����H 1
B.��֪��2SO2(g)+O2(g) ![]() 2SO3(g)����H=��98.3kJ/mol����1molSO2��0.5molO2����һ�ܱ������з�Ӧ���ų�49.15kJ������
2SO3(g)����H=��98.3kJ/mol����1molSO2��0.5molO2����һ�ܱ������з�Ӧ���ų�49.15kJ������
C.��⾫��ͭʱ����Դ�����봿ͭ�������ҵ������ҺŨ��ʼ�ձ��ֲ���
D.�ö��Ե缫��� Na2SO4��Һ������������1mol����ʱ���ɼ�18 g ˮʹ��Һ�ָ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com