
【题目】磺酰氯(SO2Cl2)在医药、染料行业有重要用途,其熔点为-54.1 C,沸点为69.2 °C,易水解。某学习小组在实验室用SO2和Cl2在活性炭作用下制备SO2Cl2(SO2 +Cl2![]() SO2Cl2),设计如图实验(夹持装置略去)。下列说法不正确的是
SO2Cl2),设计如图实验(夹持装置略去)。下列说法不正确的是
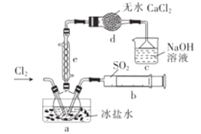
A.c中的NaOH溶液可换成NaCl溶液,效果相同
B.e中的冷却水应从下口入上口出
C.d的作用是防止水蒸气进人a中使SO2Cl2水解
D.a中冰盐水有助于SO2Cl2液化,提高SO2和Cl2的转化率.
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
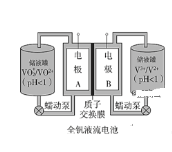
【题目】全钒液流电池是一种新型的绿色环保储能系统,工作原理如图:
离子种类 | VO2+ | VO2+ | V3+ | V2+ |
颜色 | 黄色 | 蓝色 | 绿色 | 紫色 |
(1)全钒液流电池放电时V2+发生氧化反应,该电池放电时总反应式是__________。
(2)当完成储能时,正极溶液的颜色是________
(3)质子交换膜的作用是____________
查看答案和解析>>
科目:高中化学 来源: 题型:
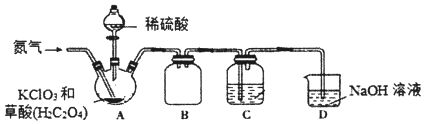
【题目】二氧化氯(C1O2)是一种黄绿色气体,沸点为11℃,不稳定,在混合气体中的体积分数大于10%就可能发生爆炸,在工业上常用作水处理剂、漂白剂。C1O2易溶于水但不与水反应,其水溶液在温度过高时有可能爆炸。某小组按照以下实验装置制备C1O2并验证其某些性质。
请回答下列问题:
(1)实验时A装置需要控制温度为60~80℃,则A装置加热的方式是___,该加热方式的优点是_____。
(2)通入氨气的主要作用有两个,一是可以起到搅拌作用,二是____。
(3)B装置的作用是___。C装置用来吸收C1O2,则C中液体易选用下列___(填序号)。
①热水 ②冰水 ③饱和食盐水
(4)装置D中C1O2与NaOH溶液反应可生成等物质的量的两种钠盐,其中一种为NaClO2,装置C中生成这两种钠盐的化学方程式为____。饱和NaClO2溶液在温度低于38℃时析出晶体NaC1O23H2O,在温度高于38℃时析出晶体NaClO2.请补充从NaClO2溶液中制得NaClO2晶体的操作步骤:a.___;b.___;c.洗涤;d.干燥。
(5)设计一个简易实验证明二氧化氯具有永久的漂白性:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)煤气化制合成气(CO和H2)
已知:C(s)+H2O(g)===CO(g)+H2(g)ΔH2=131.3kJ·mol1
C(s)+2H2O(g)===CO2(g)+2H2(g)ΔH2=90kJ·mol1
则一氧化碳与水蒸气反应生成二氧化碳和氢气的热化学方程式是_____
(2)由合成气制甲醇
合成气CO和H2在一定条件下能发生反应:CO(g)+2H2(g)![]() CH3OH(g)ΔH<0。
CH3OH(g)ΔH<0。
①在容积均为VL的甲、乙、丙、丁四个密闭容器中分别充入amolCO和2amolH2,四个容器的反应温度分别为T1、T2、T3、T4且恒定不变。在其他条件相同的情况下,实验测得反应进行到tmin时H2的体积分数如图所示,则T3温度下的化学平衡常数为_____(用a、V表示)
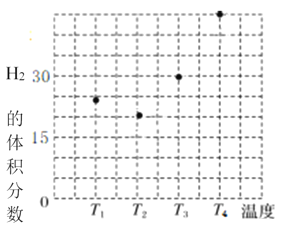
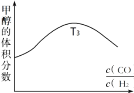
②图反映的是在T3温度下,反应进行tmin后甲醇的体积分数与反应物初始投料比![]() 的关系,请画出T4温度下的变化趋势曲线。______________
的关系,请画出T4温度下的变化趋势曲线。______________
③在实际工业生产中,为测定恒温恒压条件下反应是否达到平衡状态,可作为判断依据的是_____
A.容器内气体密度保持不变 B.CO 的体积分数保持不变
C.气体的平均相对分子质量保持不变 D.c(H2)=2c(CH3OH)
(3)由甲醇制烯烃
主反应:2CH3OH![]() C2H4+2H2O i;
C2H4+2H2O i;
3CH3OH![]() C3H6+3H2O ii
C3H6+3H2O ii
副反应:2CH3OH![]() CH3OCH3+H2O iii
CH3OCH3+H2O iii
某实验室控制反应温度为400℃,在相同的反应体系中分别填装等量的两种催化剂(Cat.1和Cat.2),以恒定的流速通入CH3OH,在相同的压强下进行甲醇制烯烃的对比研究,得到如下实验数据(选择性:转化的甲醇中生成乙烯和丙烯的百分比)
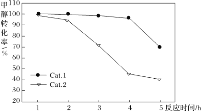
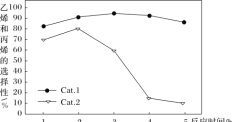
由图像可知,使用Cat.2反应2h后甲醇的转化率与乙烯和丙烯的选择性均明显下降,可能的原因是(结合碰撞理论解释)_____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环丁基甲酸是有机合成中一种有用的中间体。某研究小组以丙烯醛为原料,设计了如下路线合成环丁基甲酸。


请回答:
(1)化合物C的结构简式是 __________________。
(2)下列说法中不正确的是__________________ 。
A.化合物A能与NaHCO3溶液反应
B.化合物B和C能形成高聚物
C.化合物G的化学式为C6H8O4
D.1 mol化合物B与足量金属钠反应能生成1 mol氢气
(3)写出D + E → F的化学方程式:__________________。
(4)环丁基甲酸与苯酚反应生成一种酯X,写出化合物X满足下列条件的所有同分异构体的结构
简式:__________________
① 能使FeCl3溶液变紫色;
② 含有丙烯醛中所有的官能团;
③ 1H-NMR谱显示分子中含有5种不同化学环境的氢原子。
(5) 以1,3-丁二烯和E为原料可制备环戊基甲酸(![]() ),请你选用必要试剂,设计该合成路线。__________________
),请你选用必要试剂,设计该合成路线。__________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某新型电池,以NaBH4(B的化合价为+3价)和H2O2作原料,该电池可用作深水勘探等无空气环境电源,其工作原理如下图所示。下列说法不正确的是

A. 每消耗3mol H2O2,转移6mol e-
B. 电池工作时Na+从b极区移向a极区
C. b极上的电极反应式为:H2O2 + 2e-= 2OH-
D. a极上的电极反应式为:BH4-+ 8OH--8e-=BO2-+6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化氯(ClO2)是国内外公认的高效、广谱、快速、安全无毒的绿色消毒剂,纯ClO2易分解爆炸,其一种生产工艺如下,回答下列问题:
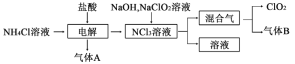
(1)气体A的名称为___________________,NCl3的电子式为_________。
(2)“电解”过程中生成的氧化产物与还原产物的物质的量之比为________。
(3)气体B能使石蕊试液显蓝色,写出NaClO2溶液和NCl3溶液在碱性条件下生成“混合气”的化学方程式____________。
(4)通常用单位质量的消毒剂得到电子的多少来衡量消毒效率的大小。C1O2和C12在消毒时自身均被还原为Cl-,则C1O2的消毒效率是Cl2的__________倍。
(5)科学家又研究出了一种新的制备C1O2的方法,反应原理如下:H2C2O4+2NaClO3+H2SO4=Na2SO4+2CO2↑+2ClO2↑+2H2O。此法提高了生产及储存、运输的安全性,原因是_____________________。若反应中转移1mol电子,则生成C1O2 ______ g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组按如图实验过程证明了海带中存在碘元素:下列说法不正确的是( )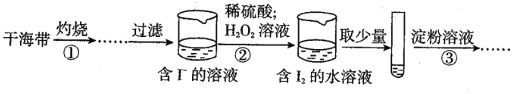
A.步骤②中发生反应的离子方程式为2I-+2H++H2O2=I2+2H2O
B.步骤③操作后,观察到试管中的溶液变为蓝色,则可说明海带中含有碘元素
C.若步骤②仅滴加稀硫酸后通入氧气,则步骤③操作后,试管中的溶液也变成蓝色
D.步骤①需要将干海带放入蒸发皿中灼烧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W为原子序数依次增大的四种短周期主族元素,A、B、C、D、E为上述四种元素中的两种或三种所组成的化合物,其中A、C、E为有机物。已知A的相对分子质量为28,B分子中含有18个电子,D分子中含有10个电子,五种化合物间的转化关系如下图所示。下列说法正确的是
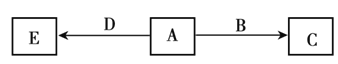
A.W是所在周期中原子半径最大的元素
B.Y的最高价氧化物的水化物为弱酸
C.X、Y、Z组成的分子中只含有极性键
D.X、Y组成的化合物的沸点一定比X、Z组成的化合物的沸点低
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com