
【题目】化学无处不在,下列与化学有关的说法正确的是( )
A. 液氨汽化时能吸收大量的热,故可用作制冷剂
B. SO2能漂白纸浆等,故可广泛用于食品的漂白
C. 味精的主要成分是蛋白质,烧菜时可加入适量
D. 氢氟酸可用于雕刻玻璃制品,这是利用酸的通性
科目:高中化学 来源: 题型:
【题目】下列各组中的两物质作用时,反应条件或反应物用量的改变,对生成物没有影响的是( )
A.Na2O2和CO2 B.Na和O2 C.NaOH 和CO2 D.C和O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将 4 molA气体和3molB气体在2L的容器中混合并在一定条件下发生如下反应:2A(g)+B(g)![]() 2C(g), 若经 2 s后测得 C的浓度为 0.6 molL-1,现有下列几种说法:
2C(g), 若经 2 s后测得 C的浓度为 0.6 molL-1,现有下列几种说法:
①用物质A 表示反应的平均速率为 0.3 molL-1s-1
②物质 B的体积分数是40%
③2 s 时物质 A 的转化率为30%
④2 s 时物质 B 的浓度为 1.0 molL-1
其中正确的是
A. ①④ B. ②③ C. ①③ D. ③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙苯( )在有机合成中占有重要的地位,有着广泛的用途。
)在有机合成中占有重要的地位,有着广泛的用途。
已知:
①![]() ΔH1=-54kJ·mol-1。
ΔH1=-54kJ·mol-1。
②![]() ΔH2=-121kJ·mol-1。
ΔH2=-121kJ·mol-1。
③H2(g)+Cl2(g)=2HCl(g) ΔH3=-185kJ·mol-1。
④相关化学键的键能数据如表所示。
化学键 | C—H | C—C | C=C | C—Cl | H—Cl |
键能/(kJ·mol-1) | 412 | 348 | x | 341 | 432 |
请回答:
(1)根据化学反应原理,缩小容器容积对反应②的影响为________。
(2)根据反应①和表中数据计算,x=________。
(3)![]()
①ΔH4=________。
②该反应正、逆反应平衡常数与温度的关系如图所示,其中表示正反应平衡常数K正的曲线为________(填“A”或“B”),理由为________。

④T1℃时,该反应的平衡常数K=________。该温度下,起始向容积为10L的容积可变的密闭容器中充入1mol![]() (g)、2molCl2(g)、1mol
(g)、2molCl2(g)、1mol![]() (g)、2molHCl(g),则开始时,v正________(填“>”“<”或“=”)v逆。
(g)、2molHCl(g),则开始时,v正________(填“>”“<”或“=”)v逆。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.控制变量法是化学实验中的—种常用方法,如表是某课外兴趣小组研究等物质的量浓度的稀硫酸和锌反应的实验数据(计算结果精确到小数点—位),分析以下数据,回答下列问题:
序号 | 硫酸的体积 /mL | 锌的质量/g | 锌的形状 | 温度/℃ | 完全溶于酸的 时间/s | 生成硫酸锌的质量/g |
① | 50.0 | 2.0 | 薄片 | 15 | 200 | m1 |
② | 50.0 | 2.0 | 薄片 | 25 | 100 | m2 |
③ | 50.0 | 2.0 | 颗粒 | 25 | 70 | m3 |
④ | 50.0 | 2.0 | 颗粒 | 35 | 35 | m4 |
⑤ | 50.0 | 2.0 | 粉末 | 25 | t1 | 5.0 |
⑥ | 50.0 | 4.0 | 粉末 | 25 | t2 | m5 |
⑦ | 50.0 | 6.0 | 粉末 | 25 | t3 | 14.9 |
⑧ | 50.0 | 8.0 | 粉末 | 25 | t4 | 19.3 |
⑨ | 50.0 | 10.0 | 粉末 | 25 | t5 | 19.3 |
(1)实验①和实验②表明_____对反应速率有影响;研究锌的形状对反应速率的影响时,最好选取实验_______ (填3个实验序号)。
(2)下列数据推断正确的是______________________。
A. t1<70 B.t1>t4 C.m12 D.m6=19.3
(3)若采用与实验①完全相同的条件,但向反应窗口中滴加少量硫酸铜溶液,发现反应速率明显加快,原因是___________________________________。
(4)根据表中数据计算:硫酸的物质的量浓度是_________________mol/L。
II.己知在 25℃、l0l kPa 下,2NO(g)+2CO(g) ![]() N2(g)+2CO2(g),现将 2molNO、2.4molCO通入恒容密闭容器中,反应过程中部分物质的浓度变化如图所示。
N2(g)+2CO2(g),现将 2molNO、2.4molCO通入恒容密闭容器中,反应过程中部分物质的浓度变化如图所示。
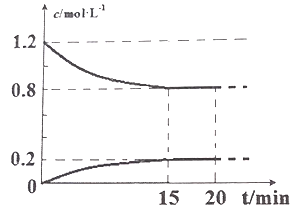
(1) 015min 内,v(CO2) =__________________。
(2)该反应的速率时间图像如下图中左图所示。若其他条件不变,仅在反应前加入合适的催化剂,其速率时间图像如下图中右图所示。以下说法正确的是______(填对应字母)。
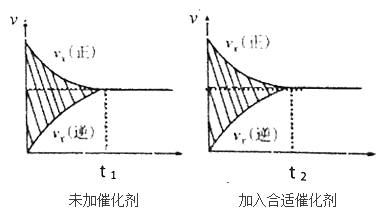
A.a1>a2 B.b12 C.t1>t2
(3) 一定条件下,己知反应NO2(g)+SO2(g) ![]() NO(g)+SO3(g),将NO2
NO(g)+SO3(g),将NO2
a.体系压强保持不变 b.混合气体颜色保持不变
c.NO2与SO2的体积比保持不变 d.每消耗lmol SO2的同时生成lmol NO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:CH3CH2OH+NaBr+H2SO4(浓)![]() CH3CH2Br+NaHSO4+H2O。实验室制备溴乙烷(沸点为38.4℃)的装置和步骤如下:
CH3CH2Br+NaHSO4+H2O。实验室制备溴乙烷(沸点为38.4℃)的装置和步骤如下:
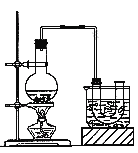
①按下图所示连接仪器,检查装置的气密性,然后向U形管和大烧杯里加入冰水;②在圆底烧瓶中加入10mL95%乙醇、28mL浓硫酸,然后加入研细的13g溴化钠和几粒碎瓷片;③小火加热,使其充分反应。
(1)反应时若温度过高可看到有红棕色气体产生,该气体的化学式为 。
(2)为了更好的控制反应温度,除用图示的小火加热,更好的加热方式是____ ______。
(3)反应结束后,U形管中粗制的溴乙烷呈棕黄色。将U形管中的混合物倒入分液漏斗中,静置,待液体分层后,分液,取下层液体。为了除去其中的杂质,可选择下列试剂中的 (填序号)。
A.Na2SO3溶液 B.H2O C.NaOH溶液 D.CCl4
(4)要进一步制得纯净的C2H5Br,可再用水洗,然后加入无水CaCl2干燥,再进行 (填操作名称)。
(5)下列几项实验步骤,可用于检验溴乙烷中的溴元素,其正确的操作顺序是:取少量溴乙烷,然后 (填序号)。
①加入AgNO3溶液 ②加入稀HNO3酸化③冷却④加热⑤加入NaOH溶液上述实验过程中C2H5Br发生的反应方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定量的甲烷在O2不足的情况下燃烧,得到CO、CO2和H2O的总质量为14.4 g,若其中水的质量为7.2 g,则CO的质量是( )
A.2.8g B.4.4g C.5.6g D.在2.8 g~5.6 g之间
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人体吸入CO后在肺中发生反应![]() 导致人体缺氧。向某血样中通 入CO与O2的混合气
导致人体缺氧。向某血样中通 入CO与O2的混合气![]() ,氧合血红蛋白 HbO2浓度随时间变化曲线如下图所示。下列说法正确的是
,氧合血红蛋白 HbO2浓度随时间变化曲线如下图所示。下列说法正确的是

A. 反应开始至4s内用HbO2表示的平均反应速率为![]()
B. 反应达平衡之前,O2与HbCO的反应速率逐渐减小
C. 将CO中毒病人放入高压氧舱治疗是利用了化学平衡移动原理
D. 该温度下反应![]() 的平衡常数为107
的平衡常数为107
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com