
| A、①② | B、②③ | C、③④ | D、①④ |


 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案 应用题作业本系列答案
应用题作业本系列答案科目:高中化学 来源: 题型:
| A、0.3mol |
| B、0.05mol |
| C、0.2mol |
| D、0.1mo |
查看答案和解析>>
科目:高中化学 来源: 题型:
 按如图装置持续通入X气体,并在管口点燃,实验结果使澄清的石灰水变浑浊,则X、Y不可以是( )
按如图装置持续通入X气体,并在管口点燃,实验结果使澄清的石灰水变浑浊,则X、Y不可以是( )| A、H2和NaHCO3 |
| B、CO和Na2CO3 |
| C、CO和CuO |
| D、H2和CaCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该反应为吸热反应 |
| B、CO2分子中的化学键为非极性键 |
| C、HCHO分子中含σ键又含π键 |
| D、每生成1.8 g H2O消耗2.24 L O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
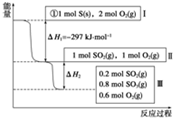 恒温,容积为1L恒容条件下,硫可以发生如下转化,其反应过程和能量关系如图所示(已知:2SO2(g)+O2(g)?2SO3(g)△H=-196.6kJ?mol-1),请回答下列问题:
恒温,容积为1L恒容条件下,硫可以发生如下转化,其反应过程和能量关系如图所示(已知:2SO2(g)+O2(g)?2SO3(g)△H=-196.6kJ?mol-1),请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
A、在粗硅的制取中发生反应2C+SiO2
| ||||
| B、由“HF比HCl稳定性好”,可推知HF比HCl沸点高 | ||||
| C、由“同温度下等浓度的Na2CO3溶液比Na2SO4溶液的pH大”,可推知C比S的非金属性弱 | ||||
| D、由“某过程发生化学键断裂”,可推知该过程发生了化学变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、P(NH3)>P(H2)>P(O2) |
| B、P(O2)>P(NH3)>P(H2) |
| C、P(H2)>P(O2)>P(NH3) |
| D、P(H2)>P(NH3)>P(O2) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com