
【题目】如图为不同化学元素组成的化合物示意图,下列说法正确的是( )
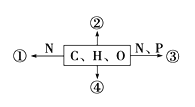
A. 若图中①为某种化合物的基本单位,则①最可能是核苷酸
B. 若②广泛分布在动物细胞内,则其一定是糖原
C. 若③为生物大分子,则其彻底水解产物最多为4种
D. 若④为重要储能物质,则动物和植物细胞都含有这种物质
科目:高中化学 来源: 题型:
【题目】R、X、Y、Z是短周期元素,原子序数依次增大。X的原子序数是R的2倍,R的原子最外层电子数是X的2倍。Z的最高价氧化物对应的水化物(M)是强电解质,向Y的钠盐溶液中滴加M溶液,产生沉淀的物质的量与M的物质的量关系如图所示。下列推断正确的是

A. R的氢化物可能使溴水或酸性高锰酸钾溶液褪色
B. Y的气态氢化物热稳定性比R的强
C. 常温常压下,Z的单质一定呈黄绿色
D. X和Z组成的化合物属于共价化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“生活无处不化学”,请你回答下列问题。
(1)食盐不慎洒落在天然气的火焰上,观察到现象是______,该变化称为______反应。
(2)沾有水的铁制器皿在高温火焰上会发黑,该反应的化学方程式是_______。
(3)小苏打(碳酸氢钠)可用于中和过多的胃酸,写出该反应的离子方程式______。
(4)使用“84”消毒液(含 NaClO)时,按一定比例与水混合,并在空气中浸泡一段时间,使 NaClO 与H2O及空气中的CO2充分 反应,目的是得到杀菌消毒效果更好的______(填物质名称),该反应的离子方程式:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将Mg、Al、Zn组成的混合物与足量的盐酸作用,放出H2的体积为2.8L(标准状况下),则这三种金属的物质的量之和可能为
A. 0.250mol B. 0.100mol C. 0.125mol D. 0.080mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁是人类较早使用的金属之一。运用铁及其化合物的知识,完成下列问题。
(1)所含铁元素既有氧化性又有还原性的物质是 ________(用字母代号填)。
A.Fe B.FeCl3C.FeSO4 D.Fe2O3
(2)向沸水中逐滴滴加1 mol/L FeCl3溶液,至液体呈透明的红褐色,该分散系中粒子直径的范围是 ________nm。
(3)电子工业需要用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出FeCl3溶液与铜反应的离子方程式:_________________________________________________________。
某校同学为测定FeCl3腐蚀铜后所得溶液的组成,进行了如下实验:
首先取少量待测溶液,滴入KSCN溶液呈红色,则溶液中含有的金属阳离子是_________________________,在此基础上,又进行了定量组成的测定:取50.0mL待测溶液,向其中加入足量的AgNO3溶液,得白色沉淀,过滤、干燥、称量,沉淀质量为43.05 g.溶液中c(Cl-)= mol/L.
(4)若要验证该溶液中含有Fe2+,正确的实验方法是 。
A.向试管中加入试液,滴入KSCN溶液,若显血红色,证明含有Fe2+。
B.向试管中加入试液,滴入酸性高锰酸钾溶液,若褪色,证明含有Fe2+。
C.向试管中加入试液,滴入氯水,再滴入KSCN溶液,若显血红色,证明原溶液中含有Fe2+
(5)欲从废水中回收铜,并重新获得FeCl3溶液设计实验方案如下:

A请写出上述实验中加入或生成的有关物质的化学式:
①_____________②____________③______________④________________
B请写出通入⑥的化学方程式__________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用废旧锂离子电池的正极材料,主要成分为 LiCoO2(难溶于水)还含有 Al以及少量 Ca、Mg、Cu、Fe 等。制备 Co3O4 微球的工艺流程如下:
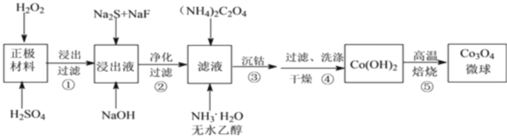
回答下列问题:
(1)LiCoO2 中 Co 元素的化合价为______。
(2)配平步骤①中生成 Co2+的离子方程式为_____LiCoO2 +____H++_____H2 O2 =_____Co2++_____O2 ![]() +_____Li++_____H 2O此过程中若用浓盐酸代替 H2SO4 和 H2O2的混合溶液,除因挥发使其利用率降低外,还有的缺点是_____。
+_____Li++_____H 2O此过程中若用浓盐酸代替 H2SO4 和 H2O2的混合溶液,除因挥发使其利用率降低外,还有的缺点是_____。
(3)步骤②中,不同 pH 下溶液中金属离子的去除效果如下图所示。该过程加入NaOH调节溶液 pH 的最佳范围是______,理由是______。
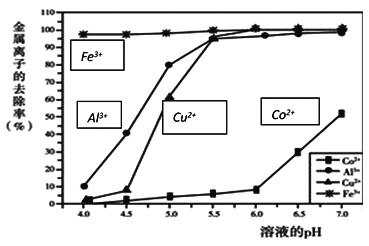
(4)步骤④中,过滤、洗涤操作均需用到的玻璃仪器有烧杯、玻璃棒、_____。
(5)步骤⑤中,Co(OH)2 在空气中高温焙烧生成 Co3O4 的化学方程式为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知伞形酮可用雷琐苯乙酮和苹果酸在一定条件下反应制得。

下列说法中正确的是
A. 一分子雷琐苯乙酮含有3个碳碳双键
B. 苹果酸的一种缩聚产物是![]()
C. 1mol伞形酮与足量NaOH溶液反应,最多可消耗2mol NaOH
D. 雷琐苯乙酮、苹果酸、伞形酮都能跟FeCl3溶液发生显色反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从海水中可以获得淡水、食盐,并可提取镁和溴等物质。流程如下图所示:
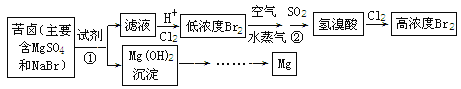
(1)用电子式表示Br2的形成过程________。提取Br2 时,第一次通入Cl2 后发生反应的离子方程式是_______;ⅦA族元素,非金属性随元素核电荷数增加而逐渐减弱的原因:同主族元素从上到下原子半径逐渐______(填“增大”或“减小”),得电子能力逐渐减弱。②中SO2表现 _________(填“氧化”“还原”“酸”“碱”)性;
(2)镁在元素周期表中的位置是________;为了实现对镁离子的富集,①中分离提纯的实验操作名称是__________;
(3)用MgCl2溶液制成无水MgCl2,加热溶液过程中,会生成Mg(OH)Cl溶液和一种酸性气体。写出该反应的化学方程式______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com