
【题目】根据下列实验操作和现象所得出的结论正确的是
选项 | 实验操作 | 实验现象 | 结论 |
A | 向硅酸钠溶液中滴加盐酸 | 有白色胶状沉淀生成 | 非金属性:Cl>Si |
B | 向溶液X中加入稀盐酸,并将产生的无色无味气体通入澄清石灰水中 | 生成白色沉淀 | 溶液X中一定含有CO32-或HCO3- |
C | 向1mL0.1mol/L MgSO4溶液中,滴入2滴0.1mol/L1NaOH溶液,再滴入2滴0.1mol/LCuSO4溶液 | 起初生成的白色沉淀逐渐变为蓝色沉淀 | Ksp[Cu(OH)2] <Ksp[Mg(OH)2] |
D | 向鸡蛋白溶液中滴入HgCl2溶液 | 有白色沉淀 | 蛋白质发生盐析 |
A. A B. B C. C D. D
【答案】BC
【解析】A,向硅酸钠溶液中滴加盐酸有白色胶状沉淀生成,说明发生反应:Na2SiO3+2HCl=H2SiO3↓+2NaCl,根据“强酸制弱酸”的复分解反应规律,酸性:HCl![]() H2SiO3,HCl不是Cl元素的最高价含氧酸,无法比较Cl与Si的非金属性强弱,A项错误;B,向溶液X中加入稀盐酸,产生无色无味气体通入澄清石灰水中产生白色沉淀,该无色无味的气体为CO2,溶液X中一定含有CO32-或HCO3-,B项正确;C,向1mL0.1mol/L MgSO4溶液中,滴入2滴0.1mol/L1NaOH溶液,产生白色Mg(OH)2沉淀,同时MgSO4过量,再滴入2滴0.1mol/LCuSO4溶液,白色沉淀逐渐变为蓝色沉淀,说明白色Mg(OH)2沉淀转化为蓝色Cu(OH)2沉淀,Cu(OH)2比Mg(OH)2更难溶于水,Ksp[Cu(OH)2]
H2SiO3,HCl不是Cl元素的最高价含氧酸,无法比较Cl与Si的非金属性强弱,A项错误;B,向溶液X中加入稀盐酸,产生无色无味气体通入澄清石灰水中产生白色沉淀,该无色无味的气体为CO2,溶液X中一定含有CO32-或HCO3-,B项正确;C,向1mL0.1mol/L MgSO4溶液中,滴入2滴0.1mol/L1NaOH溶液,产生白色Mg(OH)2沉淀,同时MgSO4过量,再滴入2滴0.1mol/LCuSO4溶液,白色沉淀逐渐变为蓝色沉淀,说明白色Mg(OH)2沉淀转化为蓝色Cu(OH)2沉淀,Cu(OH)2比Mg(OH)2更难溶于水,Ksp[Cu(OH)2]![]() Ksp[Mg(OH)2],C项正确;D,HgCl2属于重金属盐,向鸡蛋白溶液中滴入HgCl2溶液,产生白色沉淀,蛋白质发生了变性,D项错误;答案选BC。
Ksp[Mg(OH)2],C项正确;D,HgCl2属于重金属盐,向鸡蛋白溶液中滴入HgCl2溶液,产生白色沉淀,蛋白质发生了变性,D项错误;答案选BC。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】标准状况下V L氨气溶解在1 L水中(水的密度近似为1 g·mL-1),所得溶液的密度为ρ g·mL-1,质量分数为w,物质的量浓度为c mol·L-1,则下列关系中不正确的是
A. ρ=![]() B. w=
B. w=![]()
C. w=![]() D. c=
D. c=![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计了以下流程来检验碳酸钠粉末中可能含有少量氯化钠和氢氧化钠中的一种或两种杂质。

(1)步骤1所需玻璃仪器是_________;步骤3的操作名称是____________。
(2)对检验碳酸钠粉末中可能含有的杂质提出合理假设:
假设1:只含有氯化钠;
假设2:只含有____________;
假设3:氯化钠和氢氧化钠都含有。
(3)设计实验方案,进行实验。
限选以下试剂:氯化钡溶液、硝酸钡溶液、酚酞试液、稀硝酸、稀盐酸、稀硫酸、硝酸银溶液。回答下列问题:
①加入过量试剂A的名称是___________。
②填写下表:______
实验步骤 | 预期现象和结论 |
步骤4: | ①若,则假设成立 ②若,则成立 |
步骤5: |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】鉴别固体Na2CO3和NaHCO3的最好方法是( )
A.分别与同浓度的稀盐酸反应
B.分别加入NaOH溶液
C.分别加入石灰水
D.溶于水,比较其溶解性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酸浸法制取硫酸铜的流程示意图如下

(1)步骤(i)中Cu2(OH) 2CO3 发生反应的化学方程式为______________________。
(2)步骤(ii)所加试剂起调节pH 作用的离子是___________________(填离子符号)。
(3)在步骤(iii)发生的反应中,1 mol MnO2转移2 mol 电子,该反应的离子方程式为______________________。
(4)步骤(iv)除去杂质的化学方程式可表示为:3Fe3++NH4++2SO42-+6H2O=NH4Fe3(SO4)2(OH)6+6H+过滤后母液的pH=2.0,c(Fe3+)=a mol·L-1,c (NH4+)=b mol·L-1,c(SO42-)= d mol·L-1,该反应的平衡常数K=__________(用含a 、b 、d 的代数式表示)。
(5)化学镀的原理是利用化学反应生成金属单质沉积在镀件表面形成镀层。
① 若用CuSO4进行化学镀铜,应选用 ______________(填“氧化剂”或“还原剂”)与之反应。
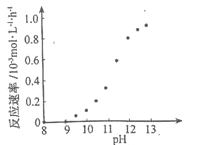
② 某化学镀铜的反应速率随镀液pH 变化如图所示。该镀铜过程中,镀液pH 控制在12.5左右。据图中信息,给出使反应停止的方法:_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将过量的氨水加到硫酸铜溶液中,溶液最终变成深蓝色,继续加入乙醇,析出深蓝色的晶体[Cu(NH3)4]SO4H2O。
(1)Cu2+价电子排布式为_______;[Cu(NH3)4]SO4H2O中,1mol[Cu(NH3)4]2+含有σ键的数目为_____。
(2)SO42-中S原子轨道杂化类型为_____,H2O与H+以配位键形成H3O+,则H3O+的空间构型为____(用文字描述)。
(3)N、O、S第一电离能由大到小的顺序为___________。
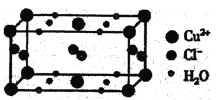
(4)某含有结晶水的铜的氯化物的晶胞结构如图所示,该化合物的化学式是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A.将煤在空气中加强热使其分解叫做煤的干馏
B.石油的分馏、裂化、裂解均为化学变化
C.向鸡蛋清溶液中滴加CuSO4溶液析出固体,加入足量蒸馏水后固体不能重新溶解
D.油脂、糖类、蛋白质都是天然有机高分子化合物,都可以发生水解反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com