
【题目】下列关于有机物说法正确的是( )
A.CH3Cl、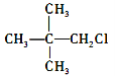 、
、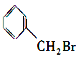 中加入 NaOH 的醇溶液共热,然后加入稀硝酸呈酸性,再滴入 AgNO3 溶液,均有沉淀生成
中加入 NaOH 的醇溶液共热,然后加入稀硝酸呈酸性,再滴入 AgNO3 溶液,均有沉淀生成
B.CH3Cl 中加入 NaOH 的水溶液共热,再滴入 AgNO3溶液,可检验该物质中含有的卤素原子
C.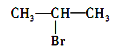 发生消去反应得到两种烯烃
发生消去反应得到两种烯烃
D.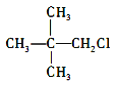 与 NaOH 的水溶液共热,反应后生成的醇能被氧化为醛
与 NaOH 的水溶液共热,反应后生成的醇能被氧化为醛
科目:高中化学 来源: 题型:
【题目】近日,我国科研团队研发出一种蓝藻人造叶片系统,其核心是一种可以向细胞外分泌蔗糖的蓝藻,其工作原理如图。下列说法不正确的是
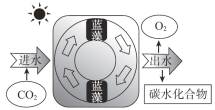
A. 该系统利用了蓝藻的光合作用
B. 理论上,系统出水量小于进水量
C. 可用银氨溶液检验产物中是否含蔗糖
D. 该系统有望为人类探索太空时解决生存难题提供新思路
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知 2Na + 2H2O = 2NaOH + H2↑,该反应中相关物质的化学用语中正确的是
A.H2 的结构式:H-H
B.中子数为 12 的钠原子:![]()
C.H2O 的电子式:![]()
D.Na+的结构示意图:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室常用浓硫酸和乙醇混合加热制取乙烯,下列说法正确的个数是( )

①浓硫酸只作催化剂
②在反应容器中放入几片碎瓷片防止混合液暴沸
③反应温度缓慢上升至 170℃
④用排水法或向下排气法收集乙烯
⑤圆底烧瓶中装的是 4mL 乙醇和 12mL 3mol/L H2SO4混合液
⑥温度计应插入反应溶液液面下,以便控制温度
⑦反应完毕后先熄灭酒精灯,再从水中取出导管
⑧该反应类型属于取代反应
⑨若 a 口出来的气体使酸性 KMnO4溶液褪色,说明有乙烯生成
A.1B.2C.3D.4 种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机玻璃(PMMA)是一种具有优良的光学性、耐腐蚀性的高分子聚合物,其合成路线之一如图所示:

请回答下列问题:
(1)写出检验A中官能团所需试剂及现象__、__。
(2)用系统命名法给B命名__。
(3)写出C与足量的NaOH乙醇溶液,在加热条件下反应的化学方程式__。
(4)写出E生成PMMA反应的化学方程式__。
(5)下列说法正确的是__。
a.B的核磁共振氢谱有3组峰,峰面积比为6∶1∶1
b.B→C的反应类型为取代反应
c.D中存在顺反异构
d.1molPMMA发生水解反应时消耗1molNaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将等物质的量的A、B混合于2 L的密闭容器中,发生下列反应2A(g) + B(g) ![]() xC(g) + 2D(g),经4min后达平衡,测得D的浓度为1.0 mol·L-1,c(A) : c(B)=2 : 3,以C表示的平均速率υ(C)=0.125 mol·L-1·min-1,下列说法不正确的是
xC(g) + 2D(g),经4min后达平衡,测得D的浓度为1.0 mol·L-1,c(A) : c(B)=2 : 3,以C表示的平均速率υ(C)=0.125 mol·L-1·min-1,下列说法不正确的是
A. 反应速率υ(A)=0.25 mol·L-1·min-1
B. 该反应方程式中,x=1
C. 4 min时,B的物质的量为2 mol
D. 该反应的平衡常数K=1/3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知反应2HI(g)=H2(g) + I2(g)的△H=+11kJ·mol-1,1molH2(g)、1molI2(g)分子中化学键断裂时分别需要吸收436KJ、151KJ的能量,则1molHI(g)分子中化学键断裂时需吸收的能量为___kJ。
(2)已知某密闭容器中存在下列平衡:CO(g)+H2O(g) ![]() CO2(g)+H2(g),CO的平衡物质的量浓度c(CO)与温度T的关系如图所示。
CO2(g)+H2(g),CO的平衡物质的量浓度c(CO)与温度T的关系如图所示。

①该反应△H__________ 0(填“>”或“<”)
②若T1、T2时的平衡常数分别为K1、K2,则K1_______K2(填“>”、“<”或“=”)。
③T3时在某刚性容器中按1:2投入CO(g)和H2O(g),达到平衡后测得CO的转化率为75%,则T3时平衡常数K3=____________。
(3)在恒容密闭容器中,加入足量的MoS2和O2,仅发生反应: 2MoS2(s)+7O2(g) ![]() 2MoO3(s)+4SO2(g) ΔH。
2MoO3(s)+4SO2(g) ΔH。
测得氧气的平衡转化率与起始压强、温度的关系如图所示:

①p1、p2、p3的大小:_________。
②若初始时通入7.0 mol O2,p2为7.0 kPa,则A点平衡常数Kp=________(用气体平衡分压代替气体平衡浓度计算,分压=总压×气体的物质的量分数,写出计算式即可)。
(4)中科院兰州化学物理研究所用Fe3(CO)12/ZSM-5催化CO2加氢合成低碳烯烃反应,所得产物含CH4、C3H6、C4H8等副产物,反应过程如图。

催化剂中添加Na、K、Cu助剂后(助剂也起催化作用)可改变反应的选择性,在其他条件相同时,添加不同助剂,经过相同时间后测得CO2转化率和各产物的物质的量分数如下表。
助剂 | CO2转化率(%) | 各产物在所有产物中的占比(%) | ||
C2H4 | C3H6 | 其他 | ||
Na | 42.5 | 35.9 | 39.6 | 24.5 |
K | 27.2 | 75.6 | 22.8 | 1.6 |
Cu | 9.8 | 80.7 | 12.5 | 6.8 |
①欲提高单位时间内乙烯的产量,在Fe3(CO)12/ZSM-5中添加_______助剂效果最好;加入助剂能提高单位时间内乙烯产量的根本原因是_____;
②下列说法正确的是______;
a 第ⅰ步所反应为:CO2+H2![]() CO+H2O
CO+H2O
b 第ⅰ步反应的活化能低于第ⅱ步
c 催化剂助剂主要在低聚反应、异构化反应环节起作用
d Fe3(CO)12/ZSM-5使CO2加氢合成低碳烯烃的ΔH减小
e 添加不同助剂后,反应的平衡常数各不相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。

试回答下列问题:
(1)h的单质在空气中燃烧发出耀眼的白光,请用原子结构的知识解释发光的原因:_____ 。
(2)o、p两种元素的部分电离能数据如下表所示:
元素 | o | p | |
电离能/ |
| 717 | 763 |
| 1509 | 1561 | |
| 3248 | 2957 | |
比较两元素的![]() 、
、![]() 可知,气态
可知,气态![]() 再失去一个电子比气态
再失去一个电子比气态![]() 再失去一个电子难。对此,你的解释是 ___________。
再失去一个电子难。对此,你的解释是 ___________。
(3)表中所列的某主族元素的电离能情况如图所示,则该元素是上述元素中的____(填元素符号)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某科研课题小组研究利用含H+、Zn2+、Mn2+、Fe2+、Fe3+、Cl-、SO42-的工业废液,制备高纯的ZnO、MnO2、Fe2O3,设计出如下实验流程:

已知:
①氢氧化锌沉淀呈白色
②氢氧化锰难溶于水
③溶液中金属离子沉淀完全时,其浓度![]()
回答下列问题:
(1)向工业废液中加入双氧水,可能观察到的现象有:溶液的颜色发生变化和_____,其中引起溶液颜色变化的离子方程式为_____。
(2)第一次调pH的目的是沉淀Fe3+。 检验Fe3+是否完全沉淀的操作:取少量滤液于洁净试管中,最好加入下列试剂中的____ (填标号),并观察实验现象。
a.稀氨水 b.KSCN溶液 c.K3Fe(CN)6溶液
(3)第二次调pH前,科研小组成员在室温下分析此时的溶液,得到相关数据见下表

为防止Mn2+也同时沉淀造成产品不纯,最终选择将溶液的pH控制为7.5,则此时溶液中Zn2+ 的沉淀率为____ 。 (第二次调pH前后液体体积的变化忽略不计)
(4)已知常温下,![]() 。在除锌时发生沉淀转化反应为
。在除锌时发生沉淀转化反应为![]() ,其平衡常数K= ___。
,其平衡常数K= ___。
(5)沉锰反应在酸性条件下完成,写出反应的离子方程式____。
(6)下列关于沉锰制备高纯MnO2的说法中,不正确的是____ (填标号)。
a.若沉锰反应时加入足量浓盐酸并加热,MnO2的产率将降低
b.若沉锰后进行过滤操作,为了加快过滤速率,不断用玻璃棒搅拌
c.若除锌时加入MnS质量为xg,沉锰反应中锰元素无损失,MnO2的产量将增加xg
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com